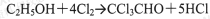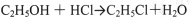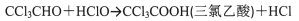-
某化学学习小组设计如图实验装置(夹持和加热装置略去)制备Cl2,并探究氯气的相关性质。

回答下列问题:
⑴ 装置中a玻璃仪器的名称为_____________;整套装置装配完毕后,首先进行的操作是______________,再添加试剂。
⑵ 若A装置中的固体药品为MnO2,其化学方程式为_______________________。若A装置中的固体药品为KClO3,则反应中每生成1 mol Cl2时转移电子的物质的量为_________mol(结果保留两位小数)。
⑶ 装置C的作用是验证氯气是否具有漂白性,Ⅰ处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是_________、_____________。
⑷ 设计装置D、E的目的是比较氯、溴、碘的非金属性。但有同学认为该设计不够严密,他的理由可能是_____________。
⑸ 甲同学提出,装置F中改用过量的Na2SO3溶液,乙同学认为此法不可行。请用离子方程式解释乙认为不可行的原因:_____________。
-
某化学兴趣小组为探究氯气的性质并用Cl2制备HClO,设计如下实验方案,请回答下列问题:
实验一:性质探究
设计图3实验装置来制备并验证氯气的性质,部分夹持设计未画出。
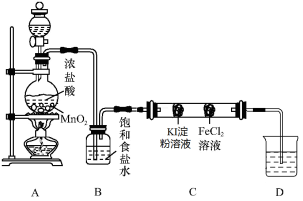
图3
(1)请写出装置A中制备氯气的反应化学方程式______________________;
(2)装置B的作用是______________________;
(3)双通管C中事先装有两个沾有相关试剂的棉球,实验现象为_____________;
实验二:制备HClO
(4)设计图4所示装置E代替图3中的装置C,用于制备较高浓度的HClO溶液。在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙。
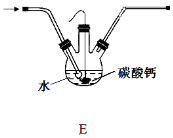
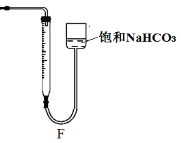
图4
①该方案反应后所得的溶液中HClO浓度比氯水中大的原因是_______________
②反应结束后将塑料网中剩余的石灰石提出液面,所得的溶液与稀盐酸混合,立即产生大量CO2气体,则反应所得溶液中的溶质除CaCl2、HClO外,还含有__________
③该小组同学测得反应中碳酸钙质量减少a g,反应后从所得的100mL溶液中取用10mL与稀盐酸混合,连接F装置测得产生的气体体积为b L(已换算成标准状况),则原溶液中CaCl2的浓度为 mol·L-1(用含a、b的代数式表示,可不必化简)。
-
某化学学习小组设计如图实验装置(夹持装置略去)制备氯气并探究氯气的相关性质。D装置为分液漏斗形状,低进高出。
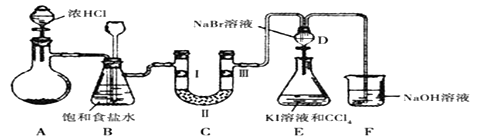
(1)若A装置中固体药品为MnO2,写出其离子反应方程式_________;若A装置中固体药品为KC1O3,则反应中每生成1 mol Cl2时转移电子数目为_______________。
(2)装置B的作用是______和________,若C处发生了堵塞,则B中的现象__________。
(3)装置C的作用是验证氯气是否具有漂白性,I处是湿润的有色布条,则II、III处应加入的物质分别是__________和__________。
-
某校化学兴趣小组为研究Cl2单质的性质,设计如图所示装置进行实验.装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸.
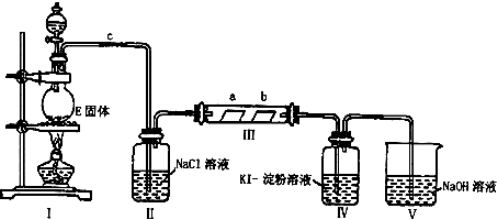
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式是: ;
(2)加入药品前,检查Ⅰ中气体发生装置气密性的操作是:  ;
;
(3)装置Ⅱ的作用是 ;
(4)实验过程中,装置Ⅳ中的实验现象为 ;发生反应的化学方程式为 ;
(5)实验结束后,该组同学在装置Ⅲ中观察b的红色退去,但是并未观察到“a无明显变化”这一预期现象,为了达到这一目的,你认为应在 之间还需添加洗气瓶(选填装置序号),该装置的作用是 ;
(6)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式 .
-
铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠
制取装置如图(加热和夹持仪器已略去),部分物质性质如下:
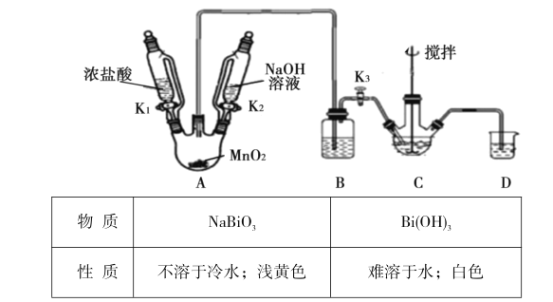
(1)C中盛放Bi(OH)3与NaOH的混合物,与Cl2反应生成NaBiO3,反应的化学方程式为__。B装置的作用是__。
(2)当观察到__(填现象)时,可以初步判断C中反应已经完成。
(3)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭__;打开__。
(4)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有_。
Ⅱ.铋酸钠的应用——检验Mn2+
(5)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+。产生紫红色现象的离子方程式为__。
Ⅲ.产品纯度的测定
(6)取上述NaBiO3产品ag,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用bmo1•L-1的H2C2O4标准溶液滴定生成的MnO4-(已知:H2C2O4+MnO4-—CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗cmL标准溶液。该产品的纯度为__(用含a、b、c的代数式表示)。
-
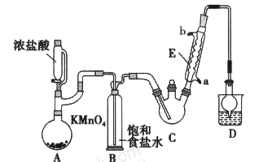
某化学兴趣小组设计如图所示装置(夹持、加热仪器略),模拟工业生产三氯乙醛(CCl3CHO)的方法,由乙醇与氯气作用,制得三氯乙醛。
查阅资料,有关信息如下:
①制备反应原理: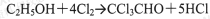
可能发生的副反应: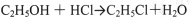
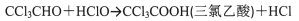
②相关物质的相对分子质量及部分物理性质:
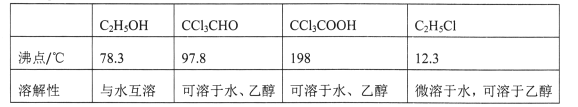
(1)仪器C和E的名称分别是____,____。
(2)仪器A中发生反应的离子方程式为____ 。
(3)该装置C最好采用____加热的方法,以控制反应温度在70℃左右。
(4)该设计流程中存在一处缺陷,该缺陷可能引起的后果是________。
(5)反应结束后,从C中的混合物中分离出CCl3COOH的方法是_____(填名称)。
-
某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去)。请回答下列问题:
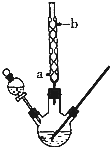
(1)水从冷凝管 __(填“a”或“b”)处进入。
__(填“a”或“b”)处进入。
(2)已知下列数据:
| 乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 |
| 熔点/℃ | ﹣117.3 | 16.6 | ﹣83.6 | ﹣ |
| 沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
又知温度高于140℃时发生副反应:2CH3CH2OH CH3CH2OCH2CH3+H2O,该副反应属于___反应(填字母)。
CH3CH2OCH2CH3+H2O,该副反应属于___反应(填字母)。
a.加成 b.取代 c.酯化 d.氧化
(3)将反应后的混合液缓缓倒入盛有足量饱和碳酸钠溶液的烧杯中,搅拌、静置。上述实验中饱和碳酸钠溶液的作用是(填字母):__。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(4)上述(3)中欲分离出乙酸乙酯,应使用的分离方法是__(填操作方法名称,下同),进行此步操作后,所得有机层中的主要无机物杂质是水,在不允许使用干燥剂的条件下,除去水可用__的方法。
(5)若实验所用乙酸质量为6.0g,乙醇质量为5.0g,得到纯净的产品质量为4.4g,则乙酸乙酯的产率是__。
(6)乙二酸和乙二醇也能发生酯化反应,写出生成环酯的化学反应方程式___。
-
某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去).请回答下列问题:
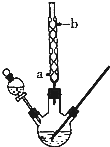
(1)水从冷凝管的______(填“a”或“b”)处进入。
(2)已知下列数据:
| 乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 |
| 熔点/℃ | ﹣117.3 | 16.6 | ﹣83.6 | ﹣ |
| 沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
又知温度高于140℃时发生副反应:2CH3CH2OH→CH3CH2OCH2CH3+H2O
①该副反应属于__________反应(填字母)。
a.加成 b.取代 c.酯化
②考虑到反应速率等多种因素,用上述装置制备乙酸乙酯时,反应的最佳温度范围是______(填字母)。
a.T<77.5℃ b.T>150℃ c.115℃<T<130℃
(3)上述实验中饱和碳酸钠溶液的作用是(填字母):___________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(4)欲分离出乙酸乙酯,应使用的分离方法是__________(填操作方法名称,下同),所用到的仪器为______ , 进行此步操作后,所得有机层中的主要无机物杂质是水,在不允许使用干燥剂的条件下,除去水可用____________的方法。
(5)若实验所用乙酸质量为6.0g,乙醇质量为5.0g,得到纯净的产品质量为4.4g,则乙酸乙酯的产率是_______。
(6)乙二酸和乙二醇也能发生酯化反应,写出生成环酯的化学反应方程式____________________。
-
CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
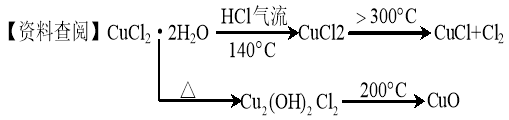
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。
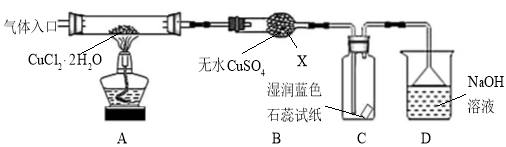
请回答下列问题:
(1)仪器X的名称是 。
(2)实验操作的先后顺序是
 (填操作的编号)。
(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
(4)装置D中发生的氧化还原反应的离子方程式是 。
【探究反思】
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
-
Ⅰ.CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl·2H2O制备CuCl,并进行相关探究。
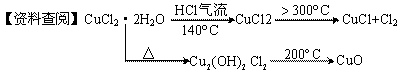
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。
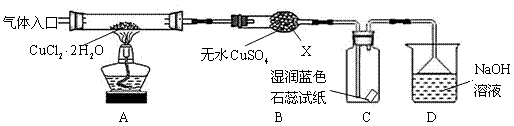
请回答下列问题:
(1)仪器X的名称是 ;
(2)实验操作的先后顺序是 →e(填操作的编号)。
→e(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
【探究反思】
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
Ⅱ.某试液中只可能含有下列K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1 mol·L-1。某同学进行了如下实验:
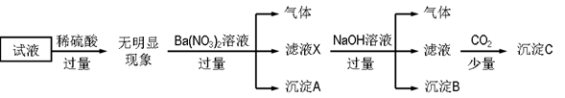
(1)根据实验现象判断,滤液X中大量存在的阳离子有 ;
(2)沉淀A的化学式 ;沉淀B的化学式 ;
(3)沉淀C的成分 (填“能”或“不能”)确定。若能确定,写出化学式 ;若不能,说明理由 。
(4)该溶液中一定存在的离子是 ;一定不存在的离子是 。