-
(1)试管Ⅰ和Ⅱ中分别加入3 mL稀盐酸(均足量),再将装0.3 g NaHCO 3和0.3 g Na2CO3粉末的小气球分别套在试管Ⅰ和Ⅱ的管口。将气球内的 NaHCO3和Na2CO3同时倒入试管中,请回答下列问题:
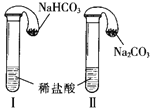
①试管Ⅰ中发生反应的离子方程式为________。
②加入固体后,试管_______(填 “Ⅰ”或“Ⅱ”)上的气球膨胀较快。
(2)为研究Na2CO3、NaHCO3与盐酸的反应是吸热反应还是放热反应,某同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 | 35 mL试剂 | 固体 | 混合前温度/℃ | 混合后温度/℃ |
| ① | 水 | 2.5 g NaHCO3 | 20.0 | 18.5 |
| ② | 水 | 3.2 g Na2CO3 | 20.0 | 24.3 |
| ③ | 盐酸 | 2.5 g NaHCO3 | 20.0 | 16.2 |
| ④ | 盐酸 | 3.2 g Na2CO3 | 20.0 | 25.1 |
①设计1、2组实验的目的是:_______。
②通过上述实验可得出:NaHCO3溶液和盐酸的反应是_____反应,对应的图像为______。
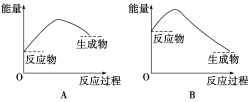
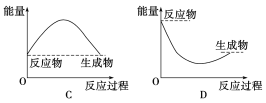
-
原高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸,将两个各装有0.3g NaHCO3或 Na2CO3粉末的小气球分别套在两支试管口,将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下:
(1)两支试管均产生大量气体,投入________的试管中气体产生较快,投入________的试管中气球变得更大(以上均填化学式).
(2)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度有升高.由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应.甲同学写出了下列热化学方程式(其中“aq”的含义是表示水溶液):HCO3-(aq)+H+(aq)=H2O(l)+CO2(g)△H>0 CO32-(aq)+2H+(aq)=H2O(l)+CO2(g)△H<0
甲下结论的方法是否正确________(填“正确”或“不正确”);为研究是吸热还是放热反应,乙同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高
或最低温度 |
| ① | 35mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 3.2Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10ml水 | 20℃ | 24.2℃ |
| ⑤ | 35mL稀盐酸 | 2.5gNaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
请你帮助填写相关内容:
该研究报告的题目可拟为《________》
通过上述实验可得出四条结论:
①NaHCO3的溶解是________ (填“吸热”或“放热”)过程;
②Na2CO3的溶解是________ (填“吸热”或“放热”)过程;
③NaHCO3的饱和溶液和盐酸的反应是________(填“吸热”或“放热”)反应;
④Na2CO3的饱和溶液和盐酸的反应是________(填“吸热”或“放热”)反应.
-
为对比Na2CO3与NaHCO3的性质,实验小组的同学们在甲、乙两支试管中分别加入足量稀盐酸,将两个分别装有Na2CO3或NaHCO3粉末的小气球分别套在两支试管口。将气球内的Na2CO3或NaHCO3倒入试管中(如下图)。
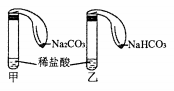
(1)该对比实验要求控制的条件是___________、___________、____________等;
(2)该实验看到的现象是__________________、__________________,乙试管中发生反应的化学方程式是______________________;
(3)泡沫灭火器是利用碳酸盐在酸性条件下反应生成CO2。由上述现象分析,如果选用Na2CO3或NaHCO3中的一种作为泡沫灭火器中的一种反应物,应选_____________,理由是___________________。
-
(1)在试管Ⅰ和Ⅱ中分别加入3mL稀盐酸(均足量),再将装有0.3gNaHCO3和0.3gNa2CO3粉末的小气球分别套在Ⅰ和Ⅱ的管口。各将气球内的NaHCO3、Na2CO3同时倒入试管中,回答:
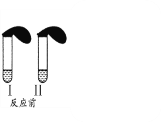
①I试管发生的离子方程式: _______________________;
②两支试管中充分反应后生成的气体总量Ⅰ_____Ⅱ,反应结束时消耗盐酸的物质的量Ⅰ_____Ⅱ(填“>”“=”或“<”)。
(2)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度升高。由此他得出:不管其状态如何,NaHCO3和盐酸反应为吸热反应,而Na2CO3和盐酸反应为放热反应。乙同学认为甲同学的判断太武断,继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| 1 | 50mL水 | 2.5gNaHCO3固体 | 20℃ | 18.5℃ |
| 2 | 50mL水 | 3.2gNa2CO3固体 | 20℃ | 24.3℃ |
| 3 | 35mL稀盐酸 | 含2.5gNaHCO3的饱和溶液15mL | 20℃ | 18.8℃ |
| 4 | 35mL稀盐酸 | 含3.2gNa2CO3饱和溶液15mL | 20℃ | 24.2℃ |
| 5 | 50mL稀盐酸 | 2.5gNaHCO3固体 | 20℃ | T℃ |
| 6 | 50mL稀盐酸 | 3.2gNa2CO3固体 | 20℃ | 25.1℃ |
通过上述实验可得出:
①Na2CO3的饱和溶液和盐酸的反应是___________(吸热或放热)反应;
②NaHCO3的饱和溶液和盐酸的反应是__________(吸热或放热)反应;
③表中⑤号试验混合后温度T℃可能是(填编号)_________________________。
A.18.5℃ B. 24.2℃ C.16.2℃
-
(11分)某化学小组设计实验探究碳酸钠、碳酸氢钠的性质,实验如下:取两支试管分别加入10 mL相同浓度的稀盐酸,将两个各装有0 5 g的Na2CO3和NaHCO3粉末的小气球分别套在两个试管上,将气球内的固体粉末同时倒人试管中,已知盐酸足量,观察实验现象。
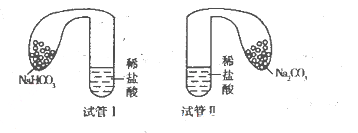
(l)两支试管中均产生气体,其中产生气体较快的为________(填“试管I”或“试管II”),投入________(填化学式)的试管中气球变得比较大。
(2)甲同学触摸上述两试管,发现试管I变冷,试管Ⅱ变热,由此提出不管其状态如何,NaHCO3与HCl反应为吸热反应,Na2CO3与HCl反应为放热反应。
为进一步探究Na2CO3、NaHCO3与盐酸反应的能量变化,乙同学进行下列实验,操作步骤为:①向试剂1中加入试剂2,搅拌、测定温度;②静置、测定温度;③再加入试剂3.搅拌、测定温度、记录。得到以下数据:
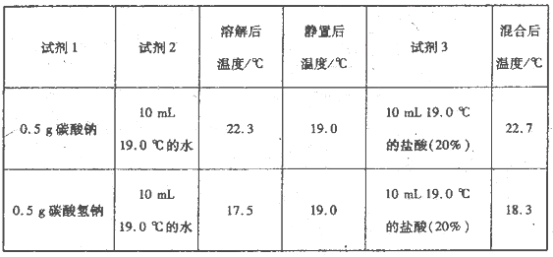
上述实验需要用到的玻璃仪器有________。
乙同学可得出结论:
①NaHCO3的溶解过程________(填“吸热”或“放热”,下同);Na2CO3的溶解过程________。
②CO32-与H+反应为一反应(填“放热”或“吸热”,下同),HCO3-与H+反应为________反应。
(3)比较甲乙同学的实验,你认为 ________(填“甲”或“乙”)的实验方案更合理、更严密。
-
(5分)某同学在试管Ⅰ和试管Ⅱ中分别加入3ml稀盐酸(均足量),再将装有0.3gNaHCO3和0.3gNa2CO3粉末的小气球 分别套在Ⅰ和Ⅱ的管口。将气球内的0.3gNaHCO3和0.3gNa2CO3同时倒入试管中。请回答下列问题:
①试管Ⅰ和试管Ⅱ发生反应的离子方程式分别为________。
②加入固体后,________ 试管(填“Ⅰ”或“Ⅱ”)上的气球膨胀较快。
-
有两试管分别装有Na2CO3和NaHCO3溶液,下列操作或判断正确的是( )
| 方案 | 操 作 | 判 断 |
| A | 分别加入澄清石灰水 | 产生沉淀者为Na2CO3 |
| B | 分别加入等浓度的稀盐酸 | 反应较剧烈者为Na2CO3 |
| C | 分别加入CaCl2溶液 | 产生沉淀者为Na2CO3 |
| D | 逐滴加入等浓度的盐酸 | 立即产生气泡者为Na2CO3 |
A. A B. B C. C D. D
-
有两试管分别装有Na2CO3和NaHCO3溶液,下列操作或判断正确的是( )
| 方案 | 操 作 | 判 断 |
| A | 分别加入澄清石灰水 | 产生沉淀者为Na2CO3 |
| B | 分别加入等浓度的稀盐酸 | 反应较剧烈者为Na2CO3 |
| C | 分别加入CaCl2溶液 | 产生沉淀者为Na2CO3 |
| D | 逐滴加入等浓度的盐酸 | 立即产生气泡者为Na2CO3 |
A. A B. B C. C D. D
-
有两支试管,分别装有Na2CO3和NaHCO3溶液,下列方案中判断正确的是( )
| 方案 | 操作 | 判断 |
| A | 分别滴加澄清石灰水 | 产生沉淀者为Na2CO3 |
| B | 分别加入过量等浓度、等体积的稀盐酸 | 反应较剧烈者为Na2CO3 |
| C | 分别加入CaCl2溶液 | 产生沉淀者为Na2CO3 |
| D | 分别逐滴加入等浓度的盐酸 | 立即产生气泡者为Na2CO3 |
A.A B.B C.C D.D
-
鉴别Na2CO3和NaHCO3两种白色固体,有4位同学为鉴别它们,分别设计了下列四种不同的方法,其中可行的是
A. 分别加入到1 mol·L-1的盐酸溶液中,看有无气泡产生
B. 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无浑浊
C. 分别取样配成溶液,滴加Ca(OH)2溶液,观察有无白色沉淀
D. 分别配成溶液,用洁净铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色






