-
LiCoO2是锂离子电池最早使用的电极材料,利用原钴矿(含Cr2O3、NiS等杂质)制备LiCoO2的工艺流程如下:

资料:i. 在含一定量Cl−的溶液中,钴离子以CoCl42-形式存在:Co2++4Cl− CoCl42−
CoCl42−
ii. CoCl42−溶于有机胺试剂,有机胺不溶于水。
iii. 盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:

(1)步骤ii选用盐酸的浓度应为__________。
a. 4 mol/L b. 6 mol/L c. 10 mol/L
(2)从平衡移动角度解释步骤ⅲ中加入NaCl固体的目的_____________。
(3)步骤iv的操作是_______。
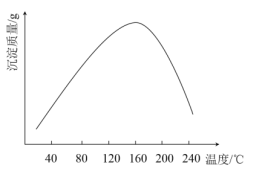
(4)步骤vi用(NH4)2CO3作沉淀剂,在一定条件下得到碱式碳酸钴(Co2(OH)2CO3)。实验测得在一段时间内加入等量(NH4)2CO3所得沉淀质量随反应温度的变化如图所示,分析曲线下降的原因____________。
(5)步骤viii中Co3O4 和Li2CO3 混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是_____________。
(6)锂离子电池的工作原理如图,充、放电过程中,Li+在LiCoO2电极和碳电极之间传递。电池的总反应为:LixC + Li1-xCoO2  C+LiCoO2
C+LiCoO2

①放电时,电池的负极是______。
②充电时,电池的阴极反应式是______。
-
LiCoO2是锂离子电池常用的电极材料。利用原钴矿(含Cr2O3、NiS等杂质)制备LiCoO2的工艺流程如图:

资料:①在含一定量Cl-的溶液中,钻离子以CoCl 形式存在:Co2++4Cl-
形式存在:Co2++4Cl- CoCl
CoCl
②CoCl 溶于有机胺试剂,有机胺不溶于水。
溶于有机胺试剂,有机胺不溶于水。
③盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:

(1)步骤ⅱ选用盐酸的浓度应为___,该过程要注意在通风橱中进行的原因为___(用离子方程式表示)。
a.4mol/L b.6mol/L c.10mol/L
(2)从平街移动角度解释步骤中加入NaCl固体的目的___。
(3)步骤ⅳ的操作是___。
(4)步骤ⅵ用(NH4)2CO3作沉淀剂,在一定条件下得到碱式碳酸钻Co2(OH)2CO3]。已知碱式碳酸钻在339℃以上开始分解,实验测得在一段时间内加入等量(NH4)2CO3所得沉淀质量随反应温度的变化如图所示。分析曲线下降的原因___。

(5)步骤ⅷ中Co3O4和Li2CO3混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是___。
(6)多次实验测定该原钴矿中钴元素的质量分数为1.18%,则原钴矿中Co2O3的质量分数为___%。(假设原钻矿中含钻元素的物质只有Co2O3)。
-
2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。LiCoO2是锂离子电池最早使用的电极材料,利用原钴矿(主要成分为Co2O3)制备LiCoO2的工艺流程如图:
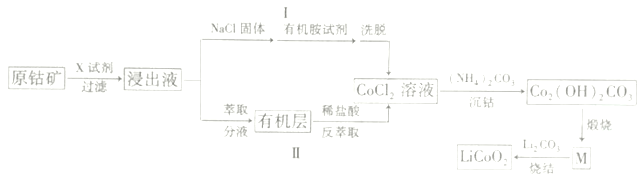
资料:在含一定量Cl-的溶液中,Co2+以CoCl42-形式存在:Co2++4C1- CoCl42-
CoCl42-
(1)若“X试剂”是稀H2SO4和H2O2,则H2O2的作用是___。
(2)若“X试剂”是盐酸,写出离子反应方程式___。
(3)途径I中加入NaCl固体的目的___(用平衡移动原理解释)。
(4)“沉钴”过程中,为了提高Co2(OH)2CO3的产量,温度不宜过高的原因是___。
(5)已知M是钴的某种氧化物,63.6gCo2(OH)2CO3,煅烧成物质M时转移电子0.4mol,则M的化学式为___;写出“烧结”的化学方程式___。
(6)取mg样品溶于稀硫酸,加入过量KI溶液,再用cmol·L-1Na2S2O3标准液滴定(淀粉溶液做指示剂),达到滴定终点时,消耗Na2S2O3溶液VmL,则产品中钻元素的百分含量为___。
(有关反应:LiCoO2+4H+=Li++Co3++2H2O,2Co3++2I-=2Co2++I2,I2+2S2O32-=S4O62-+2I-)
-
2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。利用处理后的废旧锂离子电池材料(主要成分为Co3O4,还含有少量铝箔、LiCoO2等杂质)制备CoO,工艺流程如图:
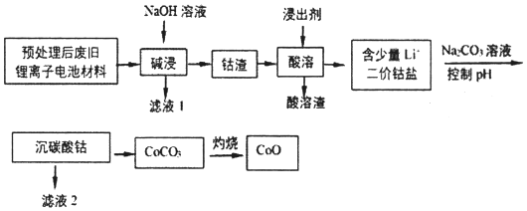
回答下列问题:
(1)Co元素在元素周期表中的位置___。
(2)废旧锂离子电池拆解前进行“放电处理”有利于锂在正极回收的原因是___;提高“碱浸”效率的措施有____(至少写两种)。
(3)不同浸出剂“酸溶”结果如表:
| 出剂 | 浸出液化学成分/(g•L-1) | 钴浸出率/% |
| Co | Al |
| (a)HCl | 80.84 | 5.68 | 98.4 |
| (b)H2SO4 | 65.0 | 6.22 | 72.3 |
| (c)H2SO4+Na2S2O3 | 84.91 | 5.96 | 98.0 |
①浸出剂(a)的钴浸出率最高,而实际工艺中一般不选用浸出剂(a)的原因是____。
②温度越高浸出反应速率越快,所以“酸溶”一般选用较高的温度。据此你选择的浸出剂是___(填序号),理由是___。
③从氧化还原角度分析,还原等物质的量的Co3O4,需要___(填“H2O2”或“Na2S2O3”)物质的量更少。
④综上分析,写出最合适的浸出剂与Co3O4反应的化学方程式____。
(4)已知:Ksp[Co(OH)2]=1.0×10-15,Ksp(Li2CO3)=1.7×10-3,Ksp(CoCO3)=1.5×10-13。若滤液2中Co2+含量为5.9×10-2g•L‑1,计算判断“沉碳酸钴”应调节pH不高于____。
-
钴酸锂(LiCoO2)是锂离子电池的一种重要正极材料。可利用湿法冶金工艺处理精选后的锂离子电池正极材料(LiCoO2、乙炔黑)重新制备高纯度LiCoO2,其流程如下。(已知:LiCoO2难溶于水,Li2CO3微溶于水、难溶于醇,CoCO3难溶于水和醇)

(l) H2O2的作用是____。
(2)“浸取”时若加入盐酸,Cl-被LiCoO2氧化产生Cl2。请写出该反应的离子方程式 ____。
(3)向含Co2+、Li+溶液中加入乙醇的作用 ___,滤渣b的主要成分是____(填化学式)。
(4)在空气中“煅烧”时发生的总化学方程式为 ___。
(5)可用碘量法来测定产品中钴的含量。取mg样品溶于稀硫酸,加入过量KI,以淀粉为指示剂,用c mol/L Na2S2O3标准溶液进行滴定,达到滴定终点时,消耗Na2S2O3标准溶液VmL,则产品中钴的含量为____(以Co2O3计)。有关反应:LiCoO2+4H+=Li++Co3++2H2O,2Co3++2I-=2Co2++I2,I2+2S2O32-= S4O62-+2I-
-
 和
和 都是锂离子电池的电极材料,可利用钛铁矿
都是锂离子电池的电极材料,可利用钛铁矿 主要成分为
主要成分为 ,还含有少量MgO、
,还含有少量MgO、 等杂质
等杂质 来制备,工艺流程如下:
来制备,工艺流程如下:

回答下列问题:
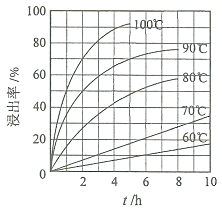
 “酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的浸出率为
“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的浸出率为 时,所采用的实验条件为______。
时,所采用的实验条件为______。
 “酸浸”后,钛主要以
“酸浸”后,钛主要以 形式存在,写出相应反应的离子方程式______。
形式存在,写出相应反应的离子方程式______。
 沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
| 温度 | 30 | 35 | 40 | 45 | 50 |
|  转化率 转化率
| 92 | 95 | 97 | 93 | 88 |
分析 时
时 转化率最高的原因______。
转化率最高的原因______。
 中Ti的化合价为
中Ti的化合价为 ,其中过氧键的数目为______。
,其中过氧键的数目为______。
 若“滤液
若“滤液 ”中
”中 ,加入双氧水和磷酸
,加入双氧水和磷酸 设溶液体积增加1倍
设溶液体积增加1倍 ,使
,使 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中 ,此时是否有
,此时是否有 沉淀生成?______
沉淀生成?______ 列式计算
列式计算 。
。 、
、 的
的 分别为
分别为 、
、
 写出“高温煅烧
写出“高温煅烧 ”中由
”中由 制备
制备 的化学方程式______。
的化学方程式______。
-
新能源汽车的大力推广,带动锂电池材料的发展。我国科学家研发出利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 、
、 、
、 等杂质)制备锂离子电极材料—
等杂质)制备锂离子电极材料— 和
和 的工艺流程如下:
的工艺流程如下:
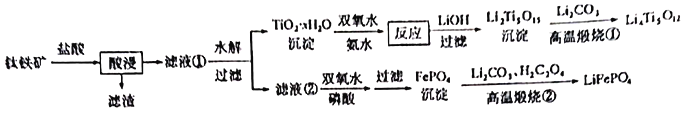
回答下列问题:
(1) 中,Fe元素的化合价为____________。
中,Fe元素的化合价为____________。
(2)“酸浸”后,钛主要以 形式存在,写出
形式存在,写出 水解的的离子方程式_________________。
水解的的离子方程式_________________。
(3) 沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
|  转化率/% 转化率/%
| 92 | 95 | 97 | 93 | 88 |
分析高于40℃时 转化率下降的原因_______________。
转化率下降的原因_______________。
(4) 中Ti的化合价为
中Ti的化合价为 ,其中过氧键的数目为_____________。
,其中过氧键的数目为_____________。
(5)滤液②中加入双氧水和磷酸,反应生成 的离子方程式为____________;若测得Fe3+沉淀完全后,溶液中
的离子方程式为____________;若测得Fe3+沉淀完全后,溶液中 为
为 ,则常温下溶液的pH=______________。(已知
,则常温下溶液的pH=______________。(已知 的
的 )
)
(6)从滤液②中得到 沉淀之后,要对其进行洗涤、干燥,检验沉淀已经洗涤干净的方法_________________________________________。
沉淀之后,要对其进行洗涤、干燥,检验沉淀已经洗涤干净的方法_________________________________________。
-
(14分)Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
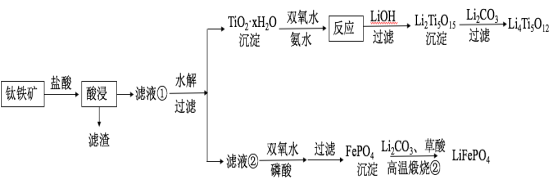
回答下列问题:
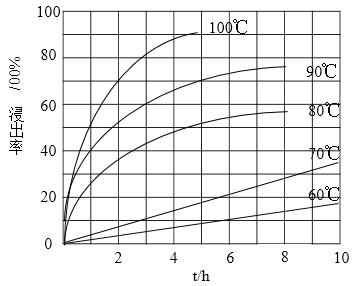
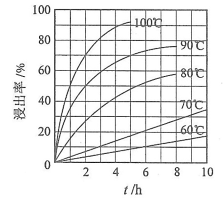
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。
(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
| TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40 ℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式 。
-
[2017新课标Ⅰ]Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
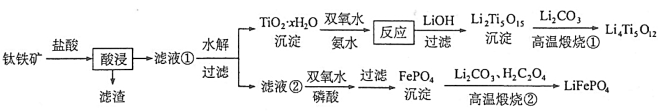
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的浸出率为70%时,所采用的实验条件为___________________。
(2)“酸浸”后,钛主要以 形式存在,写出相应反应的离子方程式__________________。
形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
| TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40 ℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中 ,加入双氧水和磷酸(设溶液体积增加1倍),使
,加入双氧水和磷酸(设溶液体积增加1倍),使 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中 ,此时是否有Mg3(PO4)2沉淀生成? (列式计算)。FePO4、Mg3(PO4)2的Ksp分别为
,此时是否有Mg3(PO4)2沉淀生成? (列式计算)。FePO4、Mg3(PO4)2的Ksp分别为 。
。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式 。
-
Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
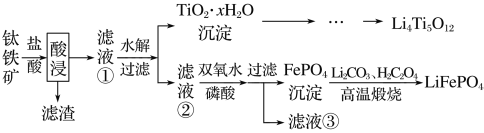
已知:“酸浸”后,钛主要以TiOCl42-形式存在FeTiO3+4H++4Cl-===Fe2++TiOCl42-+2H2O
下列说法不正确的是
A. Li2Ti5O15中Ti的化合价为+4,其中有4个过氧键
B. 滤液②中的阳离子除了Fe2+和H+,还有Mg2+
C. 滤液②中也可以直接加适量的氯水代替双氧水
D. “高温煅烧”过程中,Fe元素被氧化

CoCl42−


C+LiCoO2














