如图表示可逆反应A(g)+3B(g)⇌2C(g) △H<0达平衡后,t1时改变某一反应条件,反应速率随时间变化的情况,根据曲线判断下列说法中正确的是( )
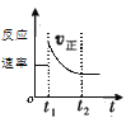
A.t1时降低了温度,平衡向正反应方向移动
B.t1时增大了压强,平衡向正反应方向移动
C.t1时可能使用了催化剂
D.t1时增大了A的浓度,同时减小了C的浓度,平衡向正反应方向移动
高三化学单选题简单题
如图表示可逆反应A(g)+3B(g)⇌2C(g) △H<0达平衡后,t1时改变某一反应条件,反应速率随时间变化的情况,根据曲线判断下列说法中正确的是( )

A.t1时降低了温度,平衡向正反应方向移动
B.t1时增大了压强,平衡向正反应方向移动
C.t1时可能使用了催化剂
D.t1时增大了A的浓度,同时减小了C的浓度,平衡向正反应方向移动
高三化学单选题简单题
如图表示可逆反应A(g)+3B(g)⇌2C(g) △H<0达平衡后,t1时改变某一反应条件,反应速率随时间变化的情况,根据曲线判断下列说法中正确的是( )

A.t1时降低了温度,平衡向正反应方向移动
B.t1时增大了压强,平衡向正反应方向移动
C.t1时可能使用了催化剂
D.t1时增大了A的浓度,同时减小了C的浓度,平衡向正反应方向移动
高三化学单选题简单题查看答案及解析
可逆反应:X+YW+Z,反应速率(V)随时间(t)变化的情况如图所示。
表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
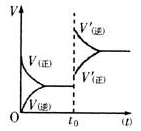
A.时条件改变引起的变化是平衡向正反应方向移动
B.若改变的条件是压强,则W、Z均为气体,X、Y中只有一种为气体
C.若改变的条件是温度,则该反应的正反应是吸热反应
D.若改变的条件是浓度,改变的方法是减小X、Y的浓度
高三化学选择题中等难度题查看答案及解析
下列图示与对应的叙述相符的是
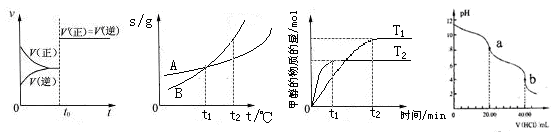 图4 图5 图6 图7
图4 图5 图6 图7
A.图4表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂
B.图5表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
C.图6表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是吸热反应
D.图7是用0.1000mol/L的盐酸滴定20.00mLNa2CO3溶液的曲线,从a→b点反应得离子方程式为:HCO3- + H+ = CO2↑ + H2O
高三化学选择题中等难度题查看答案及解析
11.有可逆反应A(g) + 3B(g) 2C(g);△H<0 。该反应的速率与时间的关系如下图所示:
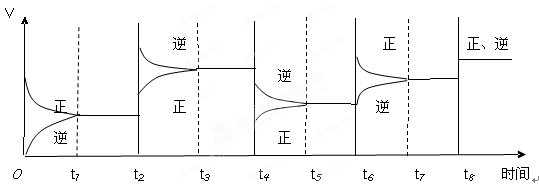
可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,则下列对t2、t4、t6、t8时改变条件的判断正确的是:
A.降低温度、增大压强、减小反应物浓度、使用了催化剂
B.使用了催化剂、增大压强、增大反应物浓度、升高温度
C.增大反应物浓度、使用了催化剂、减小压强、升高温度
D.升高温度、减小压强、增大反应物浓度、使用了催化剂
高三化学选择题中等难度题查看答案及解析
向一容积不变的密闭容器中加入、
和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为
时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知只有
阶段为使用催化剂;图一中
阶段
未画出。

下列说法不正确的是
A.此温度下该反应的化学方程式⇌
B.阶段改变的条件为减小压强
C.B的起始物质的量为1mol
D.在相同条件下,若起始时容器中加入、
和
,要达到
时刻同样的平衡,a、b、c要满足的条件为
和
高三化学单选题中等难度题查看答案及解析
如图是可逆反应A+2B2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
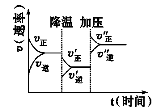
A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应
D.A、B、C、D均为气体
高三化学选择题中等难度题查看答案及解析
如图是可逆反应A+2B2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此推断错误的是
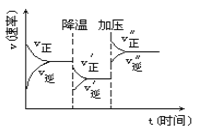
A. 正反应是放热反应
B. A、B一定都是气体
C. D一定不是气体
D. C可能是气体
高三化学单选题困难题查看答案及解析
某温度时,在体积为2L的密闭容器中,气态物质A、B、E、F的物质的量n随时间t的变化情况如图甲所示,在一定条件下反应达到平衡状态,反应进程中正反应速率随时间的变化情况如图乙所示,在、
时刻分别只改变一个条件
温度、压强或某反应物的量
。下列说法错误的是

A.此温度下,该反应的化学方程式为
B.若平衡状态和
对应的温度相同,则
和
对应的平衡常数K一定相同
C.时刻改变的条件是增大压强
D.时刻改变的条件是降低温度
高三化学单选题中等难度题查看答案及解析
向一体积不变的密闭容器中加入2mol A、 C和一定量的B三种气体。在一定条件下发生反应,各物质浓度随时间变化的情况如图甲所示。图乙为
时刻后改变反应条件,该平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.已知
阶段为使用催化剂;图甲中
阶段
未画出。下列说法不正确的是
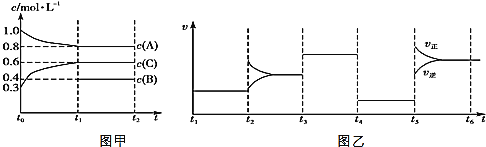
A.该反应为吸热反应
B.B在阶段平衡时转化率为
C.阶段改变的条件为减小压强
D.此温度下该反应的化学平衡常数
高三化学单选题中等难度题查看答案及解析
(14分)向一密闭容器中加入2mol A、0.6molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3-t4阶段为使用催化剂;图一中t0-t1阶段c(B)未画出。

(1)若t1=15min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=________。
(2)t4-t5阶段改变的条件为________,B的起始物质的量为________。
该反应方程式可表示为________
各阶段平衡时对应的平衡常数如下表所示:
| t1—t2 | t2—t3 | t3—t4 | t4—t5 | t5—t6 |
| K1 | K2 | K3 | K4 | K5 |
则K1=________(保留两位小数),K1、K2、K3、K4、K5之间的关系为
K1________ K2________K3________K4________K5________(用“>”、“<”或“=”连接)
(3)在相同条件下,若起始时容器中加入a molA、bmolB和cmolC,要达到t1时刻同样的平衡(各物质的百分含量相同),a、b、c要满足的条件为________。
(含a,b,c的代数式表示)
高三化学填空题困难题查看答案及解析