-
(8分)实验室利用如右图装置进行中和热的测定.请回答下列问题:
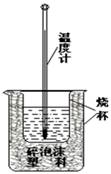
(1)该图中有两处未画出,它们是________、________.
(2)在操作正确的前提下,提高中和热测定准确性的关键是________.
(3)做一次完整的中和热测定实验,温度计需使用_______次.
-
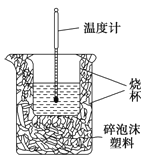
Ⅰ. 实验室利用如右图装置进行中和热的测定。回答下列问题:
(1)该图中有一处未画出,它是_____________(填仪器名称)。
(2)某同学利用50 mL 0.50 mol/L的稀盐酸与50 mL 0.55 mol/L的稀氢氧化钠溶液进行实验,最终测得中和热△H=-55.2kJ/mol。已知标准中和热为△H=-57.3kJ/mol,导致这一偏差的原因最不可能的是________(填字母序号)。
a.实验装置保温、隔热效果差
b.在量取盐酸溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
Ⅱ. 某同学用0.1000mol·L-1的标准NaOH溶液滴定未知浓度的醋酸,其操作为如下几步。请回答:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线下,并记下读数4.60mL
④移取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
(1)以上步骤有一步错误,该错误操作会导致测定结果_______(填“偏大”“偏小”或“不变”)
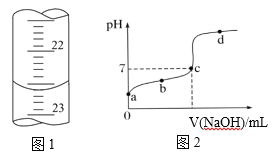
(2)如下图1是某次滴定时滴定管中的终点液面,则该次测得的醋酸物质的量浓度为_____
(3)如下图2所示为滴定图象,a、b、c、d四点中,水的电离程度最大的是 ______点。
-
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如右图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
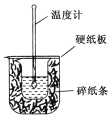
(1)从实验装置上看,图中尚缺少一种玻璃仪器是__________。
(2)大烧杯上如不盖硬纸板,求得的中和热数值__________(填“偏大”、“偏小”或“无影响”)。
(3)实验中改用60mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”).
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会__________(填“偏大”、“偏小”或“无影响”);用50mL 0.50mol/L NaOH溶液进行上述实验,测得的中和热数值会__________。(填“偏大”、“偏小”或“无影响”)
-
(9分)用右图所示装置进行中和热测定实验,请回答下列问题:
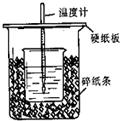
(1)大小烧杯之间填满碎泡沫塑料的作用是________,从实验装置上看,图中缺少的一种玻璃仪器是________。
(2)使用补全仪器后的装置进行实验,取50mL 0.25mol/L H2SO4溶液与50mL0.55 mol/L NaOH溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃。已知中和后生成的溶液的 比热容为4.18J/(g·℃),溶液的密度均为1g/cm3。通过计算可得中和热△H=________,
H2SO4与NaOH反应的热化学方程式为________。
(3)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量________ (填“相等”.“不相等”),所求中和热________ (填“相等”.“不相等”),若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会________ (填“偏大”、“偏小”、“不受影响”)。
-
实验室利用如图装置进行中和热的测定。回答下列问题:
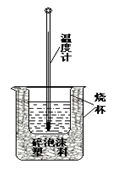
⑴该图中有两处实验用品未画出,它们是 、 ;
⑵在操作正确的前提下提高中和热测定的准确性的关键是: ;
⑶如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热△H”将 (填“偏大”、“偏小”、“不变”)原因是 。
-
实验室利用如图装置进行中和热的测定。回答下列问题:
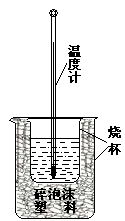
(1)该图中有两处实验用品未画出,它们是 、 ;
(2)在操作正确的前提下提高中和热测定的准确性的关键是: 。
(3)如果用0.5mol•L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将 (填“偏大”、“偏小”、“不变”)原因是 。
-
实验室利用如图装置进行中和热的测定。回答下列问题:
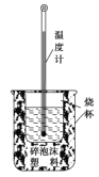
(1)该图中有两处未画出,它们是 ____________、_______________;
(2)在操作正确的前提下提高中和热测定的准确性的关键是____________________;
(3)如果用50 mL0.50 mol/L的盐酸和0.03 mol氢氧化钠固体进行实验,则实验中所测出的“中和热”的热值将____________(填“偏大”、“偏小”或“不变”);
-
已知在稀溶液里,强酸跟强碱发生中和反应生成1 mol液态水时反应热叫做中和热。现利用下图装置进行中和热的测定,请回答下列问题:
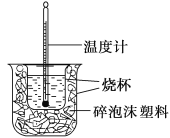
(1)图中未画出的实验器材是________________、________________。
(2)做一次完整的中和热测定实验,温度计需使用________次。
(3)实验时,将0.50 mol·L-1的盐酸加入到0.55mol·L-1的NaOH溶液中,两种溶液的体积均为50 mL,各溶液的密度均为1 g /cm3,生成溶液的比热容c=4.18 J /(g· oC),实验的起始温度为t1 oC,终止温度为t2 oC。测得温度变化数据如下:
| 序号 | 反应物 | 起始温度t1/ oC | 终止温度t2/ oC | 中和热 |
| ① | HCl+NaOH | 14.8 | 18.3 | ΔH1 |
| ② | HCl+NaOH | 15.1 | 19.7 | ΔH1 |
| ③ | HCl+NaOH | 15.2 | 18.5 | ΔH1 |
| ④ | HCl+NH3·H2O | 15.0 | 18.1 | ΔH2 |
①试计算上述两组实验测出的中和热ΔH1=______________。
②某小组同学为探究强酸与弱碱的稀溶液反应时的能量变化,又多做了一组实验④,用0.55mol·L-1的稀氨水代替NaOH溶液,测得温度的变化如表中所列,试计算反应的ΔH2=____________。
③两组实验结果差异的原因是___________________________________________。
④写出HCl+NH3· H2O反应的热化学方程式:_______________________________________。
-
(8分)实验室利用如图装置进行中和热的测定。回答下列问题:
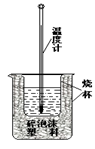
⑴该图中有两处实验用品未画出,它们是________________、____________________;
⑵在操作正确的前提下提高中和热测定的准确性的关键是:____________________________________
⑶如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将________ (填“偏大”、“偏小”、“不变”)原因是______________________________________
-
(8分)实验室利用如图装置进行中和热的测定。回答下列问题:
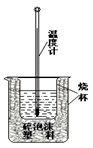
⑴该图中有两处实验用品未画出,它们是________________、____________________;
⑵在操作正确的前提下提高中和热测定的准确性的关键是:_________________________
⑶如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将________ (填“偏大”、“偏小”、“不变”)原因是______________________________________










