-
为保护环境,科学家致力二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质,如将CO2与H2混合,在一定条件下以1:3的比例发生反应,生成某种重要的化工原料和水,该化工原料可能是
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
高三化学单选题简单题查看答案及解析
-
目前,在研究新能源的前沿技术上,科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质.
(1)乙烯的产量是衡量一个国家石油化工发展水平的标志之一,下列石油化工生产能提高乙烯的产量的是:
A.蒸馏、分馏 B.催化裂化 C.催化裂解 D.催化重整
(2)下列说法不正确的是:
A.石油是混合物,分馏后的得到的馏分是纯净物
B.煤隔绝空气加强热可以得到黑褐色油状的煤焦油
C.煤的气化和液化是使煤变成清洁能源的有效途径
D.从绿色化学角度考虑,以植物为主的生物质资源,是未来的理想资源
(3)如果将CO2和H2以1:4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源.请完成以下化学方程式:CO2+4H2→______+2H2O
(4)若将CO2和H2以1:3的比例混合,使之发生反应生成某种重要的化工原料和水,该原料可能是
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
(5)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同: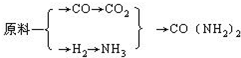
①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料.按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高.据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?______.
(6)请根据以上信息,设计工业合成尿素的条件______.高三化学解答题中等难度题查看答案及解析
-
燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点。下面是目前科学家正致力于研究的三种燃煤烟气脱硫和脱硝的方法。
(1)方法I:用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2 + H2O=(NH4)2SO3 (NH4)2SO4+ SO2 + H2O=2 NH4HSO3
①为了提高燃煤烟气中SO2去除率,可以采取的措施有:使燃煤烟气与氨水充分接触和______。
②燃煤烟气中含有大量的CO2,但在脱硫过程中,不需要先除去燃煤烟气的CO2原因是___________。
(2)方法II:用电化学原理将SO2转化为重要的化工原料H2SO4进行脱硫,装置如图所示。
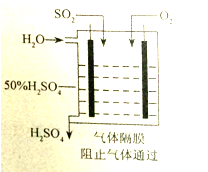
①写出通入SO2的电极的电极反应式:________。
②为使该脱硫过程稳定持续进行,硫酸溶液的浓度应维持不变,则通入的O2和加入的H2O的质量比为_________。
(3)方法Ⅲ:用乙烯作为还取剂将氨的氧化物还原为N2进行脱硝,其机理如图,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图所示。
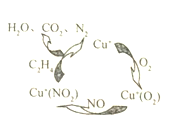

①写出该脱硝过程中乙烯和NO2反应的化学方程式:________________。
②如图,当负载率一定,达到某温度时脱硝率最高,而后却随着温度的升高脱硝率反而降低,其原因是__________;要达到最佳脱硝效果,应采取的条件是_________。
高三化学简答题困难题查看答案及解析
-
“碳捕捉和储存(CCS)”技术是指通过碳捕捉技术,将工业和有关能源产业所产生的二氧化碳分离出来再利用。当前,二氧化碳及其产品的开发、应用是很多科学家致力研究的课题。下列有关说法不正确的是( )
A.人类应将大气中的二氧化碳全部捕捉,以防产生温室效应
B.对捕捉到的二氧化碳进行净化,然后用于制造干冰
C.以捕捉到的二氧化碳为原料,用来制备甲醇等产品
D.用捕捉到的二氧化碳与海藻发生光合作用,可提高海藻产量
高三化学选择题中等难度题查看答案及解析
-
CO2是一种温室气体,对人类的生存环境产生巨大的影响,维持大气中CO2的平衡对生态环境保护有着重要意义。
(1)CO2加氢合成低碳烯烃技术能有效利用CO2,以合成C2H4为例。该转化分为两步进行:
第一步:CO2(g)+H2(g)
CO(g)+H2O(g) ΔH1=+41.3kJ/mol
第二步:2CO(g)+4H2(g)
C2H4(g)+2H2O(g) ΔH2=-210.5kJ/mol
CO2加氢合成乙烯的热化学方程式为__。
(2)利用CO2和H2合成甲醇又是一个有效利用CO2的途径,反应如下:CO2(g)+3H2(g)
CH3OH(g)+H2O(g) ΔH3
①在容积为2L的恒容密闭容器中,通入2molCO2和3molH2发生上述反应,下列说法能够表明该可逆反应达到平衡状态的是__(填字母)
a.消耗1.5molH2时,有0.5molCH3OH生成
b.转移3mol电子时,消耗11.2L(标准状况下)CO2
c.体系中气体的密度不变
d.水蒸气的体积分数保持不变
e.单位时间内生成H2与生成H2O的物质的量之比为3:1
②研究温度对该反应甲醇产率的影响。在210℃~290℃,保持原料气中CO2和H2的投料比不变,按一定流速发生上述反应。得到甲醇平衡产率与温度的关系如图所示,ΔH3__0(填“>”、“=”或“<”)。判断依据是__。
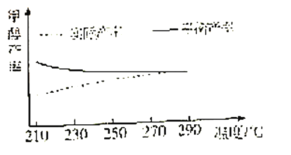
③在一固定容积的密闭容器中发生上述反应。若要提高平衡时CH3OH产率,则可以采取的措施是__(填字母)。
a.升温 b.加入催化剂 c.增加CO2的浓度 d.加入H2加压 e.加入惰性气体 f.分离出甲醇
(3)在一定温度和催化剂作用下,也可将CO2转化为燃料CH4,反应方程式为CO2(g)+4H2(g)
CH4(g)+2H2O(g)。当30℃时,一定量的CO2和H2混合气体在容积为1L的恒容密闭容器中发生上述反应,5min后达到半衡,此时各物质的浓度如下表:
物质
CO2(g)
H2(g)
CH4(g)
H2O(g)
浓度/mol·L-1
0.2
0.8
a
1.6
则a=__,该反应平衡常数K=__。
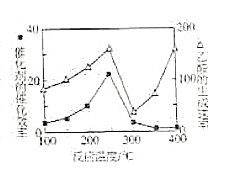
(4)以TiO2/Cu2Al2O4为催化剂,利用CH4可以将CO2直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示,乙酸的生成速率主要取决于温度影响的范围是__。250~300℃时,温度升高而乙酸的生成速率降低的原因是__。
高三化学综合题中等难度题查看答案及解析
-
近年来化学科学家采用“组合转化”技术,将二氧化碳在一定条件下转化为重要的化工原料乙烯:2CO2(g)+6H2(g)
C2H4(g)+4H2O(g);△H=+1411.0 kJ/mol,关于该反应,下列图示与对应的叙述相符的是
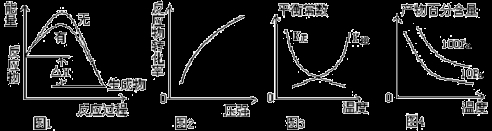
A.图1表示该反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图2表示一定条件下反应达到平衡后改变压强反应物的转化率的变化
C.图3表示一定条件下反应达到平衡后改变温度反应平衡常数的变化
D.图4 表示一定条件下反应达到平衡后改变温度、压强产物百分含量的变化
高三化学选择题中等难度题查看答案及解析
-
研究CO、NOx、SO2等的处理方法对环境保护有重要意义。
(1)科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:
2NO(g)+2CO(g)
2CO2(g)+N2(g) △H=-746.8kJ·mol-1
①为了研究外界条件对该反应的影响,进行下表三组实验,测得不同时刻NO的浓度(c)随时间变化的趋势如图1所示。1、2、3代表的实验编号依次是___________。
(已知在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。)
实验
编号
温度
(℃)
NO初始浓度
(mol·L-1)
CO初始浓度
(mol·L-1)
催化剂比表面积(m2·g—1)
催化剂用量(g)
Ⅰ
280
1.20×10-3
5.80×10-3
82
50
Ⅱ
280
1.20×10-3
5.80×10-3
124
50
Ⅲ
350
1.20×10-3
5.80×10-3
124
50
②图2表示NO的平衡转化率(α)随温度、压强变化的示意图。X表示的是__________,理由是________;Y表示的是________,且Y1________Y2(填“>”或“<”)。

(2)一定温度下,将NO2与SO2以体积比1:2置于密闭容器中发生反应NO2(g)+SO2(g)
SO3(g)+NO(g),达到平衡时SO3的体积分数为25%。该反应的平衡常数K=___________。
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3
7N2+12H2O,电解质溶液为碱性。工作一段时间后,该电池负极区附近溶液pH________(填“变大”、“变小”或“不变”),正极电极反应式为____________。
高三化学填空题中等难度题查看答案及解析
-
硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是( )
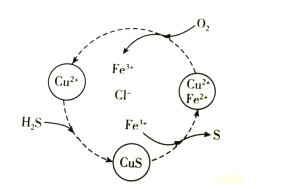
A.在图示的转化中,Fe3+和CuS是中间产物
B.在图示的转化中,化合价不变的元素只有铜
C.图示转化的总反应是2H2S+O2
2S+2H2O
D.当有1molH2S转化为硫单质时,需要消耗O2的物质的量为0.5mol
高三化学单选题中等难度题查看答案及解析
-
硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是( )
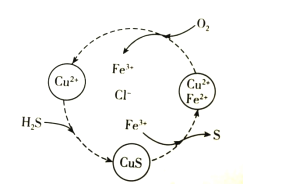
A.在图示的转化中,Fe3+和CuS是中间产物
B.在图示的转化中,化合价不变的元素只有铜
C.图示转化的总反应是2H2S+O2
2S+2H2O
D.当有1molH2S转化为硫单质时,需要消耗O2的物质的量为0.5mol
高三化学单选题中等难度题查看答案及解析
-
硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列叙述正确的是
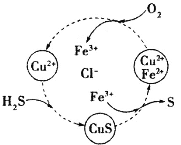
A.在转化过程中化合价不变的元素只有Cu和Cl
B.由图示的转化可得出氧化性的强弱顺序:O2>Cu2+>S
C.在转化过程中能循环利用的物质只有FeCl2
D.反应中当有34gH2S转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O2的质量为16g
高三化学单选题中等难度题查看答案及解析