-
Ⅰ.如图是旺旺同学设计的一个简易的原电池装置,请回答下列问题。
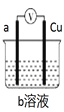
(1)若 a电极材料为碳、b溶液为 FeCl3溶液,则正极的电极反应式为____,当有1.6g负极材料溶解时,转移的电子为____mol;
(2)若 a 电极材料为铁、b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为______→ __________(填电极材料,下同),溶液中的NO3-向________极移动;
(3)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为:2H2+O2=2H2O,则正极的电极方程式为________________。
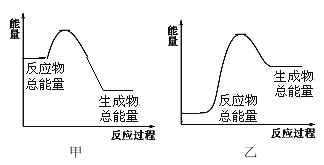
Ⅱ.已知H-H 键、N-H 键、N≡N 键的键能分别为 436kJ/mol、391kJ/mol、946 kJ/mol,关于工业合成氨的反应,请根据键能的数据判断下列问题:
(4)若有 1 mol NH3生成 ,可________(填“吸收”或“放出”)热量________kJ;该反应的能量变化可用图__________表示。(填“甲“或“乙”)
-
(12分)如图是某同学设计的一个简易的原电池装置,回答下列问题。

(1)若a为镁、b为CuCl2,则正极材料为_____,负极上的电极反应式为_________。
(2)若a为镁、b为NaOH,则Mg极上发生________反应(填“氧化”或“还原”),负极上的电极反应式为_______________。
(3)若a为铜、b为浓硝酸,则电流的方向为____→___(填电极材料),正极上的电极反应式为______。
(4)上述事实表明,确定原电池中电极的正负时,不仅要考虑电极材料本身的性质,还要考虑________。
-
根据氧化还原反应Fe + 2FeCl3 = 3FeCl2设计一个原电池装置。
(1)电解质溶液为________
(2)负极材料________,电极反应式________
(3)正极材料________,电极反应式________
-
某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
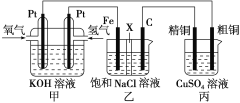
根据要求回答相关问题:
(1)通入氢气的电极为____(填“正极”或“负极”),负极的电极反应式为____________________________。
(2)石墨电极为____(填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,____(填“铁极”或“石墨极”)区的溶液先变红。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将____(填“增大”“减小”或“不变”)。精铜电极上的电极反应式为______________________________________。
(4)写出上述例题中乙池电解的总反应方程式:_________________________。
(5)若上述例题甲池中消耗标准状况下的氢气11.2 L,则丙池中理论上应析出铜的质量为____。
-
如下图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
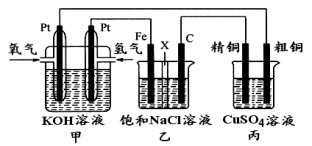
根据要求回答相关问题:
(1)通入氧气的电极为________(填“正极”或“负极”),负极的电极反应式为 。
(2)铁电极为________(填“阳极”或“阴极”),石墨电极(C)的电极反应式为 。
(3)反应一段时间后,乙装置中生成氢氧化钠主要在________区。(填“铁极”或“石墨极”)
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为 ;丙装置中阴极析出铜的质量为 。
-
(1)写出一个能证明还原性Fe比Cu强的离子方程式:______;
(2)根据上述反应设计一个原电池,画出简易装置图(标出电极名称、电极材料、电解质溶液 )______;
(3)若该电池中两电极的总质量为60g,工作一段时间后,取出两电极洗净干燥后称量,总质量为62g,则反应过程中转移电子的数目为______.
-
(1)写出一个能证明还原性Fe比Cu强的离子方程式:______;
(2)根据上述反应设计一个原电池,画出简易装置图(标出电极名称、电极材料、电解质溶液 )______;
(3)若该电池中两电极的总质量为60g,工作一段时间后,取出两电极洗净干燥后称量,总质量为62g,则反应过程中转移电子的数目为______.
-
选择适宜的材料和试剂设计一个原电池,完成下列反应:
Zn+CuSO4=ZnSO4+Cu
(1)画出装置图,并标明各部分材料名称。
(2)负极材料 ,正极材料 ,电解质溶液是 。
(3)写出电极反应式:
负极: _______________________
正极: _______________________
-
(1)选择适宜的材料和试剂设计一个原电池,完成下列反应:Zn+CuSO4=ZnSO4+Cu。
①画出装置图:___。
②电极材料和电解质溶液各是什么___。?
③写出电极反应式:负极:___;正极:___。
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25克,铜表面析出了氢气___L(标准状况下)。导线中通过___mol电子。
-
选择适宜的材料和试剂设计一个原电池,完成下列反应:Zn+CuSO4=ZnSO4+Cu
(1)画出装置图(要求在图上标出电极材料和电解质溶液)
(2)写出电极反应式:正极:________;负极:________.
(3)描述电极上的实验现象:正极:________;负极________.




