-
利用ClCH2CH2PO(OH)2(乙烯利 及Br2/CCl4(CCl4的沸点为76.8℃)等为原料制备1,2-二溴乙烷
及Br2/CCl4(CCl4的沸点为76.8℃)等为原料制备1,2-二溴乙烷 沸点为131,4℃)的装置如图所示。已知a中发生的反应为ClCH2CH2PO(OH)2+4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O。下列说法错误的是( )
沸点为131,4℃)的装置如图所示。已知a中发生的反应为ClCH2CH2PO(OH)2+4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O。下列说法错误的是( )
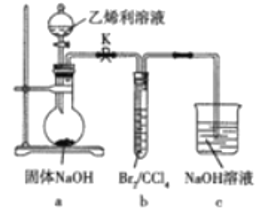
A.向圆底烧瓶中滴加乙烯利溶液前需先打开K
B.实验过程中装置b中的液体逐渐变为无色
C.装置c中的NaOH溶液的作用是吸收挥发出的Br2和乙烯
D.装置b中反应后的混合液经Na2SO3溶液洗涤、水洗、干燥、蒸馏得1,2-二溴乙烷
-
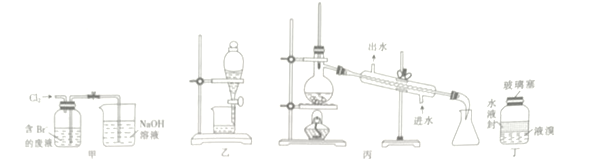
欲从含Br-的废液中提取溴单质,需经过一系列操作,实验装置及物质的性质如下:
| Br2 | CCl4 | 正十二烷 |
| 密度/g·cm-3 | 3. 12 | 1.59 | 0.753 |
| 沸点/℃ | 58.76 | 76.8 | 215~217 |
下列说法中正确的是
A. 可用装置甲氧化废液中的Br-
B. 装置乙中选用正十二烷而不用CCl4,是因为正十二烷的密度更小
C. 用装置丙进行蒸馏,先收集正十二烷再收集Br2
D. 用装置丁长期贮存液溴
-
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:制备溴乙烷的的一种方法是乙醇与氢溴酸反应,该反应的化学方程式为:CH3CH2OH+HBr CH3CH2Br+H2O。
CH3CH2Br+H2O。
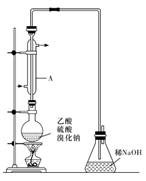
I.实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应时若温度过高,则有SO2生成,同时观察到还有一种红棕色气体产生,该气体的分子式是 。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 (填写正确选项的字母)。
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
II.溴乙烷的性质实验
(4)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是 。通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液
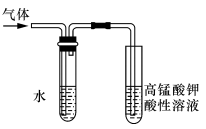
(5)溴乙烷与NaOH乙醇溶液共热可产生乙烯气体。在进行该实验时,把生成的气体通过右图所示的装置。用该装置进行实验的目的是检验乙烯的生成,该图中右侧试管中的现象是______________;左侧试管中水的作用是___________________。
-
下列说法中错误的是( )
A.无论是乙烯与Br2的加成反应,还是乙烯使酸性KMnO4溶液褪色,都与乙烯分子内含有碳碳双键有关
B.用溴的CCl4溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷
-
下列过程中发生取代反应的是
A.乙烯通往Br2的CCl4溶液中生成1,2 ---二溴乙烷
B.乙醇在空气中燃烧生成CO2和H2O
C.用氯乙烯制聚氯乙烯
D.甲烷与氯气混合后光照生成一氯甲烷
-
下列实验,所选装置不合理的是
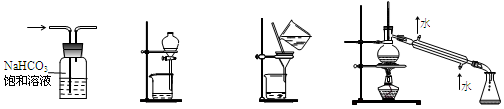
① ② ③ ④
A.除去CO2中的HCl,选①
B.分离碘的CCl4溶液和水,选②
C.除去乙醇中的苯酚,选③
D.分离CCl4(沸点76.8℃)和正丁醇(沸点117.2℃),选④
-
1,2-二溴乙烷(沸点为131℃),可溶于CCl4,某同学在实验室将乙烯通入溴的四氯化碳溶液中,在生成和纯化1,2-二溴乙烷的实验过程中,下列操作未涉及的是
A. 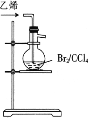 B.
B. 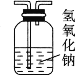 C.
C. 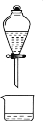 D.
D. 
-
1,2-二溴乙烷(沸点为131℃),可溶于CCl4,某同学在实验室将乙烯通入溴的四氯化碳溶液中,在生成和纯化1,2-二溴乙烷的实验过程中,下列操作未涉及的是
A. 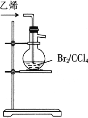 B.
B. 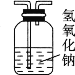 C.
C. 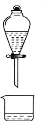 D.
D. 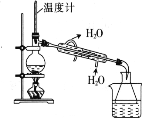
-
1,2-二溴乙烷(沸点为131℃),可溶于CCl4,某同学在实验室将乙烯通入溴的四氯化碳溶液中,在生成和纯化1,2-二溴乙烷的实验过程中,下列操作未涉及的是
A.  B.
B.  C.
C. 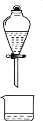 D.
D. 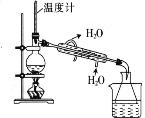
-
溴乙烷是一种重要的液体化工原料,沸点38.4℃,难溶于水且非电解质,可与碱溶液反应。实验室中可利用如下原理制取少量溴乙烷:
NaBr+H2SO4(浓)+ C2H5OH→NaHSO4+C2H5Br
某研究性学习小组的同学设计了如图所示的装置(支持及加热仪器已省略)来制备溴乙烷,并验证有副产物SO2、CO2生成(SO2沸点为-10℃)
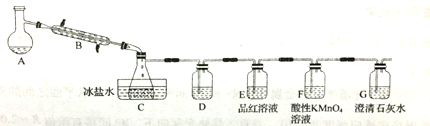
(1)仪器B的名称是_____,装置D用来检验并除去乙烯,则D中的化学方程式为:__________。F的作用是__________。证明一定有CO2生成的现象是_________。
(2)C中所得到的溴乙烷中含有少量的乙醇、Br2、HBr。为得到纯净的溴乙烷,该同学取出C中的液体依次用水洗 _________洗
_________洗 水洗,再用无水CaCl2干燥,最后进行蒸馏。洗涤实验中,所用的玻璃仪器除烧杯外还一定需要的仪器名称是_____________。
水洗,再用无水CaCl2干燥,最后进行蒸馏。洗涤实验中,所用的玻璃仪器除烧杯外还一定需要的仪器名称是_____________。
(3)假设上述实验都得到了预期的实验现象,写出乙醇与浓硫酸反应生成上述无机气体时的化学方程式:______________。
(4)设计一种实验方案,利用化学方法证明C中的液体中含有单质溴:____________。
及Br2/CCl4(CCl4的沸点为76.8℃)等为原料制备1,2-二溴乙烷
沸点为131,4℃)的装置如图所示。已知a中发生的反应为ClCH2CH2PO(OH)2+4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O。下列说法错误的是( )





 B.
B.  C.
C.  D.
D. 
 B.
B.  C.
C.  D.
D. 
 B.
B.  C.
C.  D.
D. 
