-
一氧化二氮(Nitrous oxide),无色有甜味气体,又称笑气,“笑气”的名称是由于吸入它会感到欣快,并能致人发笑。1799年,英国化学家汉弗莱·戴维发现了该气体。一氧化二氮早期被用于牙科手术的麻醉,现用在外科手术和牙科起麻醉和镇痛作用。
(1)N2O在金粉表面发生热分解反应:2N2O(g)=2N2(g)+O2(g) △H。
已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(1) △H1
4NH3(g)+3O2(g)=2N2(g)+6H2O(1) △H2
△H=________(用含△H1、△H2的代数式表示)。
(2)N2O和CO是环境污染性气体,这两种气体会发生反应:N2O(g)+CO(g)  CO2(g)+N2(g),“Fe+”常用作该反应的催化剂。其总反应分两步进行:第一步为Fe++N2O
CO2(g)+N2(g),“Fe+”常用作该反应的催化剂。其总反应分两步进行:第一步为Fe++N2O FeO++N2;第二步为____________________(写化学方程式)。第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第二步反应活化能_____(填“大于”“小于”或“等于”)第一步反应活化能。
FeO++N2;第二步为____________________(写化学方程式)。第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第二步反应活化能_____(填“大于”“小于”或“等于”)第一步反应活化能。
(3)在四个恒容密闭容器中充入相应量的气体(图甲),发生反应:2N2O(g)  2N2(g)+O2(g)△H,容器I、II、III中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g)△H,容器I、II、III中N2O的平衡转化率如图乙所示:
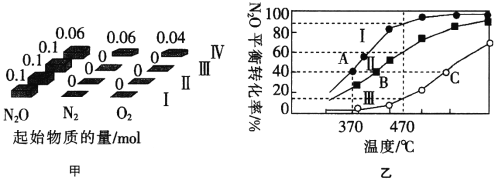
①该反应的△H______(填“>”或“<”)0。
②容器II的体积为0.5L,在470℃下进行反应,30s后达到平衡,0~30s内容器II中O2的反应速率为_______mol·L-1·s-1。
③已知容器I的体积为1L,370℃时,该反应的平衡常数k=________(保留两位有效数字)。
④图中A、B、C三点处容器内密度最大的点是________(填“A”“B”或“C”)。
-
 ,俗称笑气,是一种无色有甜味气体,在室温下稳定,有轻微麻醉作用,并能致人发笑。下列叙述中正确的是( )
,俗称笑气,是一种无色有甜味气体,在室温下稳定,有轻微麻醉作用,并能致人发笑。下列叙述中正确的是( )
A.笑气的摩尔质量为44 g
B. 个笑气分子的质量为44 g
个笑气分子的质量为44 g
C.1 mol笑气的质量为44 
D. g笑气含有
g笑气含有 个
个 分子
分子
-
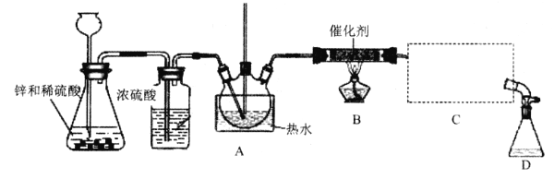
三氯甲烷又称氯仿,是一种无色透明液体,易挥发,有香气,略有甜味,不易燃烧,但在常温下与空气直接接触,易被氧化,并生成剧毒物光气,常用作有机溶剂和麻醉剂,结构简式为CHCl3。实验室中可用热还原CCl4法制备氯仿,装置示意图及有关数据如下:
| 物质 | 相对分子质量 | 密度/(g/Ml) | 沸点/℃ | 水中溶解性 |
| CHCl3 | 119.5 | 1.50 | 61.3 | 难溶 |
| CCl4 | 154 | 159 | 76.7 | 难溶 |
实验步骤:
① ;
② 向三颈瓶中滴入20mL CCl4;
③ 开始通入H2;
④ 向A处水槽中加入热水,并接通C处冷凝装置的冷水;
⑤ 点燃B处酒精灯;
⑥ 反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量NaHCO3溶液和水洗涤,分出的产物加人少量无水CaCl2固体,静置后过滤;
⑦ 对滤液进行蒸馏纯化,得到氯仿15g。请回答:
(1) A中长直玻璃管的作用为_____;①处的操作为_______。
(2) B处中发生主要反应的化学方程式为___________。
(3) C处中应选用的冷凝管为____(填选项字母);冷水应从该冷凝管的____(填“a”或 “b”)口接入。

(4)该实验中,氯仿的产率为_______。
(5)氯仿在空气中能被氧气氧化生成HCl和光气(COCl2),该反应的化学方程式为_____.
-
SO2气体为无色气体,有强烈刺激性气味,是大气主要污染物之一,某学习小组为了探究二氧化硫的某些性质,进行了如下实验。
Ⅰ.如图所示,使用试剂和装置探究二氧化硫的还原性:
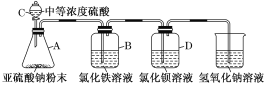
(1)装置C的名称为________。
(2)装置B中溶液的现象为_______。
(3)学生甲预测装置D中没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。学生乙经过查阅资料发现少量白色沉淀可能是硫酸钡,因为装置或溶液中少量的氧气参与了氧化反应,请写出装置D中反应的化学方程式:______________。
Ⅱ.经过思考,设计了如下装置,且所配制的溶液均使用无氧蒸馏水,检验SO2 在无氧干扰时,是否与氯化钡反应生成沉淀。
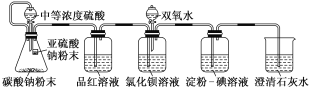
(4)加入碳酸钠粉末的目的是________。
(5)当_____时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
(6)裝置中选用澄清石灰水而不用氢氧化钠溶液的目的是____。
-
SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,某学习小组为了探究二氧化硫的某些性质,进行了如下实验。
I.如下图所示,使用药品和装置一探究二氧化硫的还原性:
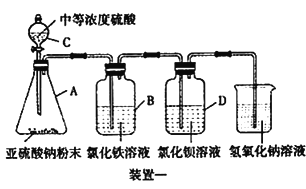
(1)装置C的名称为________。
(2)B中溶液的现象为________。
(3)学生甲预测装置D 中没有白色沉淀产生,但随着反应的进行,发现D 中产生了少量白色沉淀。学生乙经过查阅资料发现少量白色沉淀可能是硫酸钡,因为装置或溶液中少量的氧气参与了氧化反应,请写出装置D 中的反应方程式________。
II.经过思考,设计了如下装置二,且所配制的溶液均使用无氧蒸馏水,检验SO2 在无氧干扰时,是否与氯化钡反应生成沉淀。
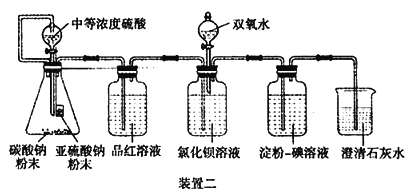
(4)碳酸钠粉末的目的是________。
(5)当______时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
(6)裝置二选用澄清石灰水而不用氢氧化钠溶液的目的是________。
-
对于某些离子的检验及结论一定正确的是( )
A. 加入稀盐酸产生无色无味并能使澄清石灰水变浑浊的气体,一定有 CO32﹣
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有 SO42﹣
C. 加入硝酸无明显现象,再滴几滴硝酸银溶液有白色沉淀,一定有 Cl﹣
D. 加入新制氯水后,再滴几滴 KSCN 溶液,变红,一定有 Fe2+
-
(11分)某些化学反应可表示为:A+B=C+D十H2O(未配平,条件略)。请回答:
(1)若A为主族元素,A与B的浓溶液在常温时发生钝化,但A与B的稀溶液反应产生无色气体并能迅速转化为红棕色。请写出A与B的稀溶液反应的化学方程________。
(2)若A、D均可用于消毒,,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式________。
(3)若A为黑色固体,C是黄绿色的单质气体。当产生标准状况下33.6LC气体时,参加反应的A的质量为________。
(4)已知炭和浓硫酸在加热时也符合上述反应式,某同学设计如下实验证明其产物。则:

若证明有水生成,需要在.A、B之间加装盛有________的干燥管。若证明生成CO2,需要C试管盛放________(填化学式)溶液。装置B可以探究SO2与品红作用的可逆性,请写出实验操作及现象________;该实验的尾气可采用NaOH溶液吸收,有关反应离子方程式为________。
-
膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。它的分子构型是三角锥形。以下关于PH3的叙述正确的是
A.PH3分子中有未成键的孤对电子 B.PH3是非极性分子
C.PH3是一种强氧化剂 D.PH3分子的P-H键是非极性键
-
某黄金冶炼公司在处理尾矿废液过程中,发生有毒HCN外溢事故,造成人员中毒。已知HCN是一种无色剧毒气体,遇皮肤或通过呼吸道吸入均会造成严重的中毒或死亡,HCN遇明火或强灯光均会易燃或易爆。它的水溶液是一种极弱的易挥发酸,结合以上信息,下列说法你认为错误的是( )
A.为了防止冶金络合剂氰化钠产生HCN,废液排放前应加入足量石灰和漂白粉
B.检查HCN外溢时,必须穿特制防护服,并用特制的手电筒
C.河水有自净能力,冶金废水可直接排放到河流中进行稀释、降解
D.实验室配制氰化钠溶液时,最好在通风橱中进行
-
无色透明的锆石(主要成分为ZrSiO4)酷似钻石,是很好的钻石代用品。锆石又称锆英石,常含有铁、铝、铜的氧化物杂质。工业上一种以锆英石为原料制备ZrO2的工艺流程如图所示:
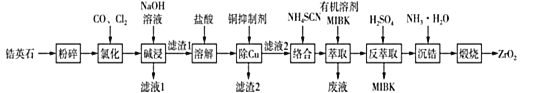
己知:i.Zr在化合物中通常显+4价,“氯化”过程中除C、O元素外,其他元素均转化为高价氯化物;
ii.SiC14极易水解生成硅酸;ZrC14易溶于水,390℃升华;
iii.Fe(SCN)3难溶于有机溶剂MIBK,Zr(SCN)4在水中的溶解度小于在有机溶剂MIBK中的溶解度。
请回答下列问题:
(1)“粉碎”锆英石的目的为 ___。
(2)①“氯化”过程中,锆英石发生的主要反应的化学方程式为 ___。
②“氯化”过程中ZrC14的产率与温度、压强的关系如图所示:
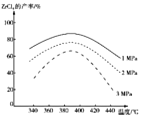
由图可知,“氯化”过程选择的最佳条件为____,“氯化”温度超过390℃时,ZrC14产率降低的原因为 ___。
(3)“滤液1”中含有的阴离子除OH-、Cl-外,还有 _______。
(4)①常用的铜抑制剂有NaCN(氰化钠),NaCN可与铜离子反应生成Cu(CN)2{Ksp[Cu(CN)2]=4×10-10}沉淀。己知盐酸溶解后的溶液中Cu2+的浓度为1 mol∙L-1,当溶液中Cu2+浓度不大于1×10-6 mol∙L-1时即达到后续生产的要求,则欲处理1L该溶液至少需要2mol∙L-1的NaCN溶液的体积为____L(溶液混合时的体积变化忽略不计,计算结果保留两位小数)。
②由于氰化钠有剧毒,所以需要对“废液”中的氰化钠进行处理,通常选用漂白粉或漂白液在碱性条件下将氰化钠氧化,其中一种产物为空气的主要成分。请写出在碱性条件下漂白液与氰化钠反应的离子方程式____。
(5)通过“萃取”“反萃取”可以分离铁,富集锆,原理为____。
CO2(g)+N2(g),“Fe+”常用作该反应的催化剂。其总反应分两步进行:第一步为Fe++N2O
FeO++N2;第二步为____________________(写化学方程式)。第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第二步反应活化能_____(填“大于”“小于”或“等于”)第一步反应活化能。
2N2(g)+O2(g)△H,容器I、II、III中N2O的平衡转化率如图乙所示:









