-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
| | | |
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42−,含有Cu+、Cu2+和SO32−。
已知:Cu+ Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu2+和SO32−。
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu+和SO32−的理由是_______________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42−,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和____________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i. Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
将对比实验方案补充完整。
步骤一:
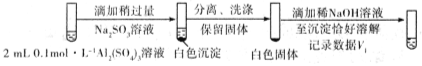
步骤二:

则V1___________V2(填>,<或=)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
| | | |
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42−,含有Cu+、Cu2+和SO32−。
已知:Cu+  Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+  CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu2+和SO32−。
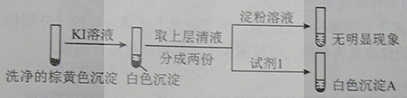
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu+和SO32−的理由是___________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42−,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.呗Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
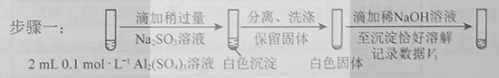
步骤二:_____________(按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4溶液 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
| | | |
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42−,含有Cu+、Cu2+和SO32−。
已知:Cu+ Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
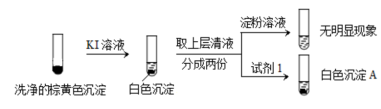
②通过下列实验证实,沉淀中含有Cu2+和SO32−。
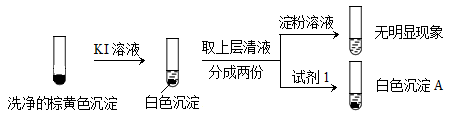
KI溶液 洗净的棕黄色沉淀 取上层清液 分成两份 淀粉溶液 试剂1 无明显现象
白色沉淀A
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu2+和SO32−的理由是___________。
(3)已知:Al2(SO4)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42−,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.被Al(OH)3所吸附;
ii.存在于铝的碱式盐中。
对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
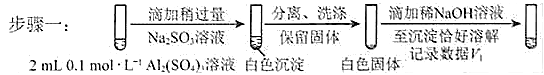
步骤二:_____________(按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
| 0.2mol·L-1Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2mol·L-1CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1mol·L-1Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
(1)经验检,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:__________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含 ,含有Cu+、Cu2+和
,含有Cu+、Cu2+和 。
。
已知:Cu+ Cu+Cu2+,Cu2+
Cu+Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是__________。
②通过下列实验证实,沉淀中含有Cu2+和 。
。

a.白色沉淀A是BaSO4,试剂1是__________。
b.证实沉淀中含有Cu2+和 的理由是__________。
的理由是__________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无 ,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和__________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.Al(OH)3所吸附;
ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
步骤一:

步骤二:__________(按上图形式呈现)。
b.假设ii成立的实验证据是__________。
(4)根据实验,亚硫酸盐的性质有__________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 滴管 | 试管 |
| 
| 0.2mol·L-1Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2mol·L-1CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 |
| 0.1mol·L-1Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 |
(1)经验检,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:__________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含 ,含有Cu+、Cu2+和
,含有Cu+、Cu2+和 。
。
已知:Cu+ Cu+Cu2+,Cu2+
Cu+Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是__________。
②通过下列实验证实,沉淀中含有Cu2+和 。
。

a.白色沉淀A是BaSO4,试剂1是__________。
b.证实沉淀中含有Cu2+和 的理由是__________。
的理由是__________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无 ,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和__________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.Al(OH)3所吸附;
ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
步骤一:

步骤二:__________(按上图形式呈现)。
b.假设ii成立的实验证据是__________。
(4)根据实验,亚硫酸盐的性质有__________。盐溶液间反应的多样性与__________有关。
-
以Na2SO3溶液和不同金属的硫酸盐溶液为实验对象,可探究盐的性质和盐溶液间反应的多样性
| 实验 | 试剂 | 现象 | 检验 结果 |
| 滴管 | 试管 |
| 
2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 | 产物为Ag2SO3 |
| 0.2 mol·L−1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | 产物含Cu+、Cu2+和SO32− |
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | 产物为 Al(OH)SO3 |
下列说法不正确的是
A. 现象Ⅰ对应的离子方程式:Ag2SO4(s) + SO32−(aq) === Ag2SO3(s) + SO42−(aq)
B. 用稀硫酸证实Ⅱ沉淀中含有Cu+的实验现象是析出红色固体
C. 现象Ⅲ中白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色
D. 上述实验现象涉及了亚硫酸盐的溶解性、氧化还原性及其水溶液的酸碱性
-
以CuSO4溶液和不同酸根离子形成的钠盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
| 实验 | 试剂 | 现象 |
| 
| 滴管 | 试管 |
| 0.2mol•L-1 CuSO4溶液 | 0.2mol•L-1NaI溶液 | Ⅰ.产生白色沉淀和黄色溶液 |
| 0.2mol•L-1Na2CO3溶液 | Ⅱ.产生绿色沉淀和无色无味气体 |
| 0.2mol•L-1Na2SO3溶液 | Ⅲ.产生棕黄色沉淀 |
(1)经检验,现象Ⅰ的白色沉淀为CuI,则反应的离子方程式为___,氧化产物与还原产物的物质的量之比为___。
(2)经检验,现象Ⅱ中产生的气体是二氧化碳,绿色沉淀是碱式碳酸铜[xCuCO3•yCu(OH)2•zH2O]。现采用氢气还原法测定碱式碳酸铜组成,请回答如下问题:
①写出xCuCO3•yCu(OH)2•zH2O与氢气反应的化学方程式___;
②实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填仪器接口字母编号):a→___→gf→___→___→___→l
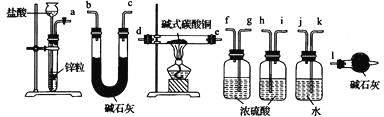
(3)经检验,现象Ⅲ的棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。已知:Cu+ Cu+Cu2+
Cu+Cu2+
①用稀硫酸证实沉淀中含有Cu+的实验现象是___。
②通过下列实验证实,沉淀中含有Cu2+和SO32-。
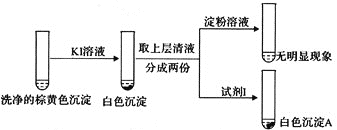
a.白色沉淀A是BaSO4,试剂Ⅰ是___。
b.证实沉淀中含有Cu2+和SO32-的理由是___。
-
为探究Na2SO3溶液的性质,某学习小组设计了一系列实验,并记录实验现象。具达如下表所示。
| 实验装置 | 实验序号 | 滴管试剂 | 试管试剂 | 实验现象 |
| 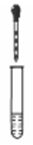
| ① | 0.2mol/LNa2SO3溶液 | 品红溶液 | 红色消失 |
| ② | 饱和Ag2SO4举泫 | 产生白色沉淀 |
| ③ | 0.2mol/L CuSO4溶液 | 溶液先变绿,继续滴加产生砖红色沉淀 |
| ④ | 0.lmol/L Al2(SO4)溶液 | 开始无明显现象,继续滴加产生白色沉淀,并有刺激性气味的气体生成 |
则以下说法不正确的是( )
A. Na2SO3溶液具有漂白性
B. Ksp(Ag2SO4)<Ksp(Ag2SO3)
C. 实验③,SO32-与Cu2+发生了氧化还原反应
D. 实验④发生反应的离子方程式为:3SO32-+2Al3++3H2O=2Al(OH)3↓+3SO2↑
-
某小组以亚硝酸钠(NaNO2)溶液为研究对象,探究NO2-的性质。
| 实验 | 试剂 | 编号及现象 |
| 滴管 | 试管 |
| 
2mL | 1%酚酞溶液 | 1 mol·L-1 NaNO2溶液 | 实验I:溶液变为浅红色,微热后红色加深 |
| 1 mol·L-1 NaNO2溶液 | 0.1 mol·L-1 KMnO4 溶液 | 实验II:开始无明显变化,向溶液中滴加稀硫酸后紫色褪去 |
| KSCN溶液 | 1 mol·L-1 FeSO4 溶液(pH=3) | 实验III:无明显变化 |
| 1 mol·L-1 NaNO2溶液 | 1 mol·L-1 FeSO4 溶液(pH=3) | 实验IV:溶液先变黄,后迅速变为棕色,滴加KSCN溶液变红 |
资料:[Fe(NO)]2+在溶液中呈棕色。
(1)结合化学用语解释实验I“微热后红色加深”的原因 ______
(2)实验II证明NO2-具有_____性, 从原子结构角度分析原因_________
(3)探究实验IV中的棕色溶液
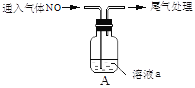
①为确定棕色物质是NO与Fe2+,而非Fe3+发生络合反应的产物,设计如下实验,请补齐实验方案。
| 实验 | 溶液a | 编号及现象 |
| 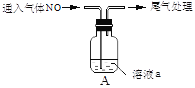
| 1 mol·L-1FeSO4溶液(pH=3) | i.溶液由___色迅速变为___色 |
| ____________________ | ii.无明显变化 |
②加热实验IV中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释上述现象产生的原因_________。
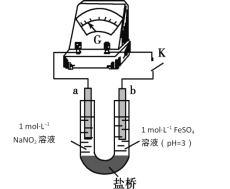
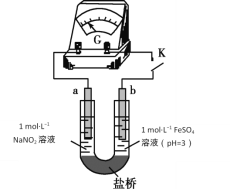
(4)络合反应导致反应物浓度下降,干扰实验IV中氧化还原反应发生及产物检验。小组同学设计实验V:将K闭合后电流表指针发生偏转,向左侧滴加醋酸后偏转幅度增大。
①盐桥的作用是____________________________
②电池总反应式为______________________
实验结论:NO2-在一定条件下体现氧化性或还原性,氧还性强弱与溶液酸碱性等因素有关。
-
某小组以亚硝酸钠(NaNO2)溶液为研究对象,探究NO2-的性质。
| 实验 | 试剂 | 编号及现象 |
| 滴管 | 试管 |
| 
2mL | 1%酚酞溶液 | 1 mol·L-1 NaNO2溶液 | 实验I:溶液变为浅红色,微热后红色加深 |
| 1 mol·L-1 NaNO2溶液 | 0.1 mol·L-1 KMnO4 溶液 | 实验II:开始无明显变化,向溶液中滴加稀硫酸后紫色褪去 |
| KSCN溶液 | 1 mol·L-1 FeSO4 溶液(pH=3) | 实验III:无明显变化 |
| 1 mol·L-1 NaNO2溶液 | 1 mol·L-1 FeSO4 溶液(pH=3) | 实验IV:溶液先变黄,后迅速变为棕色,滴加KSCN溶液变红 |
资料:[Fe(NO)]2+在溶液中呈棕色。
(1)结合化学用语解释实验I“微热后红色加深”的原因 ______
(2)实验II证明NO2-具有_____性, 从原子结构角度分析原因_________
(3)探究实验IV中的棕色溶液
①为确定棕色物质是NO与Fe2+,而非Fe3+发生络合反应的产物,设计如下实验,请补齐实验方案。
| 实验 | 溶液a | 编号及现象 |
| 
| 1 mol·L-1FeSO4溶液(pH=3) | i.溶液由___色迅速变为___色 |
| ____________________ | ii.无明显变化 |
②加热实验IV中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释上述现象产生的原因_________。
(4)络合反应导致反应物浓度下降,干扰实验IV中氧化还原反应发生及产物检验。小组同学设计实验V:将K闭合后电流表指针发生偏转,向左侧滴加醋酸后偏转幅度增大。
①盐桥的作用是____________________________
②电池总反应式为______________________
实验结论:NO2-在一定条件下体现氧化性或还原性,氧还性强弱与溶液酸碱性等因素有关。
,含有Cu+、Cu2+和
。
Cu+Cu2+,Cu2+
CuI↓(白色)+I2。
。

的理由是__________。
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。







 Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+