-
国际气候变化经济学报告中显示,大气中CO2浓度每增加一倍,可使地表平均温度上升5∼6℃。为减少温室效应的加剧,需将工业生产中产生的CO2分离出来加以利用。回答下列问题:
(1)在500℃时,Li4SiO4与低浓度的CO2反应生成两种锂盐,待该反应达到化学反应的限度后,升温至700℃,两种锂盐反应放出高浓度的CO2,而Li4SiO4可循环利用。写出700℃时两种锂盐反应的化学方程式___。
(2)CO2与NH3反应可合成化肥。
①已知:2NH3(g)+CO2(g)=NH2COONH4(s) △H=-159.5kJ•mol-1
NH2COONH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5kJ•mol-1
H2O(l)=H2O(g) △H=+44.0kJ•mo1-1
则CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的△H=___kJ•mol-1
②将足量CO2通入饱和氨水中可制得碳铵(NH4HCO3)。已知室温下Kb(NH3•H2O)=1.8×10-5,Ka1(H2CO3)=4.3×10-7,则0.0.1mol•L-1NH4HCO3溶液室温下呈___ (填“酸性”、“中性”或“碱性”)。
(3)在一定条件下,CO2与H2可用于合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比[ ]达平衡时CO2的转化率[α(CO2)]如图1所示。
]达平衡时CO2的转化率[α(CO2)]如图1所示。
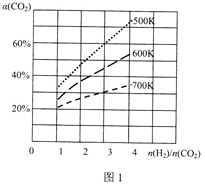
该反应的△H___0(填“>”、“=”或“<”)。
②500K、投料比[ ]=3时,H2的平衡转化率为___;设总压强为P0,则化学平衡常数Kp=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
]=3时,H2的平衡转化率为___;设总压强为P0,则化学平衡常数Kp=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③直接甲醇燃料电池(DMFC)具备低温快速启动、燃料洁净环保以及电池结构简单等特性。该电池使用合适的合金为电极,以氢氧化钠溶液、甲醇、空气为原料。写出其负极电极反应式___。
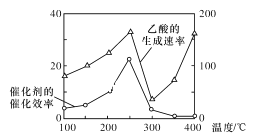
(4)在TiO2/Cu2Al2O4为催化剂时,CO2和CH4可反应生成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图2所示。300℃∼400℃时,影响乙酸生成速率的主要因素是___(填“温度”或“催化剂”)。
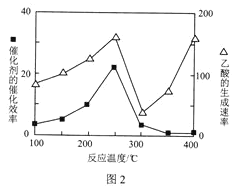
-
大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
(1)CO2溶于水生成碳酸,碳酸和亚硝酸(HNO2)的电离常数如下表所示,下列事实中,能说明亚硝酸酸性比碳酸强的是(填字母代号)____________。
| 弱酸 | HNO2 | H2CO3 |
| 电离常数 | Ka=5.1×10-4 | Ka1=4.6×10-7 |
| Ka2=5.6×10-11 |
A 常温下,亚硝酸电离常数比碳酸一级电离常数大
B 亚硝酸的氧化性比碳酸的氧化性强
C 亚硝酸与碳酸钠反应生成CO2
D 相同浓度的碳酸钠溶液的pH比亚硝酸钠的大
(2).CO2与NH3反应可合成尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g)在合成塔中进行,图中Ⅰ,Ⅱ,Ⅲ三条曲线分别表示温度为T℃时,按不同氨碳比 和水碳比
和水碳比 投料时,二氧化碳平衡转化率的情况。
投料时,二氧化碳平衡转化率的情况。
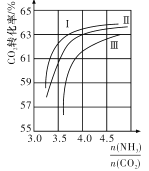
①曲线Ⅰ,Ⅱ,Ⅲ中水碳比的数值分别为0.6~0.7,1~1.1,1.5~1.6,则生产中应选用的水碳比数值范围是____________。
②推测生产中氨碳比应控制在____________(选填“4.0”或“4.5”)左右比较适宜。
③若曲线Ⅱ中水碳比为1,初始时CO2的浓度为1mol/L,则T℃时该反应的平衡常数K=____________(保留有数数字至小数点后两位)。
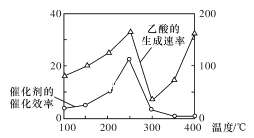
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化为乙酸,请写出该反应的化学方程式:____________。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。在温度为____________时,催化剂的活性最好,效率最高。请解释图中250~400℃时乙酸生成速率变化的原因:250~300℃时____________;300~400℃时____________。
-
大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
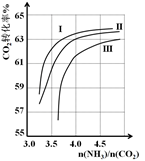
(1)CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) 在合成塔中进行。下如图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
CO(NH2)2(l)+H2O(g) 在合成塔中进行。下如图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值范围分别为0.6~0.7、1~1.1和1.5~1.61,则生产中应选用水碳比的数值范围为_______________。
②请推测生产中氨碳比控制在4.0左右还是控制在4.5左右比较适宜,并简述你的理由_______________。
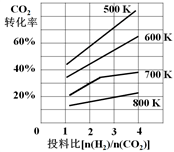
(2)CO2与H2也可用于合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
①该反应的化学平衡常数的表达式为_____________。
②该反应的∆S__________0,∆H_________0(填“>”或“<”)。
③700K投料比[n(H2)/n(CO2)] = 2时,H2的平衡转化率为___________________。
(3)固体氧化物电解池(SOEC)用于高温电解CO2/H2O,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如下如图。
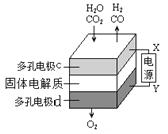
①在c极上反应分两步进行:首先水电解产生氢气,然后氢气与CO2反应产生CO。写出电极c上发生的电极反应式:___________________。
②若电解得到的1:1的合成气(CO+H2),则通入的CO2和H2O物质的量比值为__________。
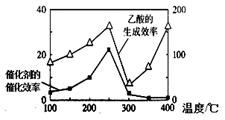
(4)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见如图。如何解释如图中250-400℃时温度升高与乙酸的生成速率变化的关系?______________________。
-
大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化为乙酸,请写出该反应的化学方程式:____。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。在温度为____时,催化剂的活性最好,效率最高。请解释图中250~400℃时乙酸生成速率变化的原因:250~300℃时___;300~400℃时___。
-
“温室效应”是哥本哈根气候变化大会研究的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有 (填字母)。
a.采用节能技术,减少化石燃料的用量 b.鼓励乘坐公交车出行,倡导低碳生活
c.利用太阳能、风能等新型能源替代化石燃料
(2)一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) △Hl=+1411.0 kJ/mol
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) △H2=+1366.8 kJ/mol
则由乙烯水化制乙醇的热化学方程式是 。
(3)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。
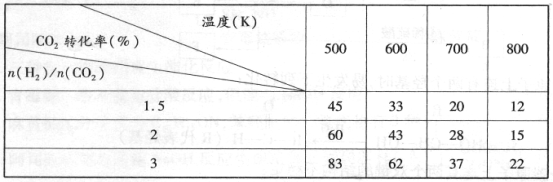
根据上表中数据分析:
①温度一定时,提高氢碳比[n(H2)/n(CO2)],CO2的转化率 (填“增大”“减小”或“不变”)。
②该反应的正反应为 (填“吸”或“放”)热反应。
-
“温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决“温室效应”的有效途径.
(1)下列措施中,有利于降低大气中CO2浓度的有 (填字母).
A.采用节能技术,减少化石燃料的用量
B.鼓励乘坐公交车出行,倡导低碳生活
C.利用太阳能、风能等新型能源替代化石燃料
(2)一种途径是将CO2转化成有机物实现碳循环.如:
2CO2(g)+2H2O(l)═C2H4(g)+3O2(g)△Hl=+1411.0kJ/mol
2CO2(g)+3H2O(l)═C2H5OH(l)+3O2(g)△H2=+1366.8kJ/mol
则由乙烯水化制乙醇的热化学方程式是 .
(3)在一定条件下,6H2(g)+2CO2(g)⇌CH3CH2OH(g)+3H2O(g).
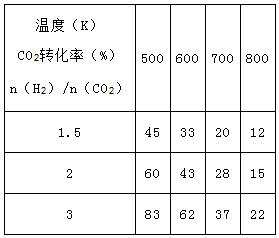
根据上表中数据分析:
①温度一定时,提高氢碳比[ ],CO2的转化率 (填“增大”“减小”或“不变”).
],CO2的转化率 (填“增大”“减小”或“不变”).
②该反应的正反应为 (填“吸”或“放”)热反应.
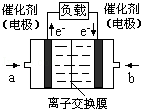
(4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则b处通入的是 (填“乙醇”或“氧气”),a处发生的电极反应是 .
-
“温室效应”是哥本哈根气候变化大会研究的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有 (填字母)。
a.采用节能技术,减少化石燃料的用量 b.鼓励乘坐公交车出行,倡导低碳生活
c.利用太阳能、风能等新型能源替代化石燃料
(2)一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) △Hl=+1411.0 kJ/mol
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) △H2=+1366.8 kJ/mol
则由乙烯水化制乙醇的热化学方程式是 。
(3)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。
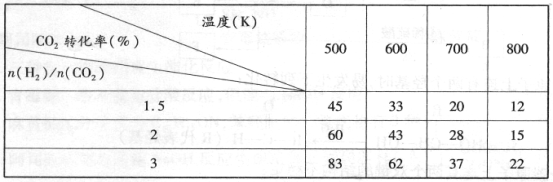
根据上表中数据分析:
①温度一定时,提高氢碳比[n(H2)/n(CO2)],CO2的转化率 (填“增大”“减小”或“不变”)。
②该反应的正反应为 (填“吸”或“放”)热反应。
-
“温室效应”是哥本哈根气候变化大会研究的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有________ (填字母)。
A.采用节能技术,减少化石燃料的用量
B.鼓励乘坐公交车出行,倡导低碳生活
C.利用太阳能、风能等新型能源替代化石燃料
(2)一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) △Hl=+1411.0 kJ/mol
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) △H2=+1366.8 kJ/mol
则由乙烯水化制乙醇的热化学方程式是________。
(3)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。
| 温度(K) CO2转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
根据上表中数据分析:
①温度一定时,提高氢碳比[ ],CO2的转化率________(填“增大”“减小”或“不变”)。
],CO2的转化率________(填“增大”“减小”或“不变”)。
②该反应的正反应为________ (填“吸”或“放”)热反应。
(4)下图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则b处通入的是________(填“乙醇”或“氧气”),a处发生的电极反应是。

-
“温室效应”是哥奉哈根世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
(1)下列措施中,有利于降低大气中CO2浓度的是________(填字母编号)。
a.采用节能技术,减少化石燃料的用量
b.鼓励乘坐公交车出行,倡导“低碳”生活
c.利崩太阳能、风能等新型能源替代化石燃料 ·
(2)CH4是另一种主要的温室气体,l克甲烷完全燃烧生成液态水和二氧化碳,放出55.64 kJ的热量,甲烷的燃烧热是________。
(3)酸阿的形成主要是由废气中的SOx和NOx造成的。通过SO2和Br2、H2O的定量反应在电解池中产生的电流变化,可以准确测定空气中SO2的含量。该反应的化学方程式为________,反应中氧化产物和还原产物的物质的量之比为________。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。
第一阶段燃烧黄铁矿的化学方程式为________;
第二阶段的反应原理是2SO2(g)+O2(g) 2SO3(g),其生产设备的名称为________;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2SO3(g),其生产设备的名称为________;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是________(填字母编号)
a. SO2为5mol·L-1,O2为3.5mol·L-1
b. SO2为3mol·L-1
c.SO2、SO3均为2.5mol·L-1
d.SO3为5mol·L-1
-
“温室效应”是哥奉哈根世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
(1)下列措施中,有利于降低大气中CO2浓度的是________(填字母编号)。
a.采用节能技术,减少化石燃料的用量
b.鼓励乘坐公交车出行,倡导“低碳”生活
c.利崩太阳能、风能等新型能源替代化石燃料 ·
(2)CH4是另一种主要的温室气体,l克甲烷完全燃烧生成液态水和二氧化碳,放出55.64 kJ的热量,甲烷的燃烧热是________。
(3)酸阿的形成主要是由废气中的SOx和NOx造成的。通过SO2和Br2、H2O的定量反应在电解池中产生的电流变化,可以准确测定空气中SO2的含量。该反应的化学方程式为________,反应中氧化产物和还原产物的物质的量之比为________。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。
第一阶段燃烧黄铁矿的化学方程式为________;
第二阶段的反应原理是2SO2(g)+O2(g) 2SO3(g),其生产设备的名称为________;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2SO3(g),其生产设备的名称为________;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是________(填字母编号)
a. SO2为5mol·L-1,O2为3.5mol·L-1
b. SO2为3mol·L-1
c.SO2、SO3均为2.5mol·L-1
d.SO3为5mol·L-1
]达平衡时CO2的转化率[α(CO2)]如图1所示。

]=3时,H2的平衡转化率为___;设总压强为P0,则化学平衡常数Kp=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。











