-
已知:废液中含+6 价铬的化合物毒性较大污染性强,常用 NaHSO3 将废液中的Cr2O72-还原成 Cr3+。请配平该反应的离子方程式:_____ Cr2O72-+_____HSO3-+____H+ = ____Cr3++_____SO42-+_____H2O
并用双线桥标出电子转移的方向和数目____________________。
高一化学填空题中等难度题查看答案及解析
-
工业废水中常含有一定量的Cr2O72﹣和CrO42﹣,它们会对人类及生态系统产生很大的伤害,必须进行处理,常用的处理方法为还原沉淀法.
该法的工艺流程为CrO42-
Cr2O72-
Cr3+
Cr(OH)3↓
①第①步的反应是否为氧化还原反应 (填“是”或“否”)
②第②步中,还原1molCr2O72﹣离子,需要 mol的FeSO4•7H2O.
③写出第③步反应的离子方程式 .
高一化学填空题中等难度题查看答案及解析
-
化学工业中会产生大带含铬废水,需进行无害化处理检测达标后才能排放。
(1)工业常用NaHSO3还原法处理,方法如下:向酸性废水中加入NaHSO3使Cr2O72- 还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
① 写出NaHSO3与Cr2O72-反应的离子方程式:__________________________________。
②已知25℃时Ksp[Cr(OH)3]=6.4×10-31。若除去废水中Cr3+,使其浓度小于1×10-5 mol•L-1,此时溶液中的c(H+)<_________mol•L-1
(2)废水中铬元素总浓度的测定方法如下:向一定量含Cr2O72-和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O72-与I-完全反应后生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:Cr3+
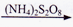 Cr2O72-
Cr2O72- I2
S4O62-
① 上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会________(选填“偏大”、“偏小”或“不变”)。
②准确移取含Cr2O72-和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000 mol•L-1的Na2S2O3标准溶液13.50 mL。计算该废水中铬元素总浓度(以mg·L-1表示),写出计算过程。_____________________________________________________
高一化学简答题困难题查看答案及解析
-
已知在酸性条件下,下列物质氧化KI时,自身发生如下变化:Cl2→2Cl﹣ ; MnO4﹣→Mn2+ ; Cr2O72﹣→Cr3+ ; HNO3→NO ;如果分别用等物质的量的这些物质氧化足量的KI,得到I2的物质的量最多的是
A.Cl2 B.MnO4﹣ C.Cr2O72﹣ D.HNO3
高一化学选择题困难题查看答案及解析
-
已知下列离子在酸性条件下都能氧化KI,它们自身发生如下变化:①Cr2O72﹣→Cr3+,②IO3﹣→I2,③MnO4﹣→Mn2+。如果分别用等物质的量的这些离子氧化足量的KI,得到I2的物质的量由多到少的顺序正确的是
A.②=③>① B.①>②=③ C.①=②>③ D.②>③>①
高一化学选择题困难题查看答案及解析
-
在一定条件下,PbO2与Cr3+反应,产物是Cr2O72−和Pb2+,则与1mol Cr3+反应所需PbO2的物质的量为( )
A.3.0mol B.1.5mol C.1.0mol D.0.75mol
高一化学单选题中等难度题查看答案及解析
-
在一定条件下,PbO2与Cr3+反应,产物是Cr2O72−和Pb2+,则与1mol Cr3+反应所需PbO2的物质的量为( )
A.3.0mol B.1.5mol C.1.0mol D.0.75mol
高一化学单选题中等难度题查看答案及解析
-
在一定条件下,PbO2与Cr3+反应,产物是Cr2O72﹣和Pb2+,则与1mol PbO2反应所需Cr3+的物质的量为
A.0.75 mol B.1.5 mol C.1.0 mol D.0.67 mol
高一化学选择题困难题查看答案及解析
-
重铬酸钾(K2Cr2O7)溶液是实验和科研中一种常用氧化剂。酸性条件下,Cr2O72-通常被还原为Cr3+。
(1)某同学欲用K2Cr2O7固体配制500 mL 0.04000 mol·L-1的K2Cr2O7溶液。
①需用的玻璃仪器有烧杯、玻璃棒、量筒、________。
②应该称取K2Cr2O7固体的质量为_________。
(2)交警常用装有重铬酸钾酒精测试仪检测司机是否酒后驾车,其化学反应原理如下:2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O。每有1 mol C2H5OH发生反应,转移电子的物质的量是________。
高一化学填空题简单题查看答案及解析
-
铁氧体(Fe3O4)法是处理含铬废水的常用方法.其原理是:用FeSO4把废水中Cr2O72-还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物
 。 处理含1 mol Cr2O72-废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
。 处理含1 mol Cr2O72-废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是A.x=1,a=5 B.x=0.5,a=8
C.x=2,a=10 D.x=0.5,a=10
高一化学选择题中等难度题查看答案及解析