-
某废水中含有的NH4+在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H =-273kL/mol
②NO2-(aq)+l/2O2(g)=NO3-(aq) △H =-73kL/mol
下列叙述不正确的是
A. lmol的NH3和1mol的NH4+都有10×6.02×1023个电子
B. 室温下,0.1mol/LHNO2(aq) pH>l,则NaNO2溶液显碱性
C. NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) △H =-346kL/mol
D. 在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
某废水中含有的NH4+在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H=-273kJ·mol-1
②NO2-(aq)+1/2O2(g)=NO3-(aq) △H=-73kJ·mol-1
下列说法正确的是( )
A.1mol的NH3和1mol的NH4+都有10×6.02 ×1023个质子
B.室温下,NH4NO2溶液呈酸性,则说明Ka(HNO2)< Kb(NH3·H2O)
C.NH4+(aq)+2O2(g) NO3—(aq)+2H+(aq)+H2O(l);△H= - 346kJ/mol
D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
某废水中含有的NH 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述不正确的是
A.1mol的NH3和1mol 的NH4+都有10×6.02×1023个电子
B.室温下,0.1 mol/L HNO2溶液pH>1,则NaNO2溶液显碱性
C.NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH= -346kJ/mol
D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
某废水中含有的NH 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述不正确的是
A. 1mol的NH3和1mol 的NH4+都有10×6.02×1023个电子
B. 室温下,0.1 mol/L HNO2溶液pH>1,则NaNO2溶液显碱性
C. NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH= -346kJ/mol
D. 在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
含氮废水中的NH4+在一定条件下可与O2发生以下反应:
① NH4+(aq) + 3/2O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ΔH = -273kL/mol
② NO2-(aq) + 1/2O2(g) = NO3-(aq) ΔH = -73kL/mol
下列叙述不正确的是
A.升高温度,可使①②反应速率均加快
B.室温下时0.1 mol/L HNO2(aq) pH>1,则NaNO2溶液显碱性
C.NH4+(aq) + 2O2(g) = NO3 -(aq) + 2H+(aq) + H2O(l) ΔH = -346kJ/mol
D.1 mol NH4+在①反应中与1 mol NO2-在②反应中失电子数之比为1:3
-
含氮废水中的NH4+在一定条件下可与O2发生以下反应:
① NH4+(aq) + O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ΔH = -273kL/mol
O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ΔH = -273kL/mol
② NO2-(aq) + O2(g) = NO3-(aq) ΔH = -73kL/mol
O2(g) = NO3-(aq) ΔH = -73kL/mol
下列叙述不正确的是
A、升高温度,可使①②反应速率均加快
B、室温下时0.1 mol/L HNO2(aq) pH>1,则NaNO2溶液显碱性
C、NH4+(aq) + 2O2(g) = NO3-(aq) + 2H+(aq) + H2O(l) ΔH = -346kJ/mol
D、1 mol NH4+在①反应中与1 mol NO2-在②反应中失电子数之比为1:3
-
氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3¯,两步反应的能量变化示意图如下:
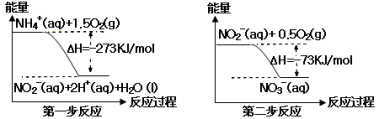
下列说法合理的是:
A.该反应的催化剂是NO2¯
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3¯
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1:3
-
氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3¯,两步反应的能量变化示意图如下:

下列说法合理的是
A.该反应的催化剂是NO2¯
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3¯
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1: 3
-
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下: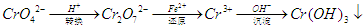 ,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
A.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g
B.溶液颜色保持不变,说明上述可逆反应达到达平衡状态
C.常温下转换反应的平衡常数K=1×1014,则转化后所得溶液的pH=6
D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5
-
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:

己知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)  Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
A.溶液颜色保持不变,说明上述可逆反应达到达平衡状态
B.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g
C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6
D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5
在一定条件下可被O2氧化,反应过程如下:


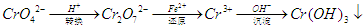 ,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是