-
硫代硫酸钠(Na2S2O3)可用作分析试剂及鞣革还原剂。它受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得。实验室模拟该工业过程的装置如图所示。

回答下列问题:
(1)a中试剂为__________,b中试剂为__________,c中试剂为____________________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是______________。
(3)d中的试剂为__________________。
(4)实验中要控制SO2生成速率,可以采取的措施有________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是__________________。
-
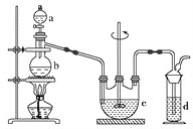
硫代硫酸钠(Na2S2O3)可用作分析试剂及鞣革还原剂。它受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得。实验室模拟该工业过程的装置如图所示。
回答下列问题:
(1)a中试剂为__________,b中试剂为__________,c中试剂为____________________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是______________。
(3)d中的试剂为__________________。
(4)实验中要控制SO2生成速率,可以采取的措施有________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是__________________。
-
硫代硫酸钠(Na2S2O3)可用作分析试剂、鞣革还原剂、脱氯剂等。它受热、遇酸易分解。它有多种制备方法,其中硫化碱法为:向热的硫化钠和亚硫酸钠混合液中通入二氧化硫,经吸硫、蒸发、结晶,制得硫代硫酸钠晶体。制备过程中发生的主要反应如下:
Na2S + H2O + SO2 —→ Na2SO3 + H2S ………… (i)
2H2S + SO2 —→ 3S + 2H2O …………………… (ii)
S + Na2SO3 —△→ Na2S2O3 …………………………(iii)
(1)已知Na2S2O3分解反应是吸热反应,由此可得出:该分解反应中,反应物断裂化学键所吸收的总能量_________(填“大于”、“小于”或“等于”)生成物形成化学键所放出的总能量。
(2)Na2S2O3具有还原性,判断依据是_________、_________(至少写出两条)。
(3)上述反应i ~ iii总反应的化学方程式为_________。制备过程中,即使将反应物的用量按化学方程式的计量数进行配比,反应后各反应物仍有剩余,这说明该过程中存在_________。
(4)为了保证硫代硫酸钠的产量,生产中通入的SO2不能过量,原因是________。
-
工业上将Na2CO3和Na2S配成溶液,再通入SO2可制取Na2S2O3,同时放出CO2。下列说法不正确的是( )
A. 上述反应中氧化剂和还原剂的物质的量比是2:l
B. 上述反应中的Na2CO3和Na2S的物质的量比最佳是1:2
C. 每生成lmol Na2S2O3转移4mol电子
D. Na2S2O3既是氧化产物,又是还原产物
-
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。在该反应中( )
A. 硫元素被氧化,碳元素被还原
B. 氧化剂与还原剂的物质的量之比为1:2
C. 每生成1molNa2S2O3,转移4mol电子
D. 相同条件下,每吸收10m3SO2就会放出2.5m3CO2
-
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。在该反应中
A. 硫元素既被氧化又被还原
B. 氧化剂与还原剂的物质的量之比为1:2
C. 每生成1molNa2S2O3,转移4mol电子
D. 相同条件下,每吸收10m3SO2就会放2.5m3CO2
-
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。在该反应中
A. 硫元素既被氧化又被还原
B. 氧化剂与还原剂的物质的量之比为1:2
C. 每生成1molNa2S2O3,转移4mol电子
D. 相同条件下,每吸收10m3SO2就会放2.5m3CO2
-
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。在该反应中
A. 硫元素被氧化
B. 氧化剂与还原剂的物质的量之比为1:2
C. 每生成1molNa2S2O3,转移4mol电子
D. 相同条件下,每吸收10m3SO2就会放出2.5m3CO2
-
Na2S2O3可用作纺织工业氯气漂白布匹后的“脱氯剂”,4Cl2+Na2S2O3+5H2O =2NaCl+2H2SO4 +  ,有关该反应的叙述不正确的是
,有关该反应的叙述不正确的是
A.Na2S2O3是还原剂
B.根据该反应可判断氧化性:Cl2>SO42-、
C. 的物质是HCl
的物质是HCl
D.上述反应中,每生成1mol SO42-,转移2mole-
-
硫代硫酸钠(Na2S2O3)具有较强的还原性,还能与中强酸反应,在精细化工领域应用广泛。将SO2通入按一定比例配制成的Na2S和Na2CO3的混合溶液中,可制得Na2S2O3·5H2O(大苏打)。
已知:Na2S、Na2CO3、Na2SO3、NaHCO3溶液呈碱性;NaHSO3溶液呈酸性。
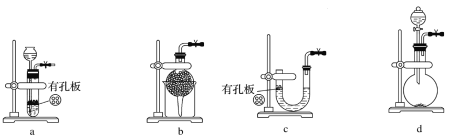
(1)实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是________(填字母代号)。
(2)向Na2S和Na2CO3的混合溶液中不断通入SO2气体的过程中,发现:
①浅黄色沉淀先逐渐增多,反应的化学方程式为_____________________________________;
②当浅黄色沉淀不再增多时,反应体系中有无色无味的气体产生,反应的化学方程式为________________________________;
③浅黄色沉淀逐渐减少(这时有Na2S2O3生成);
④继续通入过量的SO2,浅黄色沉淀又会逐渐增多,反应的化学方程式为________________________。
(3)制备Na2S2O3时,为了使反应物利用率最大化,Na2S和Na2CO3的物质的量之比应为____________;通过反应顺序,可比较出:温度相同时,同物质的量浓度的Na2S溶液和Na2CO3溶液pH更大的是________________。


