-
下列制取硫酸铜的实验设计中,能体现“经济、高效、环保”精神的最佳方案是( )
A.铜与浓硫酸共热
B.用铜片为阳极,石墨为阴极,电解稀硫酸
C.先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解
D.适当温度下,使铜片在持续通入空气的稀硫酸中溶解
高三化学单选题中等难度题查看答案及解析
-
下列制取硫酸铜的实验设计中,能体现“经济、高效、环保”精神的最佳方案是( )。
A.铜与浓硫酸共热
B.用铜片为阳极,石墨为阴极,电解稀硫酸
C.先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解
D.适当温度下,使铜片在持续通入空气的稀硫酸中溶解
高三化学选择题中等难度题查看答案及解析
-
化学实验设计或实际操作或储存时,能体现“经济、高效、环保、安全”方案是( )
A.Na 着火可以使用泡沫灭火器
B.绿色化学是指有毒气体尾气要经过无毒处理后在排放
C.实验室用浓硫酸溶解铜制备硫酸铜
D.实验室可以适当温度下,使铜片在持续通入空气的稀硫酸中溶解的方法制备硫酸铜
高三化学选择题简单题查看答案及解析
-
硫酸铜可用于消毒、制杀虫剂、镀铜等。实验小组制取CuSO4·5H2O晶体并进行热分解的探究。请回答以下问题:
探究Ⅰ:制取CuSO4·5H2O晶体
小组同学设计了如下两种方案:
甲:将铜片加入足量浓硫酸中并加热
乙:将铜片加入稀硫酸,控温40~50℃,滴加双氧水
(1)方案甲发生反应的化学方程式为____________,反应结束后有大量白色固体析出。简述从中提取CuSO4·5H2O晶体的方法:倒出剩余液体,____________。
(2)方案乙发生反应:Cu+H2SO4+H2O2=CuSO4+2H2O,该实验控温40~50℃的原因是________;与方案甲相比,方案乙的主要优点有_________、___________。(写出2种)
探究Ⅱ:用以下装置(加热装置省略)探究CuSO4·5H2O晶体热分解产物
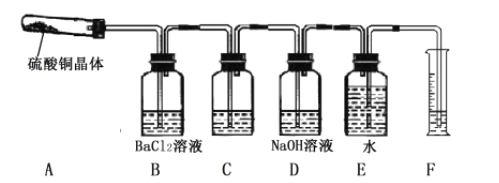
已知:CuSO4·5H2O脱水后升高温度,会继续分解成CuO 和气体产物,气体产物可能含有SO3、SO2、O2中的1~3 种。
(3)称5.00gCuSO4·5H2O于A 中加热,当观察到A中出现_____________,可初步判断晶体已完全脱水并发生分解。加热一段时间后,A中固体质量为3.00g,则此时A中固体的成分为___________。
(4)装置B中迅速生成白色沉淀,说明分解产物中有__________,C装置的作用是____________。
(5)理论上E中应收集到VmL气体,事实上体积偏少,可能的原因是______________。(不考虑泄漏等仅器与操作原因)。
高三化学填空题中等难度题查看答案及解析
-
为使反应:Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是( )
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
高三化学选择题简单题查看答案及解析
-
为使反应:Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
高三化学选择题简单题查看答案及解析
-
某化学兴趣小组设计如下实验方案,将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:
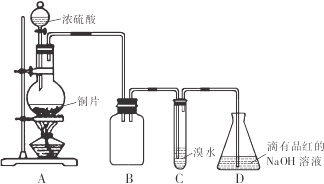
请回答下列问题:
(1)装置B的作用是______。
(2)设计装置C的目的是验证SO2的______性,装置C中发生反应的离子方程式是______装置D中NaOH全部转化为NaHSO3的标志是______。
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
序号
实验操作
现象
结论
①
加几小块CaCO3固体
有气泡产生
I或Ⅱ
②
滴加少量淀粉KI溶液,振荡
_______
Ⅲ
③
滴加少量溴水,振荡
_________
Ⅱ
④
滴加少量酸性KMnO4溶液、振荡
溶液为紫色
____
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb,的相对大小:___。
高三化学实验题中等难度题查看答案及解析
-
某化学兴趣小组设计如下实验方案。将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如下图所示:
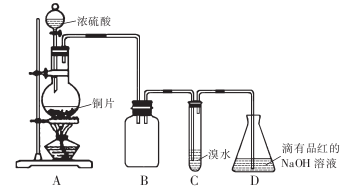
请回答下列问题:
(1)装置B的作用是________________
(2)设计装置C的目的是验证SO2的____________性,装置C中发生反应的离子方程式是____________。装置D中NaOH全部转化为NaHSO3的标志是________________。
(3)向NaHSO3溶液中加入NaCl0溶液时,反应有三种可能的情况:
I.HSO3-与ClO -恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HCl0)

(4)请设计简单实验证明:室温下HS03-的电离平衡常数Ka与水解平衡常数Kb,的相对大小:________
高三化学实验题极难题查看答案及解析
-
某化学兴趣小组设计如下实验方案。将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示。请回答下列问题:
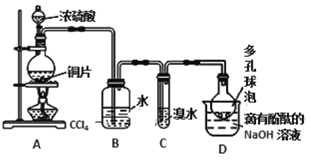
(1)装置B的作用是________________。
(2)装置C中发生反应的离子方程式是_____________________________。
SO2在装置D中完全转化为酸式酸根离子的过程中,溶液颜色变化是________。
(3)已知酸性:HCl>H2SO3>HClO。向Na2SO3溶液中加入盐酸酸化的NaClO溶液时,证明NaClO不足时的试剂是________。
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka大于其水解平衡常数Kh。______________。
高三化学实验题中等难度题查看答案及解析
-
某课外兴趣小组探究利用废铜屑制取CuSO4溶液,设计了以下几种实验方案。完成下列填空:
(1)方案一:以铜和浓硫酸反应制备硫酸铜溶液。方案二:将废铜屑在空气中灼烧后再投入稀硫酸中。和方案一相比,方案二的优点是________________________;方案二的实验中,发现容器底部残留少量紫红色固体,再加入稀硫酸依然不溶解,该固体为________。
(2)方案三的实验流程如图所示。
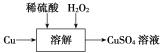
溶解过程中有气体放出,该气体是________。随着反应的进行,生成气体速率加快,推测可能的原因是________________________________________________________________________________。
(3)设计实验证明你的推测:______________________________。
方案四的实验流程如图所示。
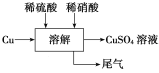
(4)为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为________;
(5)对方案四进行补充完善,设计一个既能防止污染,又能实现物料循环的实验方案(用流程图表示)__________________________________。
高三化学综合题中等难度题查看答案及解析