-
下表给出五种短周期元素的相关信息。
| 元素 | 相关信息 |
| A | 常温、常压下,其单质是最轻的气体,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化。该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 常温下其单质为黄绿色气体,其单质水溶液有漂白、杀菌作用 |
请按要求回答下列问题:
(1)D元素核外电子排布 ;
(2)A、B两元素形成的含有非极性键的化合物的结构式 ;A、B两元素形成的具有相同电子数的离子有(填化学式):______________、_____________。
(3)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1∶2)一起用作火箭助推剂,两者发生反应生成无毒物质,写出上述化学反应方程式: 。
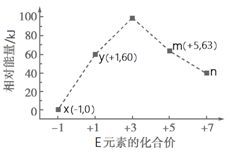
(4)一定条件下,在水溶液中1 mol E-、EO(x=1,2,3,4)的能量(kJ)相对大小如右图所示。n是 (填离子符号)。离子反应y→x+m的热化学方程式为 。
(5)Na2DB3水溶液中各离子浓度的大小顺序是 (填离子符号)
-
下表给出了五种元素的相关信息,其中A、B、C、D为短周期元素.
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料. |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障. |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂. |
| D | 室温下其单质呈粉末固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
| E | 它是人体不可缺少的微量元素,其单质也是工业生产中不可缺少的金属原材料,常用于制造桥梁、轨道等. |
(1)E在元素周期表中的位置是______ 。
(2)B和D对应的气态氢化物中,稳定性强的是 ______ ,熔沸点高的是 ______ (用具体的化学式表示)。
(3)D的单质与烧碱水溶液加热时发生自身氧化还原反应生成两种具有强还原性的阴离子,写出该反应的离子方程式 ______________。
(4)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1:2)一起用作火箭助推剂,写出两者发生反应生成无毒物质的化学方程式________。
(5)以上这五种元素组成一种工业上用途极广的复盐,该物质中A、B、C、D、E的质量比为5:56:7:16:14.则其水溶液的pH ______ 7(填“>”“=”或“<”),原因是______ (用离子方程式表示).溶液中离子浓度从大到小的顺序为 __________________ 。
-
X、Y、Z、U、V是元素周期表前四周期中的五种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | 地壳中含量最多的金属,其氧化物可用作耐火材料 |
| Y | 单质在常温常压下为黄绿色气体 |
| Z | 常温常压下,单质是淡黄色固体,常在火山口附近沉积 |
| U | 常温下单质遇浓硫酸钝化,其一种核素的质量数为56,中子数为30 |
| V | 属短周期元素,原子的最外层电子数是内层电子数的2/5 |
请回答下列问题:
(1)元素X位于周期表中第________周期第________族,其离子结构示意图为________。
(2)上述元素中最高价氧化物对应的水化物酸性最强的是________(写化学式),非金属气态氢化物还原性最强的是________(写化学式)。
(3)在碱性条件下,Y的单质可与UO2-反应制备一种可用于净水的盐UO42-,该反应的离子方程式是________。
(4)我国首创的海洋电池被大规模用于海洋灯塔。该电池是以X板为负极,铂网为正极,海水为电解质溶液,电池总反应为:4X+3O2+6H2O=4X(OH)3。该电池正极反应为________。
(5)已知25℃时,Ksp[U(OH)3]=2.63×10-39,则该温度下反应U(OH)3+3H+ U3++3H2O的平衡常数K=________。
U3++3H2O的平衡常数K=________。
-
X、Y、Z、W是短周期中常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X元素形成的一种同素异形体是天然晶体中硬度最大的单质 |
| Y | 常温常压下,Y单质是淡黄色固体,用于制造黑火药 |
| Z | Z的基态原子核外有3个能级上有电子,且有3个单电子 |
| W | W元素形成的双原子分子,常温下为黄绿色气体,一种常见工业原料 |
(1)W元素位于元素周期表中第________周期________族,与Y同主族且位于第四周期元素的基态原子核外电子排布式为________。
(2)XY2分子中含有的σ键和π键个数比为________,在相同条件下XY2与XO2相比,熔点较高的是________(填化学式)。结合相关理论解释Z所在族的元素第一电离能大于同周期后一族元素的原因:________。
(3)Y、W元素形成的化合物Y2W2和过量氢化物ZH3在无水条件下反应生成Y4Z4、单质Y8和一种可以作为化肥的物质,请写出相应化学方程式:________。
(4)已知:①lmolY(s)转化为气态Y(g) \吸收能量280 kJ;
②2XO(g)+O2(g)= 2XO2(g) ΔH=-566.0KJ/mol;
③Y(s)+O2(g)=YO2(g) ΔH=-299.0KJ/mol;一定条件下,可以利用X的氧化物XO和Y的氧化物YO2生成Y(g)单质和X的氧化物而达到消除污染目的。请写出该反应的热化学方程式:________。
-
X、Y、Z、W是元素周期表短周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的原子核外3个能级上有电子,且每个亚层上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的非金属性大于Y |
| W | W的一种同位素的质量数为28,中子数为14 |
(1)Y位在元素周期表位置是________________,
Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(2)XY2是一种常用的溶剂,XY2的分子的结构式为 。在H―Y、H―Z两种共价键中,
键的极性较强的是 。
(3)W的氧化物属于 晶体,请写出它的一种用途:_____________ 。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
XO(g)+ O2(g)→XO2(g)+283.0 kJ·mol
O2(g)→XO2(g)+283.0 kJ·mol
Y(g)+ O2(g)→YO2(g)+296.0 kJ·mol
此反应的热化学方程式是 。
-
(12分)X、Y、Z、M是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| M | M的一种核素的质量数为63,中子数为34 |
(1)属于主族元素的原子半径从大到小的顺序是(写化学式,下同)________,Y和Z的最高价氧化物对应的水化物的酸性较强的是________,在H-Y、H-Z两种共价键中,键的极性较强的分子是________。
(2)XY2是一种常用的溶剂,XY2的电子式是________,XY2的分子中存在________个σ键。
(3)M位于周期表第____周期第________族,M的基态原子核外电子排布式是________;M2Y在空气中煅烧生成M2O的化学方程式是________。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:XO(g)+ O2(g)= XO2(g) △H = -283.0 kJ·mol-1
O2(g)= XO2(g) △H = -283.0 kJ·mol-1
Y(g)+ O2(g)= YO2(g)△H = -296.0 kJ·mol-1
写出此反应的热化学方程式____________。
-
(12分)X、Y、Z、M是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| M | M的一种核素的质量数为63,中子数为34 |
(1)属于主族元素的原子半径从大到小的顺序是(写化学式,下同)________,Y和Z的最高价氧化物对应的水化物的酸性较强的是________,在H-Y、H-Z两种共价键中,键的极性较强的分子是________。
(2)XY2是一种常用的溶剂,XY2的电子式是________,XY2的分子中存在________个σ键。
(3)M位于周期表第____周期第________族,M的基态原子核外电子排布式是________;M2Y在空气中煅烧生成M2O的化学方程式是________。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:XO(g)+ O2(g)= XO2(g) △H = -283.0 kJ·mol-1
O2(g)= XO2(g) △H = -283.0 kJ·mol-1
Y(g)+ O2(g)= YO2(g)△H = -296.0 kJ·mol-1
写出此反应的热化学方程式____________。
-
(14分)
X、Y 、Z 、W是元素周期表前四周期中的四种常见元素,其相关信息如下表;
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1) Y位于元素周期表第_ 周期第)________族,Y和Z的最高价氧合物对应的水化物的酸性较强的是_ (化学式)
(2XY2是一种常用的溶剂,XY2的分子中存在_ 个 键。在H-Y,H-Z两种共价键中,键的极性较强的是________,键长较长的是________。
键。在H-Y,H-Z两种共价键中,键的极性较强的是________,键长较长的是________。
(3)W的基态原子核外电子排布式是________。W2Y在空气中煅烧生成的W2O化学方程式是________。
(4)处理含XO、YO2验到气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
XO(g)+ O2(g)=XO2(g) △H= -283.0kJ.mol-1
O2(g)=XO2(g) △H= -283.0kJ.mol-1
Y(s)+O2(g)=YO2(g) △H= -296.0 kJmol-1
此反应的热化学方程式是________
-
(14分)
X、Y 、Z 、W是元素周期表前四周期中的四种常见元素,其相关信息如下表;
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1) Y位于元素周期表第_ 周期第)________族,Y和Z的最高价氧合物对应的水化物的酸性较强的是_ (化学式)
(2XY2是一种常用的溶剂,XY2的分子中存在_ 个 键。在H-Y,H-Z两种共价键中,键的极性较强的是________,键长较长的是________。
键。在H-Y,H-Z两种共价键中,键的极性较强的是________,键长较长的是________。
(3)W的基态原子核外电子排布式是________。W2Y在空气中煅烧生成的W2O化学方程式是________。
(4)处理含XO、YO2验到气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
XO(g)+ O2(g)=XO2(g) △H= -283.0kJ.mol-1
O2(g)=XO2(g) △H= -283.0kJ.mol-1
Y(s)+O2(g)=YO2(g) △H= -296.0 kJmol-1
此反应的热化学方程式是________
-
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第 周期表 族,Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子核外电子排布式是 。W2Y在空气中煅烧生成W2O的化学方程式是 。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
XO(g)+ O2(g)=XO2(g)
O2(g)=XO2(g)  H=-283.0 kJ·mol-2
H=-283.0 kJ·mol-2
Y(g)+ O2(g)=YO2(g)  H=-296.0 kJ·mol-1
H=-296.0 kJ·mol-1
此反应的热化学方程式是 。
