-
常温下,用0.10 mol·L-1HCl溶液滴定20 mL 0.050 mol·L-1Na2CO3和0.025 mol·L-1NaHCO3混合溶液,得出如图所示的滴定曲线。下列说法不正确的是

A. a点溶液显碱性的主要原因:CO32-+H2O HCO3-+CH-
HCO3-+CH-
B. b点溶液中:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c点溶液中:c(Na+)=c(HCO3-)+2c(CO32-)+ c(Cl-)
D. d点溶液中:c(Na+)> c(Cl-)> c(HCO3-)>c(H+)>c(OH-)
-
常温下,用0.10 mol·L-1HCl溶液滴定20 mL 0.050 mol·L-1Na2CO3和0.025 mol·L-1NaHCO3混合溶液,得出如图所示的滴定曲线。下列说法不正确的是

A. a点溶液显碱性的主要原因:CO32-+H2O HCO3-+CH-
HCO3-+CH-
B. b点溶液中:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c点溶液中:c(Na+)=c(HCO3-)+2c(CO32-)+ c(Cl-)
D. d点溶液中:c(Na+)> c(Cl-)> c(HCO3-)>c(H+)>c(OH-)
-
常温下,用0.1000mol·L-1HCl溶液滴定10.00mL浓度为0.1000 mol·L-1Na2CO3溶液,所得滴定曲线如图所示。已知H2CO3的Ka1=10-6.4,Ka2=10-10.2,下列说法不正确的是
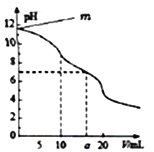
A. m=11.6
B. 当V=5 时,c(Na+)>c(CO32-) >c(HCO3-)>c(OH-)>c(H+)
C. 若用酚酞作指示剂,溶液由红色变为浅红色时,消耗盐酸体积约为10mL
D. 当V=a时c(Na+)>c(Cl-)>c(H+)=c(OH-)
-
常温下,用0.1mol•L-1HCl溶液滴定10.0mL浓度为0.1mol•L-1Na2CO3溶液,所得滴定曲线如图所示。下列微粒浓度大小关系正确的是
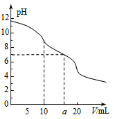
A.当V=0时:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-)
B.当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-)
C.当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D.当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-)
-
在常温下,0.10mol·L-1Na2CO3溶液25mL 用0.10mol·L-1盐酸滴定,其滴定曲线如图。对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )
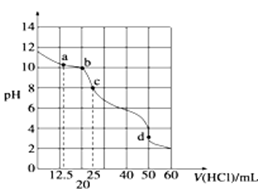
A.a点:c(CO2-3)=c(HCO-3)>c(OH-)
B.b点:5c(Cl-)>4c(HCO-3)+4c(CO2-3)
C.c点:c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3)
D.d点:c(H+)=c(CO2-3)+c(HCO-3)+c(OH-)
-
在常温下,下列说法正确的是
A.0.10mol·L-1Na2CO3溶液25mL 用0.10mol·L-1盐酸滴定。当滴定到消耗20mlHCl时所得溶液中离子浓度间的关系有:5c(Cl-)=4c(HCO3-)+4c(CO32-)+4c(H2CO3)
B.物质的量浓度相等的①(NH4)2CO3 ②(NH4)2SO4 ③(NH4)2Fe(SO4)2 三种溶液中水的电离程度:③>①>②
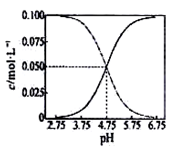
C.醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如右图所示,当pH=4.5溶液中:C(CH3COO-)>C(CH3COOH)>C(H+)>C(OH-)
D.等体积等物质的量浓度的NaF溶液与NaCl溶液中离子总数:N(NaF)> N(NaCl)
-
下列有关溶液中粒子浓度的关系式中一定不正确的是
A. 在常温下,0.10mol·L-1Na2CO3溶液25mL 用0.10mol·L-1盐酸滴定,当滴定到消耗20mLHCl时所得溶液中离子浓度间的关系有:5c(Cl-)=4c(HCO3-)+4c(CO32-)+4c(H2CO3)
B. pH=12的氨水与pH=2的盐酸等体积混合溶液中:c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+)
C. 25℃时,0.1 mol•L﹣1pH=4.5的NaHSO3溶液中:c(HSO3﹣)>c(H2SO3)>c(SO32﹣)
D. 常温下,等浓度的CH3COONa和CH3COOH混合溶液:c(CH3COO﹣)﹣c(CH3COOH)=2[c(H+)−c(OH−)]
-
下列有关溶液中粒子浓度的关系式中一定不正确的是
A.在常温下,0.10mol•L﹣1Na2CO3溶液25mL 用0.10mol•L﹣1盐酸滴定.当滴定到消耗20mlHCl时所得溶液中离子浓度间的关系有:5c(Cl﹣)=4c(HCO3﹣)+4c(CO32﹣)+4c(H2CO3)
B.常温下,pH=12的氨水与pH=2的盐酸等体积混合溶液中:c(NH4+)>c(Cl﹣)>c(OH﹣)>c(H+)
C.25℃时,0.1 mol•L﹣1pH=4.5的NaHSO3溶液中:c(HSO3﹣)>c(H2SO3)>c(SO32﹣)
D.常温下,等浓度的CH3COONa和CH3COOH混合溶液:c(CH3COO﹣)﹣c(CH3COOH)=2[c(H+)﹣c(OH﹣)]
-
向10 mL 0.1 mol·L-1Na2CO3溶液中逐滴滴加V mL 0.1 mol·L-1HCl溶液,下列有关滴定过程中粒子浓度关系正确的是
A.当V=0时,c(OH-)=c(H+)+c( )+c(H2CO3)
)+c(H2CO3)
B.当V=5时,c(Na+)+c(H+)=2c( )+c(
)+c( )+c(OH-)
)+c(OH-)
C.当V=10时,c(Cl-)=c( )+c(
)+c( )+c(H2CO3)
)+c(H2CO3)
D.当V=15时,c(Na+)=c(Cl-)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
-
常温下,在10 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是
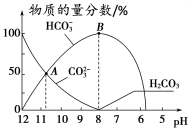
A. 在0.1 mol·L-1Na2CO3溶液中:c(Na+)+c(H+)=c(CO )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)
B. 当溶液的pH为7时,溶液的总体积为20 mL
C. 在B点所示的溶液中,离子浓度最大的是HCO
D. 在A点所示的溶液中:c(CO )=c(HCO
)=c(HCO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)

HCO3-+CH-





