-
亚硫酸钠是工业中重要的原料。某亚硫酸钠样品因在空气中放置而被部分氧化为硫酸钠。某化学实验小组设计实验测定样品中亚硫酸钠的含量。
(1)甲方案
①准确称取5.0g样品放入烧杯中,加足量稀盐酸,充分搅拌溶解。
②边搅拌边滴加1mol·L-1BaCl2溶液至过量
③过滤,洗涤,干燥,称得固体质量为m1g
(2)乙方案
准确称取5.0g样品置于右图锥形瓶中,并通一段时间N2。打开分液漏斗活塞,逐滴加入70%硫酸至不再产生气体。再通入一段时间N2,最终称得C装置反应前后增重m2g
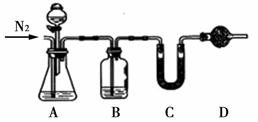
回答下列问题
(1)甲方案步骤①中发生了离子反应,其离子方程式为________。
(2)如何判断步骤②中滴加BaCl2溶液已过量___________。
(3)甲方案测得的样品中亚硫酸钠的含量为___________(用含带m1的代数式 表示)
表示)
(4)乙方案中第一次通入氮气的目的是___________。
(5)乙方案中B装置的作用是______,若C、D置中药品相同,则是______(填药品名称),若无D装置,测定结果___(填“偏大”、“偏小”、“无影响”)
(6)有同学设计实验通过测量产生的SO2气体体积来测定样品中的亚硫酸钠含量,下列实验装置最准确、最恰当的是_________。
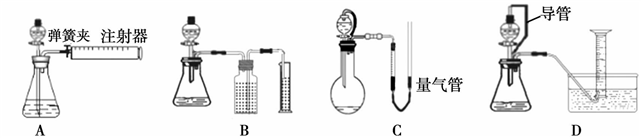
-
亚硫酸盐是一种常见的食品添加剂。为检验某食品中亚硫酸盐含量(通常以1kg样品中含 的质量计),某研究小组同学设计了如下实验方案。
的质量计),某研究小组同学设计了如下实验方案。
I.称取样品W g;
II.向样品中加人足量稀硫酸:
III.将II中产生的 ,用足量
,用足量 溶液吸收;
溶液吸收;
IV.将III所得硫酸溶夜用氢氧化钠溶液滴定;
V.数据处理。
(1) 是一种食品添加剂。写出
是一种食品添加剂。写出 与稀
与稀 反应的离子方程式:____________
反应的离子方程式:____________
(2)步骤中H2O2的作用是 __________________________
(3)步骤N中可选用的指示剂为__________。下图显示滴定终点时,滴定管(量程为25mL)读数为_______________。

(4)步骤IV中消耗 溶液V mL,则1 kg样品中含
溶液V mL,则1 kg样品中含 的质量是__________g(用含W、V的代数式表示)。
的质量是__________g(用含W、V的代数式表示)。
(5)此实验方案测得亚硫酸盐含量偏低,步骤II会产生该误差,请说明理由。(写出2条)_______________________。
-
亚硫酸盐是一种常见的食品添加剂。为检验某食品中亚硫酸盐含量(通常以1kg样品中含 的质量计),某研究小组同学设计了如下实验方案。
的质量计),某研究小组同学设计了如下实验方案。
I.称取样品W g;
II.向样品中加人足量稀硫酸:
III.将II中产生的 ,用足量
,用足量 溶液吸收;
溶液吸收;
IV.将III所得硫酸溶夜用氢氧化钠溶液滴定;
V.数据处理。
(1) 是一种食品添加剂。写出
是一种食品添加剂。写出 与稀
与稀 反应的离子方程式:____________
反应的离子方程式:____________
(2)步骤中H2O2的作用是 __________________________
(3)步骤N中可选用的指示剂为__________。下图显示滴定终点时,滴定管(量程为25mL)读数为_______________。
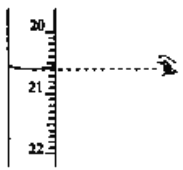
(4)步骤IV中消耗 溶液V mL,则1 kg样品中含
溶液V mL,则1 kg样品中含 的质量是__________g(用含W、V的代数式表示)。
的质量是__________g(用含W、V的代数式表示)。
(5)此实验方案测得亚硫酸盐含量偏低,步骤II会产生该误差,请说明理由。(写出2条)_______________________。
-
亚硫酸盐是一种常见的食品添加剂。为检验某食品中亚硫酸盐含量(通常以1 kg样品中含SO2的质量计),某研究小组同学设计了如下实验流程(所加试剂均为足量)。

请回答:
(1)亚硫酸盐作为食品添加剂的作用是 (填字母)。
a.防腐保鲜 b.增强营养
(2)反应①中通入N2的目的是 (填字母)。
a.冷却产生的气体
b.与生成的气体反应
c.将生成的气体全部赶出
(3)反应①~③中属于氧化还原反应的是 (填序号)。
(4)若取样品X g,反应③消耗0.01 mol/L NaOH溶液100 mL,则1 kg样品中含SO2的质量是 g(用含X的代数式表示)。
-
(8分)亚硫酸盐是一种常见的食品添加剂。为检验某食品中亚硫酸盐含量(通常以1 kg样品中含SO2的质量计),某研究小组同学设计了如下实验流程(所加试剂均为足量)。

 请回答:
请回答:
(1)亚硫酸盐作为食品添加剂的作用是 (填字母)。
a.防腐保鲜 b.增强营养
(2)反应①中通入N2的目的是 (填字母)。
a.冷却产生的气体
b.与生成的气体反应
c.将生成的气体全部赶出
(3)反应①~③中属于氧化还原反应的是 (填序号)。
(4)若取样品X g,反应③消耗0.01 mol/L NaOH溶液100 mL,则1 kg样品中含SO2的质量是 g(用含X的代数式表示)。
-
亚硫酸盐是一种常见食品添加剂。为检测某食品中亚硫酸盐含量(通常以1 kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:
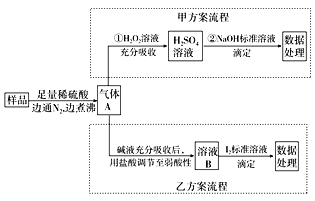
(1)甲方案第①步利用了H2O2的______性,H2O2是二元弱酸,写出H2O2电离方程式________________________
(2)甲方案第②步选酚酞做指示剂进行滴定,应选择图中________滴定管(填标号)。滴定时边滴边摇动锥形瓶,眼睛应观察________。

A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是__________________________________________
(3)写出乙方案滴定时的离子方程式:___________________________________。
(4)按乙方案若取样品20g配成100mL溶液,滴定消耗0.01000 mol·L-1 I2溶液的体积如表所示:
| 滴定次数 | 待测溶液 体积/mL | 标准溶液的体积/mL |
| 滴定前刻度 | 滴定后刻度 |
| 1 | 20.00 | 1.02 | 21.03 |
| 2 | 20.00 | 2.00 | 25.00 |
| 3 | 20.00 | 0.60 | 20.59 |
滴定中误差较大的是第________次实验,造成这种误差的可能原因是________。
A.滴定管在装液前未用标准溶液润洗2~3次
B.滴定开始前滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
则1 kg样品中含SO2的质量是________g。
-
(12分)重铬酸钠Na2Cr2O7·2H2O俗称红矾钠,是一种重要的无机盐产品,可作氧化剂,在印染、颜料、电镀、医药等工业方面有广泛的用途。某化学兴趣小组设计实验测定市场上的红矾钠中Na2Cr2O7的质量分数,其步骤如下:
I.称取Wg红矾钠,溶于酸配成l00mL溶液;
Ⅱ.用cmol·L-1的标准KMnO4酸性溶液滴定20.00mL一定浓度的FeSO4溶液,消耗KMnO4溶液20.00rnL;
Ⅲ.取20.00mL Na2Cr2O7溶液,用上述FeSO4溶液滴定,达到滴定终点时,消耗24.00mLFeSO4溶液;
查阅资料知:Cr相对原子质量为52
Cr2O2-7具有强氧化性,在酸性条件下易被还原为Cr3+
回答下列问题:
(1)Na2Cr2O7与FeSO4的反应离子方程式为.
(2)步骤Ⅱ中的滴定过程选用________(填“酸式”或“碱式”)滴定管。
(3)已知:MnO-4+5Fe2++8H+==Mn2++5Fe3++4H2O,此红矾钠中Na2Cr2O7的质量分数的表达式为________。
(4)判断下列操作对Na2Cr2O7的质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”):
①步骤Ⅲ中的滴定过程,滴定终点读数时俯视读数________;
②配制c mol·L-1的KMnO4标准溶液时,转移时有少量溶液洒出________。
(5)有同学提出FeSO4有很强的还原性,在空气中易被氧化而变质,因此对测定结果会造成影响,请你分析后指出,如果FeSO4变质,对测定结果的影响是________(填“偏高”、“偏低”或“无影响”)。
-
某化学学习小组设计以下实验方案:测定某含有NaCl的小苏打样品中 的质量分数。已知:
的质量分数。已知: 受热分解成碳酸钠、二氧化碳和水。
受热分解成碳酸钠、二氧化碳和水。
(方案一)称取一定质量样品,置于仪器A中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)仪器A的名称为___________;A应该放在_________中冷却。恒重操作的目的是________。
(2)本实验从称量空的A仪器开始,完成一次平行实验至少需要称重____次。做平行实验的目的是___________。
(方案二)称取一定质量的样品(样品的质量为m0),置于小烧杯中,加适量水溶解;向小烧杯中加入足量澄清石灰水,过滤,洗涤、干燥,称量沉淀的质量为m1,计算。(已知碳酸钙式量为100, 的式量为84)。
的式量为84)。
(3)反应方程式为_____________,则样品中 的质量分数可以表示为_________。
的质量分数可以表示为_________。
(方案三)往Y形管中注入一定体积和浓度的稀硫酸并放入准确称取的ag样品,连接好注射器(如图),再将Y形管倾斜,使样品与酸液充分反应。
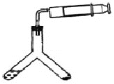
(4)a不能太大,理由是___________,若测定结果偏高,其原因可能是______(选填序号)。
①样品未完全反应
②温度未恒定即记录数据
③少量 溶解在溶液中
溶解在溶液中
(方案四)称取一定质量样品,配成待测溶液,用标准盐酸滴定。
(5)下列叙述正确的是_______(选填序号)。
①用烧杯配制100mL待测溶液
②用酚酞为指示剂
③当滴至待测液变色并能将该颜色保持半分钟即为滴定终点
④盛盐酸的滴定管未润洗会造成实验结果偏高
-
某实验小组为测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量Wg样品进行实验,下列实验方法所对应的实验方案和测量数据最合理的是

A. A B. B C. C D. D
-
(14分)某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应:
4FeS2+11O2 2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2,进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。

实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。
(已知:5SO2 + 2KMnO4 + 2H2O == K2SO4 + 2MnSO4 + 2H2SO4 )
请回答下列问题:
(1)称量样品质量能否用托盘天平________(填“能”或“不能”);
(2)装置a的作用是________ ________;
(3)上述反应结束后,仍需通一段时间的空气,其目的是 ;
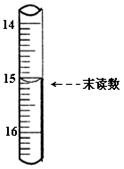
(4)滴定时,发生反应的离子方程式为________,已知滴定管初读数为0.10mL,末读数如上图所示,消耗草酸溶液的体积为 ________mL;
(5)该样品中FeS2的纯度为;
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是________。(填编号)
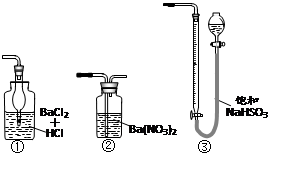

表示)





 请回答:
请回答:





