-
由两种元素组成的化合物M,是某种具有优异磁学性质的新型电子材料的主要成分。其制备流程如下:
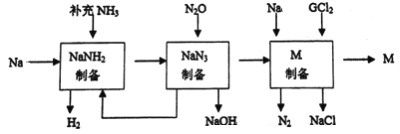
取2.38g 的M 用足量稀硫酸溶解,在所得反应液中加入足量的NaOH溶液,发现有刺激性气味且能使湿润红色石蕊试纸变蓝的气体产生,同时溶液中产生白色沉淀,迅速变成灰绿色,最终变为红褐色,沉淀灼烧后质量为3.20g。请回答:
(1)写出NaNH2的电子式________, M的化学式________________;
(2)根据图示信息,用一个化学方程式表示NaN3制备方法_________________________。
-
(12分)纳米ZnS具有独特的光电效应,在电学、磁学、光学等领域应用广泛。以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
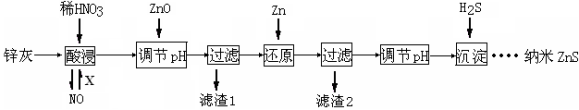
请回答下列问题。
(1)酸浸时FeO与稀HNO3反应的离子方程式 。
(2)将酸浸的尾气循环利用,加入的X气体可以是 。
(3)流程中加入ZnO调pH的目的是 。
(4)滤渣2中的成分是 。
(5)已知ZnS的溶度积Ksp=1.6×10-24,溶液中Zn2+浓度为0.01mol·L-1,则溶液中S2—浓度大于 mol·L一1,才生成ZnS沉淀。
(6)试设计简单实验方案,判断所得ZnS样品颗粒是否为纳米级 。
-
纳米ZnS具有独特的光电效应,在电学、磁学、光学等领域应用广泛.以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:(已知Ksp=3.810﹣38; Ksp=210﹣20;Ksp(ZnS)=1.610﹣24)
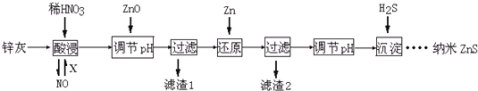
下列说法不正确的是:
A. 酸浸时FeO与稀HNO3反应的离子方程式为3FeO+10H++ NO3﹣═3Fe3++NO↑+5H2O
B. 将酸浸的尾气循环利用,加入的X气体可以是O2
C. 滤渣2中的成分是Zn和Fe
D. 当溶液中Zn2+浓度为小于1.010﹣5mol•L﹣1时,则可认为其沉淀完全.若要使Zn2+沉淀完全,溶液中S2﹣浓度应大于1.610﹣19mol•L﹣1
-
纳米ZnS具有独特的光电效应,在电学、磁学、光学等领域应用广泛.以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
(已知Ksp[Fe(OH)3]=3.8×10﹣38; Ksp[Cu(OH)2]=2×10﹣20;Ksp(ZnS)=1.6×10﹣24)
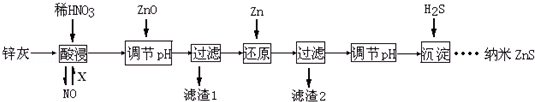
下列说法不正确的是
A.酸浸时FeO与稀HNO3反应的离子方程式为3FeO+10H++NO ═3Fe3++NO↑+5H2O
═3Fe3++NO↑+5H2O
B.将酸浸的尾气循环利用,加入的X气体可以是O2
C.滤渣2中的成分和Zn和Fe
D.当溶液中Zn2+浓度为小于1.0×10﹣5mol•L﹣1时,则可认为其沉淀完全.若要使Zn2+沉淀完全,溶液中S2﹣浓度应大于1.6×10﹣19mol•L﹣1
-
铅及其化合物有着优异的性能和广泛的应用。工业上利用铅浮渣(主要成分是PbO、Pb还含有少量的Ag、CaO) 可制备硫酸铅。制备流程图如下:
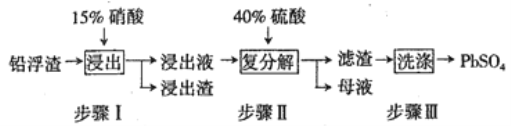
已知: Ksp(PbSO4)=1.6×10-8Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生,浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式__________________,为防止Ag被溶解进入溶液,步骤I操作时应注意____________。
(2)粗PbSO4产品含有的杂质是________;要得到纯净的PbSO4,需要用试剂进行多次洗涤,再用蒸馏水洗涤。最好选用的试剂是__________________。
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的SO42-过多,循环利用时可能出现的问题是_____________________。
(4)若将步骤II中的Pb2+完全沉淀,则溶液中的c(SO42-)至少为_____mol/L。
(5)(CH3COO)2Pb是皮毛行业的染色助剂,可用PbSO4 与CH3COONH4反应制备,写出反应的离子方程式_________________________。
-
铅及其化合物有着优异的性能和广泛的应用。工业上利用铅浮渣(主要成分是PbO、Pb,还含有少量的Ag、CaO)制备硫酸铅。制备流程图如下
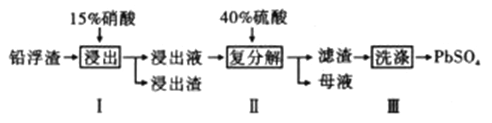
已知:Ksp(PbSO4)=1.6×10-8 Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式___________________________,为防止Ag被溶解进入溶液,步骤I操作时应注意_______________________。
(2)粗PbSO4产品含有的杂质是____________;要得到纯净的PbSO4,需要用试剂进行多次洗涤,再用蒸馏水洗涤。最好选用的试剂是_________________。
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的SO42-过多,循环利用时可能出现的问题是______________________________。
(4)若将步骤Ⅱ中的Pb2+完全沉淀,则溶液中的c(SO42-)至少为___________mol/L。
(5)(CH3COO)2Pb是皮毛行业可溶于水的染色助剂,可用PbSO4与CH3 COONH4反应制备,写出该反应的离子方程式_______________________。
(6)铅蓄电池是电压稳定、使用方便的二次电池。PbSO4在其中扮演了重要角色,写出铅蓄电池充电时阳极的电极反应_______________________。
-
高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上以菱铁矿(主要成分是FeCO3及少量SiO2)为原料制备高铁酸钠生产过程如下:
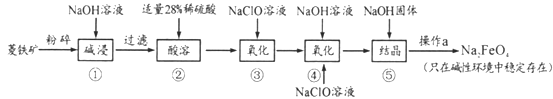
(1)Na2FeO4中铁元素的化合价为___,高铁酸钠用于杀菌消毒时的化学反应类型为____(填“氧化还原反应”、“复分解反应”或“化合反应”)。
(2)按照上述流程,步骤①中碱浸时能否用较便宜的Ca(OH)2替代NaOH_____(填“能”或“不能”),理由是___________。
(3)步骤②中28%的稀硫酸需要用98%的浓硫酸配制,配制时所需玻璃仪器除量筒外,还____(填字母序号)。步骤③中检验Fe2+全部转化成Fe3+的方法是:__________。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒 E.酸式滴定管;
(4)步骤④中除生成Na2FeO4外,还有NaCl生成,其离子方程式为_________;己知步骤⑤是向Na2FeO4溶液中继续加入氢氧化钠固体得到悬浊液,则操作a的名称为_____。
(5)理论上,每获得0.5mol的FeO42-消耗 NaClO的总质量为_____。
-
高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上以菱铁矿(主要成分是FeCO3及少量SiO2)为原料制备高铁酸钠生产过程如下:
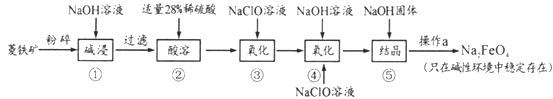
(1)Na2FeO4中铁元素的化合价为___,高铁酸钠用于杀菌消毒时的化学反应类型为____(填“氧化还原反应”、“复分解反应”或“化合反应”)。
(2)按照上述流程,步骤①中碱浸时能否用较便宜的Ca(OH)2替代NaOH_____(填“能”或“不能”),理由是___________。
(3)步骤②中28%的稀硫酸需要用98%的浓硫酸配制,配制时所需玻璃仪器除量筒外,还____(填字母序号)。步骤③中检验Fe2+全部转化成Fe3+的方法是:__________。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒 E.酸式滴定管;
(4)步骤④中除生成Na2FeO4外,还有NaCl生成,其离子方程式为_________;己知步骤⑤是向Na2FeO4溶液中继续加入氢氧化钠固体得到悬浊液,则操作a的名称为_____。
(5)理论上,每获得0.5mol的FeO42-消耗 NaClO的总质量为_____。
-
新能源汽车的大力推广,带动锂电池材料的发展。我国科学家研发出利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 、
、 、
、 等杂质)制备锂离子电极材料—
等杂质)制备锂离子电极材料— 和
和 的工艺流程如下:
的工艺流程如下:
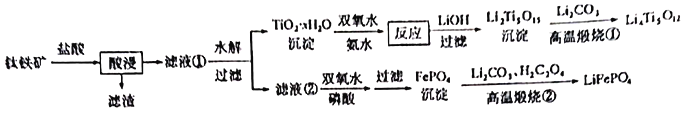
回答下列问题:
(1) 中,Fe元素的化合价为____________。
中,Fe元素的化合价为____________。
(2)“酸浸”后,钛主要以 形式存在,写出
形式存在,写出 水解的的离子方程式_________________。
水解的的离子方程式_________________。
(3) 沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
|  转化率/% 转化率/%
| 92 | 95 | 97 | 93 | 88 |
分析高于40℃时 转化率下降的原因_______________。
转化率下降的原因_______________。
(4) 中Ti的化合价为
中Ti的化合价为 ,其中过氧键的数目为_____________。
,其中过氧键的数目为_____________。
(5)滤液②中加入双氧水和磷酸,反应生成 的离子方程式为____________;若测得Fe3+沉淀完全后,溶液中
的离子方程式为____________;若测得Fe3+沉淀完全后,溶液中 为
为 ,则常温下溶液的pH=______________。(已知
,则常温下溶液的pH=______________。(已知 的
的 )
)
(6)从滤液②中得到 沉淀之后,要对其进行洗涤、干燥,检验沉淀已经洗涤干净的方法_________________________________________。
沉淀之后,要对其进行洗涤、干燥,检验沉淀已经洗涤干净的方法_________________________________________。
-
锶(Sr)为第五周期IIA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
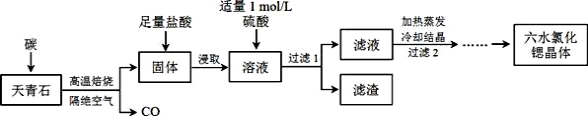
(1)SrCl2的电子式为_____________。
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_______________________。
(3)加入硫酸的目的是______________________。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L(注:此时滤液中Ba2+浓度为1×10-5mol/L;SrSO4和BaSO4溶度积常数依次为3×10-7、1×10-10。)
(4)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO31.100×10-2mol的AgNO3溶液(溶液中除Cl-外,不含其它与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_______________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______________(保留4位有效数字)。
(5)工业上常用电解熔融SrCl2制锶单质。由SrCl2·6H2O制取无水氯化锶的方法是_________。









