-
向H2O2溶液中加入适量稀硫酸酸化的硫酸亚铁溶液,依次观察到如下现象:①反应刚开始,仅有少量气泡产生;②反应片刻后,有大量气泡产生;③试管底部最终出现红褐色沉淀。下列判断正确的是
A.①中仅发生一个反应 B.Fe3+能催化H2O2的分解
C.反应过程中溶液pH不断减小 D.FeSO4与等物质的量的H2O2恰好反应
高三化学选择题困难题查看答案及解析
-
向H2O2溶液中加入适量稀硫酸酸化的硫酸亚铁溶液,依次观察到如下现象:①反应刚开始,仅有少量气泡产生;②反应片刻后,有大量气泡产生;③试管底部最终出现红褐色沉淀。下列判断正确的是
A.①中仅发生一个反应 B.Fe3+能催化H2O2的分解
C.反应过程中溶液pH不断减小 D.FeSO4与等物质的量的H2O2恰好反应
高三化学选择题困难题查看答案及解析
-
下列实验操作对应的现象或结论均正确的是( )
选项
操作
现象
结论
A
向H2O2溶液中滴加少量硫酸酸化的FeSO4溶液
溶液变为棕黄色后迅速出现大量气泡
Fe2+催化H2O2发生分解反应生成O2
B
将相同体积、相同pH的盐酸和醋酸溶液分别稀释a倍、b倍
稀释后溶液pH相同
a>b
C
向25mL沸水中滴加5~6滴FeCl3饱和溶液,继续煮沸
生成红褐色沉淀
制得Fe(OH)3胶体
D
相同温度下,测定等浓度的NaHCO3和NaHSO4溶液的pH
前者pH比后者的大
非金属性:S>C
A.A B.B C.C D.D
高三化学单选题中等难度题查看答案及解析
-
下列实验、现象与结论正确且相符的是( )
实验
现象
结论
A
向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液
溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成
Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动
B
将充满NO2的密闭玻璃球浸泡在热水中
红棕色变深
反应:
2NO2 (g)
N2O4(g)ΔH<0
C
SO2通入新制氯水
溶液褪色
SO2具有漂白性
D
向2支盛有2mL相同浓度硝酸银溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液
一支无明显现象,另一支产生黄色沉淀
相同条件下,AgI比AgCl的溶解度大
A. A B. B C. C D. D
高三化学单选题中等难度题查看答案及解析
-
某小组电解K2Cr2O7溶液,研究过程如下:
实验一 电压不同时,用石墨电极电解硫酸酸化的pH=2.5的饱和K2Cr2O7 溶液,实验现象如下:
电压/V
实验现象
2.0
阳极缓慢产生少量气泡,阴极没有气泡
3.0
阳极产生较多气泡,阴极产生少量气泡
>5.0
两极均快速产生大量气泡,阴极产生气泡的速率约为阳极的2倍
(1)阳极产生的气体是______________________。
(2)电压为2.0 V时,阴极区检出Cr3+,结合实验现象判断在阴极放电的主要离子是_______。
(3)电压高于5.0 V时,被电解的主要物质是______________。
实验二 探究其他因素对电解K2Cr2O7溶液的影响。用相同强度的稳恒电流(单位时间内转移的电子数始终相同),分别电解3份500 mL相同浓度的K2Cr2O7溶液,电解时间均为30 min。实验结果如下:
实验序号
Ⅰ
Ⅱ
Ⅲ
电极材料
阴极:石墨
阳极:石墨
阴极:石墨
阳极:石墨
阴极:石墨
阳极:铁
加入的物质
1 mL浓硫酸
1 mL浓硫酸、
少量硫酸铁
1 mL浓硫酸
电极表面是否产生气泡
两极均产生气泡
两极均产生气泡
阴极:产生气泡
阳极:无明显气泡产生
Cr2O72−还原率/%
12.7
20.8
57.3
阴极变化
实验结束后取出电极,仅Ⅰ中阴极上附着银白色固体,经检验为金属Cr
(4)对比Ⅰ、Ⅱ可知,阴极表面是否析出金属Cr,以及Ⅱ中Cr2O72−的还原率提高均与______填离子符号)有关。
(5)Ⅲ中Cr2O72−还原率较Ⅰ、Ⅱ有较大提高,分析其原因:
①阳极区:阳极反应:_______,进而使Cr2O72−被还原。
②阴极区:由于_______,进而促进了Cr2O72−在阴极区被还原,依据的实验现象是___________。
(6)工业上处理含Cr2O72−的废水,用铁作阳极,控制一定的电压,初始pH为3~4,将Cr2O72−最终转化为难溶的Cr(OH)3除去,结合上述实验,电压不宜过高、pH不宜过小的目的,除节约成本和防止腐蚀设备外,还有__________。
高三化学实验题中等难度题查看答案及解析
-
在稀硫酸中加入适量铁粉,反应完全后再加入适量氢氧化钠溶液,放置片刻,从反应体系中观察到颜色变化是( )
A.无色→灰绿色→红褐色
B.无色→浅绿色→白色→灰绿色→红褐色
C.灰绿色→绿褐色→蓝色
D.无色→白色→浅绿色→灰绿色→红褐色
高三化学选择题简单题查看答案及解析
-
在稀硫酸中加入适量铁粉,反应完全后再加入适量氢氧化钠溶液,放置片刻,从反应体系中观察到颜色变化是( )
A.无色→灰绿色→红褐色
B.无色→浅绿色→白色→灰绿色→红褐色
C.灰绿色→红褐色→蓝色
D.无色→白色→浅绿色→灰绿色→红褐色
高三化学选择题简单题查看答案及解析
-
下列实验现象是因为放热引起的是( )
A.将HCl通入水中,液面沿着导管上升
B.将浓硫酸快速加入水中,水沸腾、飞溅
C.向H2O2溶液中加入少量MnO2粉末,大量气泡生成
D.向溴水中加入CCl4,振荡后静置一段时间,水层褪色
高三化学单选题简单题查看答案及解析
-
锰及其化合物有广泛应用。
(1)在稀硫酸酸化的双氧水中加入二氧化锰粉末,产生大量气泡,且黑色固体消失;向反应完全后的溶液中加入高锰酸钾溶液生成黑色沉淀。经检测:1mol KMnO4完全反应转移3mol电子。在双氧水参与的反应中,二氧化锰除了作催化剂还作 ;写出加入高锰酸钾后产生黑色沉淀的离子方程式 。
(2)菱锰矿是生产铁锰合金中锰的来源,其主要成分是碳酸锰。已知锰常见的化合价有+2、+4、+6、+7。在空气中灼烧菱锰矿生产四氧化三锰,然后用铝热反应制备锰。写出菱锰矿粉末在空气中高温灼烧生成四氧化三锰的化学方程式 。如果冶炼1100kg锰,理论上消耗铝的质量为 kg。

(3)工业生产中为了制备硫酸锰,往往将硫酸锰溶液中亚铁离子氧化成铁离子,调节pH除去铁离子。向混合溶液中滴加稀硫酸酸化,加入软锰矿(主要成分是二氧化锰)氧化亚铁离子,写出该过程的离子方程式 。
(4)酸性高锰酸钾可氧化乙醇,配平下列反应方程式:
KMnO4+ H2SO4+ CH3CH2OH= K2SO4+ MnSO4+ CH3COOH+ □。
高三化学填空题困难题查看答案及解析
-
下列有关实验的叙述正确的是
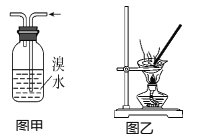
A. 向KI溶液中加入淀粉,然后滴入少量稀硫酸,开始无明显现象,片刻后溶液变蓝,则证明氧化性:H2SO4>I2
B. 图甲用于除去乙烯中的SO2
C. 用图乙装置蒸干明矾溶液制KAl(SO4)2·12H2O晶体
D. 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
高三化学单选题中等难度题查看答案及解析