-
(12分) 从回收的含铜电缆废料中提取铜时,假若设计如下两种方案,回答有关问题。
方案甲:
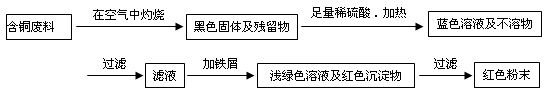
方案乙:
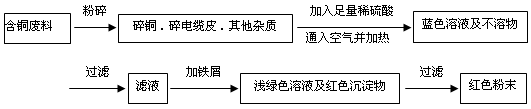
(1)两个方案中,符合当前生产中绿色化学理念的是方案________,理由是________。
(2)方案乙中铜溶解生成蓝色溶液时发生反应的离子方程式为________________________,
若不考虑绿色化学要求,溶解铜生成硫酸铜时,还可将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使铜溶解完全,则理论上硫酸和硝酸的物质的量之比最佳为:________︰________。
(3)为了提高原料的利用率,最后一步所得浅绿色滤液通过蒸发浓缩、冷却结晶、过滤、洗涤、自然干燥可得到一种结晶水合物的晶体。获得晶体后对其进行检测:
①先取a g的晶体进行脱水实验,获得无水固体为(a—1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。
通过计算测知该晶体的化学式是________。
(4)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上用硫酸铜等原料常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3 = 2 CuCl ↓+ 3 Na2SO4 + CO2↑
测定CuCl质量分数时先准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3 溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:
Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+ = Fe 3+ + Ce3+
通过计算说明上述样品中CuCl的质量分数是否符合标准。
-
从回收的含铜电缆废料中提取铜时,假若设计如下两种方案,回答有关问题。
方案甲:
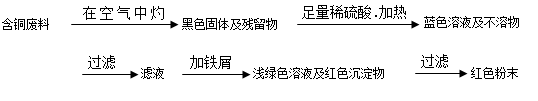
方案乙:

(1)两个方案中,符合当前生产中绿色化学理念的是方案________,理由是________方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾。
(2)方案乙中铜溶解生成蓝色溶液时发生反应的离子方程式为________________ _ ______。
(3)为了提高原料的利用率,最后一步所得浅绿色滤液通过蒸发浓缩、冷却结晶、过滤、洗涤、自然干燥可得到一种结晶水合物的晶体。获得晶体后对其进行检测:
①先取a g的晶体进行脱水实验,获得无水固体为(a—1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。通过计算测知该晶体的化学式是________。
(4)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上用硫酸铜等原料常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3=2 CuCl ↓+ 3 Na2SO4 + CO2↑
测定CuCl质量分数时先准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3 溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+ =Fe 3+ + Ce3+
计算上述样品中CuCl的质量分数为________。
-
(16分)某化学研究性小组同学提出回收含铜电缆废料中提取铜的两种方案,并向老师咨询,老师就以下几个方面与同学们展开讨论:
方案甲:
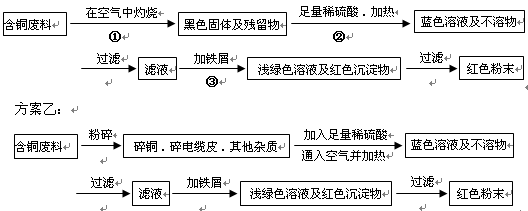
(1)两个方案哪个符合当前生产的绿色理念,为什么?
________.
(2)写出方案甲中的②③步骤与铜有关的离子反应的离子方程式。
__________________ _ __________
_________________ _________。
(3)老师建议,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑,目的是:________。
(4)老师请同学们用化学方法检验红色粉末中是否含有过量的铁屑。请你填写下列表格写出实验操作、预期实验现象、结论及操作(②中相关的离子方程式)。
| 序号 | 实验操作 | 实验现象 | 结论及离子方程式 |
| ① | 取适量的样品于试管内 | —— | —— |
| ② | 用滴管滴入足量硫酸溶液,并充分振荡试管 | | |
| ③ | | 溶液先黄色,滴入KSCN溶液后显红色 | |
| | | |
(5)为了提高原料的,老师建议把最后一步所得浅绿色滤液通过蒸发.冷却结晶.过滤.洗涤.自然干燥得到一种带结晶水的硫酸亚铁晶体。
研究小组按老师的建议完成上面操作步骤,获得晶体后对其进行检测
①先取a g的晶体进行脱水实验,获得无水固体为(a—1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。研究小组通过计算测知该晶体的化学式是________。
-
某化学研究性小组同学提出回收含铜电缆废料中提取铜的两种方案,并向专家咨询,专家就以下几个方面与同学们展开讨论:
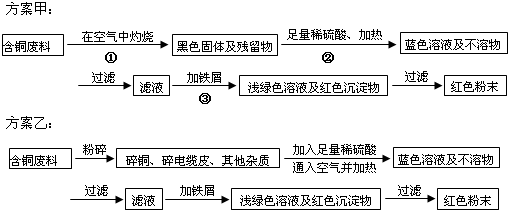
(1)两个方案哪个符合当前生产的绿色理念,为什么?______.
(2)方案甲中的②③步骤与铜有关的反应是离子反应吗?若是,写出离子方程式.______.
(3)专家建议,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑,目的是:______.
(4)专家请同学们用简便的方法检验红色粉末中是否含有过量的铁屑,同学们运用所学的知识提出了几种方案,请你写出其中的一种方案.______.
(5)为了提高原料的利用率,专家建议把最后一步所得浅绿色滤液通过蒸发、冷却结晶、______、洗涤、自然干燥得到一种带结晶水的硫酸亚铁晶体.研究小组按专家的建议完成上面操作步骤,获得晶体后对其进行检测
①先取a g的晶体进行脱水实验,获得无水固体为(a-1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全.
研究小组通过计算测知该晶体的化学式是______.
-
某化学研究性小组同学提出回收含铜电缆废料中提取铜的两种方案,并向专家咨询,专家就以下几个方面与同学们展开讨论:
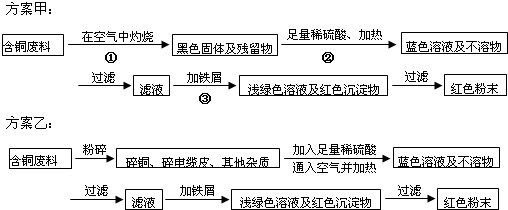
(1)两个方案哪个符合当前生产的绿色理念,为什么?______.
(2)方案甲中的②③步骤与铜有关的反应是离子反应吗?若是,写出离子方程式.
②______③______.
(3)专家建议,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑,目的是:______.
(4)专家请同学们用简便的方法检验红色粉末中是否含有过量的铁屑,同学们运用所.
-
某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示两个方案,并提出下列问题:
方案甲:
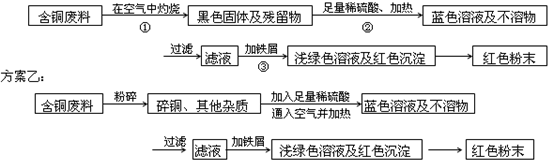
方案乙:
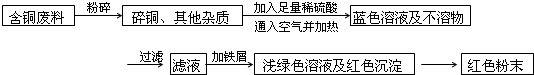
(1)两个方案哪个符合当前的绿色理念:______;
(2)写出方案甲中步骤②、③反应的离子方程式:______、______;
(3)无论是甲还是乙方案,在“加铁屑”时,都加入稍过量的铁屑,你认为这么做的道理是:______;
(4)①用简便的方法检验红色粉末中含有过量的铁屑:______;②如何除去红色粉末中所含过量的Fe得干燥的红色粉末:______.
-
某同学拟定了以下实验方案,来确定一批合金废料的成分并加以回收利用。
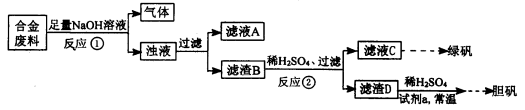
请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和____(填化学式)。
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为____;滤渣D、稀硫酸和试剂a总反应的化学方程式为________。
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加________。
Na2SiO3溶液与过量的CO2反应的离子方程式为。
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,标况) | 1.12 | 2.24 | 3.36 | 4.48 |
①实验①最先溶解的金属发生反应的化学方程式是。
②滤渣B中Fe的质量分数为____%(精确到0.1%)。
-
某同学拟定了以下实验方案,来确定一批合金废料的成分并加以回收利用.
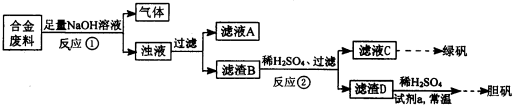
请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe和______(填化学式).
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为______;滤渣D、稀硫酸和试剂a总反应的化学方程式为______.
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na2SiO3的方法是:取少量滤液A于试管中,滴加______.
Na2SiO3溶液与过量的CO2反应的离子方程式为______.
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | | |
| NO体积(L,体积) | 1.12 | 2.24 | 3.36 | 4.48 |
①实验①最先溶解的金属发生反应的化学方程式是______.
②滤渣B中Fe的质量分数为______%(精确到0.1%).
-
工业废料和废水的处理离不开化学。
I. 某工业废料含SiO2、FeS和CuS等物质,采用如下实验方案进行回收利用。请回答下列问题:

(1)已知步骤①中发生的化学反应为非氧化还原反应,写出产生气体的电子式_______,该气体可用足量的NaOH溶液吸收,该反应的离子方程式是_______________________________
(2)Si 原子在周期表中的位置____________,写出晶体Si的一种主要用途___________。步骤②的操作依次为____________________、过滤、洗涤、干燥。滤渣2的主要成分是SiO2和S ,写出步骤③涉及的化学方程式_________________________________。
II.用一种阴、阳离子双隔膜三室电解槽处理含镍酸性废水并获得金属镍的模拟装置如图。
镍棒与外接电源____极相连。A极区电极反应式是__________________________。 电解一段时间后,B中NaCl溶液的浓度_________填“增大”、“减少”);若将图中阳离子膜去掉,将A、B两室合并,则A极区电极产物是________。

-
[2012·德州一模](12分)有色金属冶炼厂剩下的废料中,含有金、银、铂、钯等贵重金属,为提高经济效益,某科技小组要从废料中提取金、银、铂、钯等贵重金属,步骤设计如下图甲,试回答下列问题:
(1)实验步骤中,浓硫酸浸煮产生尾气的主要成分是________(填化学式),常用足量NaOH溶液进行尾气处理,发生反应的离子方程式为。
(2)在实验室中操作I中需要的玻璃仪器有________。
(3)实验过程中所需的氯气在制备中,会混有杂质(H2O和HCl),科技小组设计了图乙所示的实验装置,证明水蒸气和HCl杂质的存在,请根据设计示意图完成下列有关问题:
①A是氯气发生装置,其中发生的离子方程式为________。
②实验装置的接口顺序为:b接________,________接________,________接a。
③装置D的作用是________。
④在实验中,一组员认为该实验设计存在缺陷:不能证明最终通入AgNO3溶液的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,他们提出在某两个装置之间再加装置E。如右图所示。你认为装置E应加在________之间(填装置字母序号),并且在广口瓶中放入________(填写所有试剂或用品名称)。













