铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,高铁酸盐在碱性环境中比酸性环境中相对稳定。工业上用湿法制备高铁酸钾的基本流程如下图所示:
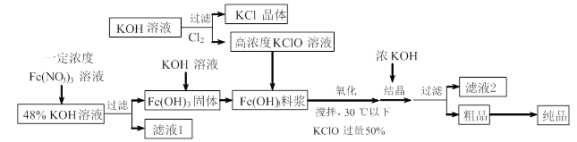
下列有关说法不正确的是
A.控制反应温度30℃以下的原因是防止生成的K2FeO4发生分解
B.结晶过程中加入浓KOH溶液其作用是增大K+浓度,促进K2FeO4晶体析出
C.滤液2中阳离子可通过焰色反应检验确定
D.湿法制备高铁酸钾,也可以在Fe(OH)3料浆中直接通入足量氯气
高三化学选择题困难题
铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,高铁酸盐在碱性环境中比酸性环境中相对稳定。工业上用湿法制备高铁酸钾的基本流程如下图所示:

下列有关说法不正确的是
A.控制反应温度30℃以下的原因是防止生成的K2FeO4发生分解
B.结晶过程中加入浓KOH溶液其作用是增大K+浓度,促进K2FeO4晶体析出
C.滤液2中阳离子可通过焰色反应检验确定
D.湿法制备高铁酸钾,也可以在Fe(OH)3料浆中直接通入足量氯气
高三化学选择题困难题
铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,高铁酸盐在碱性环境中比酸性环境中相对稳定。工业上用湿法制备高铁酸钾的基本流程如下图所示:

下列有关说法不正确的是
A.控制反应温度30℃以下的原因是防止生成的K2FeO4发生分解
B.结晶过程中加入浓KOH溶液其作用是增大K+浓度,促进K2FeO4晶体析出
C.滤液2中阳离子可通过焰色反应检验确定
D.湿法制备高铁酸钾,也可以在Fe(OH)3料浆中直接通入足量氯气
高三化学选择题困难题查看答案及解析
高铁酸钾()是一种新型、高效、多功能水处理剂,且不会造成二次污染。
查阅资料:
①为紫色固体,微溶于
溶液,具有强氧化性,在酸性或中性溶液中快速产生
,在碱性溶液中较稳定。
②与
溶液在20℃以下反应生成
,在较高温度下则生成
。
(1)实验室常利用氯气制备后与
、
反应制备
。根据下列仪器,请你组装合理、简洁的实验装置,所用装置的接口连接顺序是________。
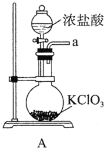
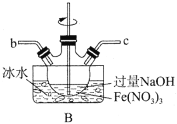
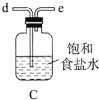
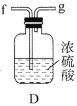
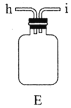
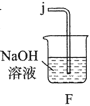
(2)写出装置A中发生反应的离子方程式________。
(3)三颈烧瓶用冰水浴的原因是________,A处盛放的仪器名称是________。
(4)将实验得到的再加入饱和
溶液中,可析出紫黑色的
粗晶体,其原因是________。
(5)用滴定法测定所制粗的纯度(杂质与
不反应):取
粗
样品,加入足量硫酸酸化的
溶液,充分反应后,用
标准溶液滴定生成的I2,滴定消耗标准溶液的体积为
。涉及的反应有:
,
。
①滴定时选用的指示剂是________,滴定终点的现象是________。
②制得粗的纯度是________。
高三化学实验题中等难度题查看答案及解析
(14分)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:

(1)在农业生产中,滤液1可用作▲ 。
(2)上述氧化过程中,发生反应的离子方程式是:▲ ,控制反应温度30℃以下的原因是:▲ 。
(3)结晶过程中加入浓KOH溶液的作用是:▲ 。
(4)某温度下,将Cl2通入KOH溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为▲ 。
(5)实验测得铁盐溶液的质量分数、反应时间与K2FeO4产率的实验数据分别如图1、图2所示。为了获取更多的高铁酸钾,铁盐的质量分数应控制在▲ 附近、反应时间应控制在▲ 。
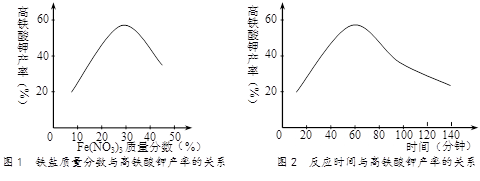
高三化学实验题中等难度题查看答案及解析
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,容易分解,工业上制备高铁酸钾的基本流程如下图所示:
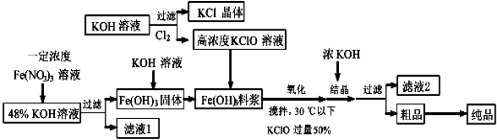
(1)K2FeO4中铁化合价为 在农业生产中,滤液1可用作。
(2)氧化过程中搅拌目的是 由粗品到纯品的实验方法是
(3)上述Fe(OH)3浆料中加入KClO溶液进行氧化过程中,发生反应的离子方程式是:,控制反应温度30℃ 以下的原因是: 。
(4)结晶过程中加入浓KOH溶液的作用是: 。
(5)某温度下,将Cl2通入KOH溶液中,反应后得到KCl、KClO、KClO3的混合液,经测定ClO-与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 。
高三化学实验题困难题查看答案及解析
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。K2FeO4为紫色固体,微溶于KOH溶液。K2FeO4具有强氧化性,在酸性或中性溶液中迅速产生O2,在碱性溶液中较稳定。某学习小组设计了下面的实验制备K2FeO2并探究其性质。
(一)K2FeO4的制备
该小组用下图所示装置制备K2FeO4(夹持装置略)。
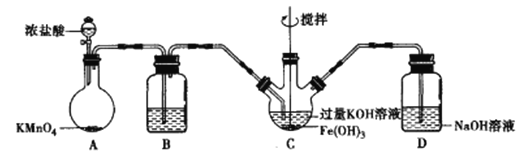
(1)以上装置图中有一处明显的错误请你帮助指出来:___________。B中应盛装的试剂是___________。
(2)写出A中发生反应的离子方程式:___________。
(3)C中发生的反应有Cl2+2OH-=Cl-+ClO-+H2O,还有生成K2FeO4的反应。写出得到紫色固体K2FeO4的化学方程式:___________。
(二)性质探究
用KOH溶液充分洗涤C中所得固体得到固体物质K2FeO4。
(4)絮凝实验:甲同学取少量K2FeO4加入浑浊的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清。请结合方程式,说明K2FeO2的净水原理:___________。
(5)乙同学取少量K2FeO4,向其中滴入稀盐酸发现产生黄绿色气体。产生黄绿色气体的原因可能是____。
(6)丙同学取少量K2FeO4,向其中滴入MnSO4和适量H2SO4的混合溶液,振荡后溶液呈紫色,丙同学认为氧化性FeO42->MnO4-。请你设计一个实验,验证丙同学的结论是否正确:___________。
高三化学实验题中等难度题查看答案及解析
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。K2FeO4为紫色固体,微溶于KOH溶液。K2FeO4具有强氧化性,在酸性或中性溶液中迅速产生O2,在碱性溶液中较稳定。某学习小组设计了下面的实验制备K2FeO2并探究其性质。
Ⅰ.K2FeO4的制备
该小组用如图所示装置制备K2FeO4(夹持装置略)。
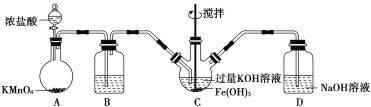
(1)以上装置图中有一处明显的错误请你帮助指出来:___________。B中应盛装的试剂是___________。
(2)写出A中发生反应的离子方程式__________________________________。
(3)C中发生的反应有Cl2+2OH-===Cl-+ClO-+H2O,还有生成K2FeO4的反应。写出得到紫色固体K2FeO4的化学方程式为____________。
Ⅱ.性质探究
用KOH溶液充分洗涤C中所得固体得到固体物质K2FeO4。
(4)絮凝实验:甲同学取少量K2FeO4加入浑浊的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清。请结合方程式,说明K2FeO4的净水原理:_________________。
(5)乙同学取少量K2FeO4,向其中滴入稀盐酸发现产生黄绿色气体。产生黄绿色气体的原因可能是___。
(6)丙同学取少量K2FeO4,向其中滴入MnSO4和适量H2SO4的混合溶液,振荡后溶液呈紫色,丙同学认为氧化性FeO42->MnO4-。请你设计一个实验,验证丙同学的结论是否正确:_____________
高三化学实验题中等难度题查看答案及解析
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,不会造成二次污染。
己知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
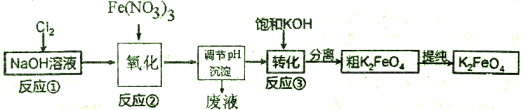
(1)①上述氧化过程中,发生反应的离子方程式是__________,在实际生产中一般控制反应温度30℃以下,其原因是__________。
②沉淀过程中加入浓KOH溶液可析出高铁酸钾(K2FeO4 ),这说明__________。
③在提纯K2FeO4中采用重结晶、洗涤、低温烘干的方法,沉淀洗涤方法是__________。
④某温度下,将C12通入NaOH溶液中,反应后得到NaCl,NaC1O,NaClO3的混合溶液,经测定ClO-与C1O3-离子的物质的量之比是1: 2,则C12与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为__________。
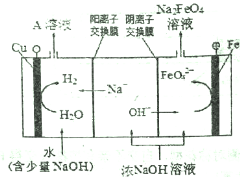
(2)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应式为__________,其中可循环使用的物质是__________。
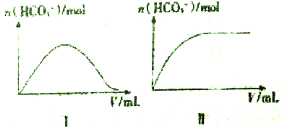
(3)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.己知:25℃时,几种酸的电离平衡常数如下表所示。

25℃时,向一定浓度的Na2CO3溶液中分别滴入等物质的量浓度的下列溶液至过量:
①NaHSO3②HNO3③HC1O,溶液中的n (HCO3-)与所加入溶液体积(V)的关系如上图所示。其中符合曲线Ⅱ的溶液为__________。
高三化学实验题简单题查看答案及解析
高铁酸钾(K2FeO4,暗紫色固体),是一种新型、高效、多功能的水处理剂。完成下列填空:
(1)K2FeO4溶于水得到浅紫红色的溶液,且易水解,生成氧气和氢氧化铁。写出该水解反应的离子方程式_________;说明高铁酸钾做水处理剂的原理______。
(2)下图分别是1mol/L的K2FeO4溶液在不同pH和温度下c(FeO42-)随时间的变化曲线。
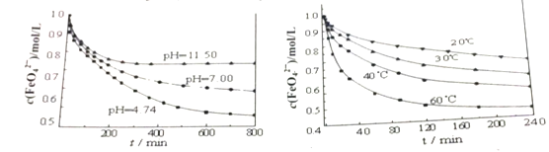
根据以上两图,说明配制K2FeO4溶液的注意事项______________。
高三化学填空题中等难度题查看答案及解析
高铁酸钾是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通入氯气,然后再加入Fe(NO3)3溶液的方法制备K2FeO4,发生反应:
①Cl2+KOH→KCl+KClO+KClO3+H2O(未配平);
②2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O。
下列说法正确的是
A.反应①中每消耗4 mol KOH,吸收标准状况下44.8L Cl2
B.氧化性:K2FeO4> KClO
C.若反应①中n(ClO-)∶n(ClO3-)=5∶1,则氧化剂与还原剂的物质的量之比为2:1
D.若反应①的氧化产物只有KClO,则得到0.2mol K2FeO4时消耗0.3mol Cl2
高三化学多选题中等难度题查看答案及解析
(题文)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂。
(1)工业上的湿法制备方法是用KClO 与Fe(OH)3在KOH 存在下制得K2FeO4,该反应氧化剂与还原剂物质的量之比为_____________。
(2)实验室用食盐、废铁屑、硫酸、KOH等为原料,通过以下过程制备K2FeO4:
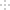
①操作(Ⅰ)的方法为在隔绝空气条件下________、________、过滤、洗涤、隔绝空气减压干燥。
②写出产生X气体的化学方程式_______________________________________。
(3)测定某K2FeO4样品的质量分数,实验步骤如下:
步骤1:准确称量1.0g样品,配制100mL溶液;
步骤2:准确量取25.00mL K2FeO4溶液加入到锥形瓶中;
步骤3:在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-;
步骤4:加稀硫酸,使CrO42-转化为Cr2O72-,CrO2-转化为Cr3+,Fe(OH)3转化为Fe3+;
步骤5:加入二苯胺磺酸钠作指示剂,用0.1000mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显紫红色),记下消耗(NH4)2Fe(SO4)溶液的体积,做3次平行实验,平均消耗30.00mL的(NH4)2Fe(SO4)2溶液。
已知:K2Cr2O7水溶液显黄色,滴定时发生的反应为:6Fe2++Cr2O72-+14H+==6Fe3++2Cr3++7H2O。
①步骤2中准确量取25.00mLK2FeO4溶液加入到锥形瓶中所用的仪器是________。
②写出步骤3中发生反应的例子方程式___________________________________。
③根据上述实验数据,测定该样品中K2FeO4的质量分数为___________。(K2FeO4摩尔质量为198g/mol)。
高三化学综合题中等难度题查看答案及解析