-
下列各溶液中微粒的物质的量浓度关系错误的是( )
A.0.2mol/LK2CO3溶液中c(OH-)=c(HCO-3)+c(H+)+2c(H2CO3)
B.0.1mol/LNaHA溶液中其中pH=3,c(HA-)>c(H+)>c(H2A)>c(A2-)
C.向Na2SO4溶液中滴加稀HNO2得到pH=4的混合溶液c(Na+)=2c(SO2-4)
D.pH=a的HA溶液与pH=b的MOH溶液任意比混合c(H+)+c(M+)=c(OH-)+c(A-)高三化学选择题中等难度题查看答案及解析
-
下列选项中,微粒的物质的量浓度关系正确的是( )
A.向硝酸钾溶液中滴加稀盐酸得到pH=4的混合溶液:c(K+)=c(NO3-)
B.1.0mol/LK2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
C.浓度均为0.1mol/L的小苏打溶液和氢氧化钠溶液等体积混合:c(Na+)+c(H+)=c(CO32-)+c(OH-)+c(HCO3-)
D.向氯化铵溶液中加入一定量氨水得到碱性混合溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+)高三化学选择题中等难度题查看答案及解析
-
下列各溶液中微粒的物质的量浓度关系错误的是( )
A.0.2mol/L K2CO3溶液中c(OH-)=c(HCO-3)+c(H+)+2c(H2CO3)
B.0.1mol/L NaHA溶液中其中pH=3,c(HA-)>c(H+)>c(H2A)>c(A2-)
C.向Na2SO4溶液中滴加稀CH3COOH得到pH=4的混合溶液c(Na+)=2c(SO2-4)
D.pH=a的HA溶液与pH=b的MOH溶液任意比混合c(H+)+c(M+)=c(OH-)+c(A-)
高三化学选择题简单题查看答案及解析
-
下列有关溶液中微粒的物质的量浓度关系正确的是
A. 在0.1mol/LNa2CO3溶液中:c(OH-)-c(H+)= c(HCO3-)+2c(H2CO3)
B. 向0.2 mol/LNaHCO3溶液中加入等体积0.1mol/LNaOH溶液:c(CO32-) >c(HCO3-) >c(OH-)>c(H+)
C. 常温下,pH=7的NH4Cl和NH3·H2O的混合溶液中: c(Cl-)>c(NH4+)>c(OH-)=c(H+)
D. 0.10mol/LCH3COONa 溶液中通入HCl气体至 pH = 7:c(Na+) >c(Cl-)=c(CH3COOH)
高三化学选择题困难题查看答案及解析
-
下列溶液中各微粒的浓度关系正确的是
A. 0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+ c(H2CO3)
B. pH 相等的NaF 与CH3COOK 溶液:[c(Na+)-c(F-)]>[c(K+)-c(CH3COO-)]
C. pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4 溶液,NH4+大小顺序为①=②>③
D. 0.2 mol·L-1HCl与0.1 mol·L-1NaAlO2 溶液等体积混合:c(Cl-)>c(Na+)>c(H+)>c(Al3+)>c(OH-)
【答案】C
【解析】根据质子守恒,0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+ 2c(H2CO3),故A错误;根据电荷守恒,NaF 溶液中[c(Na+)-c(F-)]= [c(OH-)-c(H+)],CH3COOK 溶液[c(K+)-c(CH3COO-)]= [c(OH-)-c(H+)],PH相等,所以[c(Na+)-c(F-)]=[c(K+)-c(CH3COO-)],故B错误; NH4Cl 、(NH4)2SO4由于NH4+水解溶液呈酸性,pH相等,所以NH4+浓度相等,NH4HSO4 溶液主要由于NH4HSO4电离呈酸性,所以NH4HSO4 溶液中NH4+浓度最小,故C正确;0.2 mol·L-1HCl与0.1 mol·L-1NaAlO2 溶液等体积混,完全反应生成氯化钠、氯化铝、氢氧化铝,所以c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-),故D错误。
【题型】单选题
【结束】
8直接排放含SO2的烟气会形成酸雨,危害环境。某化学兴趣小组进行如下有关SO2性质和含量测定的探究活动。
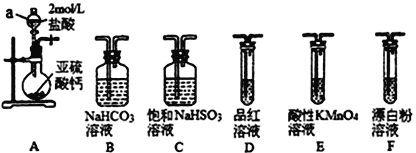
(1)装置A中仪器a的名称为________。写出A中发生反应的离子方程式_________________________。若利用装置A 中产生的气体证明+4价的硫元素具有氧化性,试用化学方程式表示该实验方案的反应原理_______________________________________。
(2)选用图中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是__________________________________。
②丙同学设计的合理实验方案为:按照A→C→______→F→尾气处理(填字母) 顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是____________________________。
③其中裝置C的作用是____________________________。
(3)为了测定装置A残液中SO2的含量,量取10.00mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00 mL0.0500 mol·L-1的KMnO4溶液吸收。充分反应后,再用0.2000 mol·L-1的KI标准溶液滴定过量的KMnO4,消耗KI溶液20.00mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+ 10I-+2MnO4-+16H+=2Mn2++5I2+8H2O
①残液中SO2的含量为____g·L-1。
②若滴定前读数时平视,滴定终点读数时俯视则测定结果________ (填“偏高”、“偏低”或“无影响”)。
高三化学实验题困难题查看答案及解析
-
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A. 0.1mol/L的Na2CO3溶液中:c(HCO3-)=2c(HCO3-)+c(H+)- c(OH-)
B. 物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中: c(HClO)+c(ClO-)=2c(HCO3-)+2c(CO32-)+2c(H2CO3)
C. 向3.0L0.1mol/LNaOH溶液中缓慢通入CO2至溶液增重8.8g时,溶液中: c(Na+)>c(CO32-)> c(HCO3-) >c(OH-)>c(H+)
D. 等物质的量的CH3COOH、CH3COONa混合溶液PH=4.75中:c(CH3COO-)+ c(OH-)>c(CH3COOH)+ c(H+)
高三化学选择题困难题查看答案及解析
-
下列溶液中微粒的物质的量浓度关系正确的是( )
A. 0.1mol/LNaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
B. 室温下,向0.01mol/LNH4HSO4溶液中滴加等体积0.01mol/LNaOH溶液:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
C. Na2CO3溶液:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)
D. 25℃时,浓度均为0.1mol/L的CH3COOH和CH3COONa等体积混合:c(CH3COOH)+c(CH3COO-)=0.2mol/L
高三化学选择题困难题查看答案及解析
-
下列溶液中各微粒的浓度关系不正确的是
A. 0.1mol·L-1NaHCO3溶液中: c(H+)=c(CO32-)+c(OH-)-c(HCO3-)
B. 等体积、等物质的量浓度的NaX和弱酸HX混合后呈酸性的溶液中:c(X-) >c(Na+)>c(HX)>c(H+)>c(OH-)
C. 将0.2 mol·L-1 NaA溶液和0.1 mol·L-1盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)+C(OH-)
D. 1.5 L 0.1 mol·L-1 NaOH溶液中缓慢通入CO2至溶液增重4.4 g时,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
高三化学多选题中等难度题查看答案及解析
-
下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1mol/LCH3COONa溶液:c(Na+)=c(CH3COO—)
B.0.1mol/L NaHCO3溶液:c(Na+)>c(HCO3—)>c(OH—)>c(H+)>c(CO32—)
C.由NH4Cl与NH3· H2O组成的碱性溶液:c(NH4+)>c(Cl—)>c(OH—)>c(H+)
D.向NaCl溶液中滴加盐酸得到pH=2的混合溶液:c(Na+)+c(H+)=c(Cl—)
高三化学选择题简单题查看答案及解析
-
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是
A.0.1mol·L-1NaHCO3溶液中的粒子浓度:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)>c(OH-)>c(H+)
B.将标况下2.24L的CO2通入150mL 1mol·L-1NaOH溶液中充分反应后的溶液:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3)
C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合溶液的pH等于7,则反应后的混合液:2c(R2-)+c(HR-)>c(Na+)
D.0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(OH-)+2c(A-)=c(H+)+2c(HA)
高三化学选择题极难题查看答案及解析