-
[化学-选修3:物质结构与性质]
氧族元素是指位于元素周期表第16列的元素,包括氧、硫、硒(Se)、碲(Te)、钋(Po)五种元素。
请回答下列问题:
(1)与氧同周期的相邻元素中,第一电离能由大到小的顺序为_______________。
(2)臭鼬排放的臭气主要成分为3-MBT(3-甲基-2-丁烯硫醇,结构如下图)。

1mol3-MBT中含有σ键数目为_______________(NA为阿伏伽德罗常数的值)。沸点:3-MBT____________(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是___________________。
(3)S有+4和+6两种价态的氧化物。
①下列关于气态SO3和SO2的说法中正确的是_____________(填选项字母)。
| A.中心原子的价层电子对数目相等 |
| B.都是极性分子 |
| C.中心原子的孤对电子数目相等 |
| D.都含有极性键 |
②SO3分子的空间构型为________,与其互为等电子体的阴离子为_____________(举一例)。将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图,此固态SO3中S原子的杂化轨道类型是_______。

(4)元素X与硒同周期,X元素原子核外未成对电子数最多,X为________(填元素符号),X的基态原子的电子排布式为_______。
(5)单质钋是由_____键形成的晶体;若已知Po的摩尔质量为Mg·mol-1,原子半径为r pm,阿伏伽德罗常数的值为NA,则钋晶体的密度的表达式为_________g/cm3
-
氧族元素是指位于元素周期表第16列的元素,包括氧、硫、硒(Se)、碲(Te)、钋(Po)、鉝(Lv)六种元素。请回答下列问题:
(1)O及与O同周期的相邻元素,第一电离能由大到小的顺序为_________。
(2)S有+4和+6两种价态的氧化物。
①下列关于气态SO3和SO2的说法中正确的是______ (填选项字母)。
A.中心原子的价层电子对数目相等 B.都是极性分子
C.中心原子的孤对电子数目相等 D.都含有极性键
②SO3分子的空间构型为_________,与其互为等电子体的阴离子为______(举一例)。将纯液态SO3冷却到289.8 K时凝固得到一种螺旋状单链结构的固体,其结构如图,此固态SO3中硫原子的杂化轨道类型是___。

(3)元素X与硒同周期,X元素原子核外未成对电子数最多,X为____(填元素符号),X的基态原子的电子排布式为_____。
(4)单质钋(Po)是简单立方堆积的金属晶体,若已知Po的摩尔质量为M g·mol-1,原子半径为r pm,阿伏伽德罗常数的值为NA,则钋晶体的密度的表达式为___g/cm3。
-
氧族元素是指位于元素周期表第16列的元素,包括氧、硫、硒(Se)、碲(Te)、钋(Po)五种元素。请回答下列问题:
(1)与氧同周期的相邻的元素中,第一电离能由大到小的顺序为________________。(填元素符号)
(2)气态SO3分子的空间构型为______________;与其互为等电子体的阴离子为___________(举一例)。
(3)将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如下图,此固态SO3中S原子的杂化轨道类型是_____________。
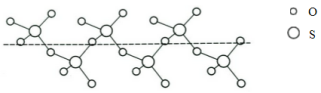
(4)元素X与硒同周期,X元素原子核外未成对电子数最多,X为_________(填元素符号);X的基态原子的电子排布式为___________________。
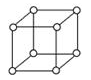
(5)单质钋是由___________键形成的晶体;有资料表明,只有钋的晶体中的原子具有如图所示的堆积方式,若已知Po的摩尔质量为M g·mol-1,原子半径为r pm,阿伏伽德罗常数的值为NA,则钋晶体的密度的表达式为____________g/cm3。
-
氧族元素是指位于元素周期表第16列的元素,包括氧、硫、硒(Se)、碲(Te)、钋(Po)五种元素。
请回答下列问题:
(1)①与氧同周期的相邻元素及氧的第一电离能由大到小的顺序为________________。
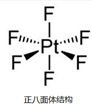
②已知:离子型配位化合物O2[PtF6]中铂元素为+ 5价,它可由反应PtF6+O2= O2[PtF6]制得,PtF6分子结构如图所示。PtF6分子中Pt的杂化轨道类型是否为sp3?答:_____(填“是”或“否”),其原因是_______。
(2)臭鼬排放的臭气主要成分为3-MBT(3-甲基-2-丁烯硫醇,结构简式为 )。1mol3-MBT中含有σ键数目为_______(NA为阿伏伽德罗常数的值)。沸点:3-MBT____(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是_______________________。
)。1mol3-MBT中含有σ键数目为_______(NA为阿伏伽德罗常数的值)。沸点:3-MBT____(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是_______________________。
(3)S有+4和+6两种价态的氧化物。
①下列关于气态SO3和SO2的说法中正确的是_____(填字母)。
A.中心原子的价层电子对数目相等
B.都是极性分子
C.中心原子的孤对电子数目相等
D.都含有极性键
②SO3子的空间构型为________,与其互为等电子体的阴离子为_____(举一例)。
(4)元素X与硒同周期,且该周期中X元素原子核外未成对电子数最多,则X为____基态原子的电子排布式为_______。
(5)单质钋是由_____键形成的晶体,其晶胞为简单立方;若已知Po的摩尔质量为Mg·mol-1,原子半径为rpm,阿伏伽德罗常数的值为NA,则钋晶体的密度的表达式为_____g·cm-3(只列表达式)。
-
氧族元素是指位于元素周期表第16列的元素,包括氧、硫、硒(Se)、碲(Te)、钋(Po)五种元素。
请回答下列问题:
(1)①与氧同周期的相邻元素及氧的第一电离能由大到小的顺序为________________。
②已知:离子型配位化合物O2[PtF6]中铂元素为+ 5价,它可由反应PtF6+O2= O2[PtF6]制得,PtF6分子结构如图所示。PtF6分子中Pt的杂化轨道类型是否为sp3?答:_____(填“是”或“否”),其原因是_______。

(2)臭鼬排放的臭气主要成分为3-MBT(3-甲基-2-丁烯硫醇,结构简式为 )。1mol3-MBT中含有σ键数目为_______(NA为阿伏伽德罗常数的值)。沸点:3-MBT____(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是_______________________。
)。1mol3-MBT中含有σ键数目为_______(NA为阿伏伽德罗常数的值)。沸点:3-MBT____(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是_______________________。
(3)S有+4和+6两种价态的氧化物。
①下列关于气态SO3和SO2的说法中正确的是_____(填字母)。
A.中心原子的价层电子对数目相等
B.都是极性分子
C.中心原子的孤对电子数目相等
D.都含有极性键
②SO3子的空间构型为________,与其互为等电子体的阴离子为_____(举一例)。
(4)元素X与硒同周期,且该周期中X元素原子核外未成对电子数最多,则X为____基态原子的电子排布式为_______。
(5)单质钋是由_____键形成的晶体,其晶胞为简单立方;若已知Po的摩尔质量为Mg·mol-1,原子半径为rpm,阿伏伽德罗常数的值为NA,则钋晶体的密度的表达式为_____g·cm-3(只列表达式)。
-
氧、硫、硒(Se)、碲(Te)、钋(Po)是元素周期表中原子序数依次增大的同主族元素。回答下列问题:
(1)硒在元素周期表中的位置________。
(2) Po的中子数为________。
Po的中子数为________。
(3)某温度时,该族单质与H2反应生成气态H2X的热化学方程式如下:
O2(g)+2H2(g)=2H2O(g) △H1=-484 kJ/mol
S(g)+H2(g) H2S(g) △H2=-20 kJ/mol
H2S(g) △H2=-20 kJ/mol
Se(g)+H2(g) H2Se(g) △H3=+81kJ/mol
H2Se(g) △H3=+81kJ/mol
①硫和硒氢化物的热稳定性:H2S________ H2Se(填“>”、“=”或“<”);判断依据是________。
②写出O2(g)与H2S(g)反应生成H2O(g)和S(g)的热化学方程式________。
-
已知O、S、Se、Te、Po、Lv是同主族元素,其原子序数依次增大。回答下列问题:
(1)Lv在周期表中的位置是_________。
(2)下列有关性质的比较,能用元素周期律解释的是_________。
a.离子半径:Te2->Se2- b.热稳定性:H2O>H2S
c.熔、沸点:H2O>H2S d.酸性:H2SO4>H2SeO4
(3)从原子结构角度解释Se与S的最高价氧化物对应的水化物酸性不同的原因_________。
(4)实验室用如下方法制备H2S并进行性质验证。
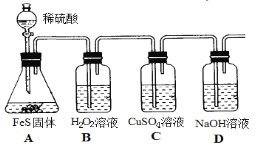
①设计B装置的目的是证明_________,B中实验现象为_______________。
②实验中经检测发现C中溶液pH降低且出现黑色沉淀。C中反应的离子方程式是_______________。
③有同学根据“强酸制弱酸”原理认为装置A、C中两个反应相矛盾,认为C中不可能出现上述现象。该观点不正确的理由是_______________。
-
下图是元素周期表的一部分:
| C | N | O | F | |
| Si | P | S | Cl | |
| Ge | As | Se | Br | |
| Sn | Sb | Te | I | |
| Pb | Bi | Po | At | |
 阴影部分元素的外围电子排布式的通式为____。Sb的元素名称为____。基态P原子中,电子占据的最高能级符号为____,该能层具有的原子轨道数为____。
阴影部分元素的外围电子排布式的通式为____。Sb的元素名称为____。基态P原子中,电子占据的最高能级符号为____,该能层具有的原子轨道数为____。
 氮族元素氢化物
氮族元素氢化物 、
、 、
、 的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物
的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物 性质可能有____。
性质可能有____。

A.稳定性
B.沸点
C. 键能
键能
D.分子间作用力
 某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____种。
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有____种。

 和
和 、
、 及
及 能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元
能形成一种蓝色配位化合物普鲁士蓝。如图是该物质的结构单元 未标出
未标出 ,该图是普鲁士蓝的晶胞吗?____
,该图是普鲁士蓝的晶胞吗?____ 填“是”或“不是”
填“是”或“不是” ,平均每个结构单元中含有____个
,平均每个结构单元中含有____个 。
。

 磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是
磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是 四面体,多磷酸盐中是
四面体,多磷酸盐中是 四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____。
四面体。下图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为____。

-
氧、硫、硒、碲都位于元素周期表的VIA族,其化合物在化工生产中有广泛应用。
(1)下列性质的递变顺序不正确的是_____(填字母)。
A.酸性:H2SeO4>H2SeO3 B.非金属性:O>S>Se>Te
C.还原性:H2Te>H2Se>H2S>H2O D.热稳定性:H2O>H2Te>H2Se>H2S
E.沸点: H2Te>H2Se>H2S>H2O
(2)在常温下进行的置换反应X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的单质,W、V是化合物。
①若W是水,且作还原剂,反应的化学方程式为_________。
②若V是水,为还原产物,反应的化学方程式为_____________。
(3) ①一定温度下,向恒容密闭容器中充入一定量的H2S,发生反应H2S(g) S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是_______(填字母)。
S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是_______(填字母)。
A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.  不再变化 D.H2S与H2的消耗速率相等
不再变化 D.H2S与H2的消耗速率相等
②已知:液态CS2完全燃烧生成CO2、SO2气体,每转移3mol电子时放出269.2kJ热量。写出表示CS2(1)的燃烧热的热化学方程式:______________。
(4) ①工业上,用S02还原TeC14溶液制备碲(Te),反应中氧化产物与还原产物的物质的量之比为____________。
②以石墨为电极,电解强碱性Na2TeO3溶液也可获得碲,电解过程中阴极的电极反应式为_____;阳极产生的气体是_____ (填化学式)。
-
氧、硫、硒、碲都位于元素周期表的VIA族,其化合物在化工生产中有广泛应用。
(1)下列性质的递变顺序不正确的是_____(填字母)。
A.酸性:H2SeO4>H2SeO3 B.非金属性:O>S>Se>Te
C.还原性:H2Te>H2Se>H2S>H2O D.热稳定性:H2O>H2Te>H2Se>H2S
E.沸点: H2Te>H2Se>H2S>H2O
(2)在常温下进行的置换反应X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的单质,W、V是化合物。
①若W是水,且作还原剂,反应的化学方程式为_________。
②若V是水,为还原产物,反应的化学方程式为_____________。
(3) ①一定温度下,向恒容密闭容器中充入一定量的H2S,发生反应H2S(g) S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是_______(填字母)。
S2(g)+2H2(g)。下列情况中,可判断该反应达到平衡状态的是_______(填字母)。
A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.  不再变化 D.H2S与H2的消耗速率相等
不再变化 D.H2S与H2的消耗速率相等
②已知:液态CS2完全燃烧生成CO2、SO2气体,每转移3mol电子时放出269.2kJ热量。写出表示CS2(1)的燃烧热的热化学方程式:______________。
(4) ①工业上,用S02还原TeC14溶液制备碲(Te),反应中氧化产物与还原产物的物质的量之比为____________。
②以石墨为电极,电解强碱性Na2TeO3溶液也可获得碲,电解过程中阴极的电极反应式为_____;阳极产生的气体是_____ (填化学式)。

)。1mol3-MBT中含有σ键数目为_______(NA为阿伏伽德罗常数的值)。沸点:3-MBT____(CH3)2C=CHCH2OH(填“高于”或“低于”),主要原因是_______________________。









