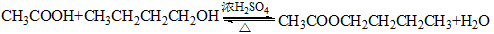-
有机物的反应往往伴随副反应发生,因此 需要分离提纯。有一种水果香精的合成步骤如下:
Ⅰ合成:
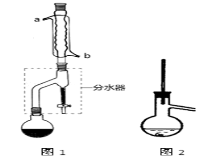
在干燥的圆底烧瓶中加入11.5 mL(9.3 g,0.125 mol)正丁醇、7.2 mL(7.5 g,0.125 mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00 mL水,其水面低于分水器回流支管下沿3~5 mm,然后用小火加热,反应大约40 min。
Ⅱ分离提纯:
① 将烧瓶中反应后的混合物冷却后与分水器中的酯层合并,转入分液漏斗,依次用10 mL水、10 mL 10% 碳酸钠溶液洗至中性,充分振荡后静置,分去水层。
② 将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥。
③ 将乙酸正丁酯粗产品转入50 mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。
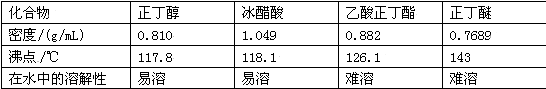
主要试剂及产物的物理常数如下:
制备过程中还可能有的副反应:
2CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
(1)合成和分离过程中均使用沸石,其作用________________________ 。
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从______(填a或b)管口通入。
(3)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先_______(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中,如果蒸馏装置如图2所示,则收集到的产品中可能混有___________杂质。
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃)
C.沙子 D.石蜡油(沸点200~300℃)
(5)如何根据装置中的实验现象判断该合成反应达到了终点_______________ 。
(6)反应结束后,若放出的水为6.98 mL(水的 密度为1g/mL),则正丁醇的利用率约为__________。
密度为1g/mL),则正丁醇的利用率约为__________。
-
有机物的反应往往伴随副反应发生,因此需要分离提纯。有一种水果香精的合成步骤如下:

Ⅰ合成:
在干燥的圆底烧瓶中加11.5mL(9.3g,0.125mol)正丁醇、7.2mL(7.5g,0.125mol)冰醋酸(乙酸)和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00mL水,其水面低于分水器回流支管下沿3~5mm,然后用小火加热,反应大约40min。
Ⅱ分离提纯:
①当分水器中的液面不再升高时,冷却,放出分水器中的水,把反应后的溶液与分水器中的酯层合并,转入分液漏斗中,用10mL10%碳酸钠溶液洗至酯层无酸性(pH=7),充分振荡后静置,分去水层。
②将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥(生成MgSO4•7H2O晶体)
③将乙酸正丁酯粗产品转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品,主要试剂及产物的物理常数如下:
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/(g/mL) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
制备过程中还可能与的副反应有2CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
根据以上信息回答下列问题:
(1)写出合成乙酸正丁酯的化学方程式____________。
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从______(填a或b)管口通入。
(3)步骤①中碳酸钠溶液的作用主要是除去硫酸、_________、___________。
(4)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先___________(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中,如果蒸馏装置如图2所示,则收集到的产品中可能混有___________________杂质。
(5)步骤③的常压蒸馏,需控制一定的温度,你认为在_______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃) C.石蜡油(沸点200~300℃) D.沙子
(6)反应结束后,若放出的水为6.98mL(水的密度为1g/mL),则正丁醇的转化率约为_______。
-
有一种水果香精乙酸正丁酯的合成提纯步骤如下:
(1)合成:在干燥的圆底烧瓶中加11.5mL(9.3g,0.125mol)正丁醇 、3~4滴浓H2SO4、7.2mL(7.5g,0.125mol)冰醋酸,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器(分离出生成的水)中预先加入5.00mL水,其水面低于分水器回流支管下沿3~5mm,然后用小火加热,反应大约40min。
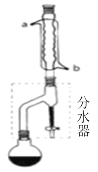
(2)分离提纯:
① 当分水器中的液面不再升高时,冷却,从分水器下端放出分水器中的水,把反应后的烧瓶中的溶液与分水器中的酯层合并,转入分液漏斗中,用10mL10%碳酸钠溶液洗至酯层无酸性(pH=7),充分震荡后静置,分去水层。
② 将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥(生成MgSO4•7H2O晶体)。
③ 将乙酸正丁酯粗产品转入50mL图中的仪器中,加几粒沸石进行加热,收集产品,主要试剂及产物的物理常数如下:
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/(g/mL) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
制备过程中还可能存在的副反应有:2CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O。根据以上信息回答下列问题:
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O。根据以上信息回答下列问题:
(1)写出合成乙酸正丁酯的化学方程式_________。
(2)步骤①中碳酸钠溶液的作用主要是___________,若改用NaOH溶液洗涤酯层,收集到的产物比预期少,原因是:_____________。
(3)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先___________(填实验操作名称),步骤③中加热分离有机物的实验方法名称是______________。
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃) C.沙子 D.石蜡油(沸点200~300℃)
(5)反应结束后,若放出的水为6.98mL(水的密度为1g/mL),则正丁醇的转化率约为:______________。
-
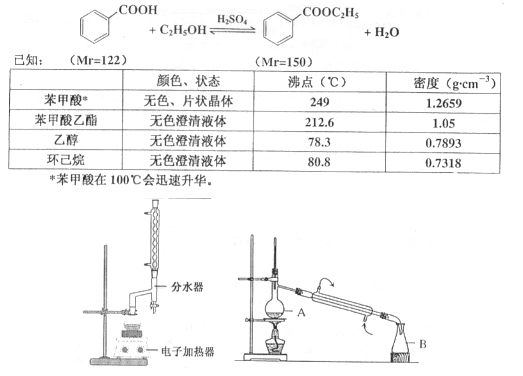
(10分)苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
实验步骤如下:
①在100 mL圆底烧瓶中加入12.20 g苯甲酸、25mL乙醇(过量)、20mL环己烷,以及4mL浓硫酸,混合均匀并加入沸石,按左上图所示装好仪器,控制温度在65~70℃加热回流2h。反应时环己烷-乙醇-水会形成“共沸物”(沸点62.6℃)蒸馏出来。再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并有机层。加入氯化钙,对粗产品进行蒸馏(装置如图所示)。低温蒸出乙醚后,继续升温,接收210~213℃的馏分。
⑤检验合格,测得产品体积为12.86mL.
回答下列问题:
⑴步骤①中使用分水器不断分离除去水的目的是________。
⑵步骤②中应控制馏分的温度在________。
A.65~70℃ B. 78~80℃ C. 85~90℃ D. 215~220℃
⑶若Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是________。
⑷蒸馏装置图中仪器A的名称是________,在步骤④中加入氯化钙的作用是________。
⑸该实验产品的产率为________。
-
苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
已知: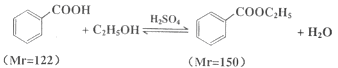
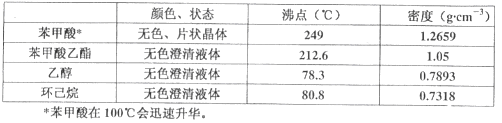
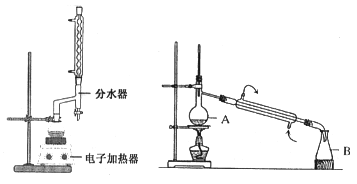
实验步骤如下:①在100 mL圆底烧瓶中加入12.20 g苯甲酸、25mL乙醇(过量)、20mL环己烷,以及4mL浓硫酸,混合均匀并加入沸石,按左上图所示装好仪器,控制温度在65~70℃加热回流2h。反应时环己烷-乙醇-水会形成“共沸物”(沸点62.6℃)蒸馏出来。再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并有机层。加入氯化钙,对粗产品进行蒸馏(装置如图所示)。低温蒸出乙醚后继续升温,接收210~213℃的馏分。
⑤检验合格,测得产品体积为12.86mL.
(1)步骤①中使用分水器不断分离除去水的目的是_________________。
(2)步骤②中应控制馏分的温度在___________________。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(3)步骤③中若Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是_____________。
(4)步骤④中分液操作叙述正确的是__________。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞。将分液漏斗倒转用力振摇
B.振摇几次后需打开分液漏斗下口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.分液操作时,分液漏斗中的下层液体由下口放出,然后再将上层液体由下口放出
蒸馏装置图中仪器A的名称是___________,在步骤④中加入氯化钙的作用是_________。
(5)该实验产品的产率为____________。
【答案】 有利于平衡不断向正方向移动,提高苯甲酸乙酯产率 C 苯甲酸乙酯中混有苯甲酸,在受热至100℃时发生升华 AB 蒸馏烧瓶 吸水剂 90.02%
【解析】试题分析:本题考查苯甲酸乙酯的制备。
(1)反应 +CH3CH2OH
+CH3CH2OH
 +H2O为可逆反应,使用分水器不断分离除去水,减小生成物浓度,有利于平衡不断向正反应方向移动,提高苯甲酸乙酯的产率。
+H2O为可逆反应,使用分水器不断分离除去水,减小生成物浓度,有利于平衡不断向正反应方向移动,提高苯甲酸乙酯的产率。
(2)根据题意,反应时环己烷-乙醇-水会形成“共沸物”蒸馏出来。烧瓶内的苯甲酸乙酯中混有乙醇、环己烷、苯甲酸和硫酸,步骤②继续加热蒸出苯甲酸乙酯中的乙醇、环己烷,乙醇的沸点为78.3℃,环己烷的沸点为80.8℃,苯甲酸乙酯的沸点为212.6℃,所以步骤②应控制馏分的温度在85~90℃,答案选C。
(3)步骤③中加入Na2CO3除去苯甲酸乙酯中混有的苯甲酸和硫酸,若Na2CO3加入不足,苯甲酸没有完全除去,步骤④蒸馏时蒸馏烧瓶中可见白烟的原因是:苯甲酸乙酯中混有苯甲酸,苯甲酸在受热至100℃时发生升华。
(4)A,为了使乙醚和水溶液充分接触,水溶液中加入乙醚转移至分液漏斗中后,需塞上玻璃塞,将分液漏斗倒转用力振摇,A项正确;B,为防止分液漏斗中气压过大将玻璃塞弹出,振摇几次后需打开分液漏斗下口的玻璃塞放气,B项正确;C,经几次振摇并放气后,需将分液漏斗置于铁架台上静置、待液体分层,C项错误;D,分液操作时,分液漏斗中的下层液体由下口放出,然后将上层液体从上口倾倒出来,D项错误;答案选AB。蒸馏装置图中仪器A的名称是蒸馏烧瓶。在步骤④中加入CaCl2的作用是作为吸水剂,除去水。
(5)由于乙醇过量,以苯甲酸计算理论生成的苯甲酸乙酯, ~
~ ,n(苯甲酸乙酯)理论=n(苯甲酸)=
,n(苯甲酸乙酯)理论=n(苯甲酸)= =0.1mol,m(苯甲酸乙酯)理论=0.1mol
=0.1mol,m(苯甲酸乙酯)理论=0.1mol 150g/mol=15g,该实验产品的产率=
150g/mol=15g,该实验产品的产率= 100%=90.02%。
100%=90.02%。
【题型】实验题
【结束】
19
根据下列四种元素的第一至第四电离能数据(单位:kJ/mol),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
(1)在周期表中,最可能处于同一族的是___________
A.S和U B.S和T C.T和U D.R和T E.R和U
(2)T的氯化物的化学式为___________________
(3)如果U元素是短周期的元素,你估计它的第2次电离能飞跃数据将是第_____个。
(4)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是_________,其中元素_______的第一电离能反常高的原因是_____________。
-
实验室制备乙酸正丁酯的化学方程式
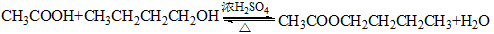
制备过程中还可能的副反应有

主要实验步骤如下:
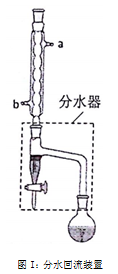
①在干燥的圆底烧瓶中加11.5mL正丁醇、7.2mL冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图1装置安装好分水器、冷凝管。然后小火加热。
②将烧瓶中反应后的混后物冷却与分水器中的酯层合并,转入分液漏斗,
③依次用10mL水,10mL 10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥。
④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。主要试剂及产物的物理常数:
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度(g·cm-3) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点(℃) | 118.0 | 118.1 | 126.1 | 142 |
根据以上信息回答下列问题。
(1)图Ⅰ装置中冷水应从 (填a或b),管口通入,反应混合物冷凝回流,通过分水器下端旋塞分出的生成物是 ,其目的是 。
(2)在步骤①④中都用到沸石防暴沸,下列关于沸石的说法正确的是 。
A.实验室沸石也可用碎瓷片等代替
B.如果忘加沸石,可速将沸石加至将近沸腾的液体中
C.当重新进行蒸馏时,用过的沸石可继续使用
D.沸石为多孔性物质,可使液体平稳地沸腾
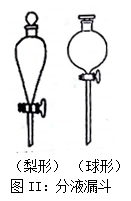
(3)在步骤③分液时,应选择图Ⅱ装置中 形分液漏斗,其原因是 。
(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去的杂质 。若改用氢氧化钠溶液是否可以 (填“可以”或“不可以”),其原因 。
(5)步骤④的常压蒸馏,需收集 ℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管 ,可能原因是 。
-
苯甲酸乙酯(C9H10O2)有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,其制备步骤如下:
①在100 mL烧瓶中加入12g苯甲酸;25 mL乙醇(过量)及4 mL浓硫酸和沸石,按如图所示的装置连接好。
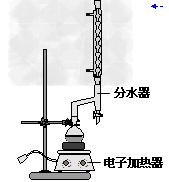
②检查装置的气密性。
 ③加热回流2 h,反应过程中即时打开旋塞放掉生成的水。
③加热回流2 h,反应过程中即时打开旋塞放掉生成的水。
④反应结束,冷却至室温,向烧瓶中加饱和Na2CO3溶液
至溶液呈中性。
⑤用分液漏斗分离出有机层,即得到粗产品。
⑥向粗产品中加无水CaCl2,蒸馏得精产品。
(1)制备苯甲酸乙酯的化学方程式为 。
(2)步骤②的方法是 。
(3)步骤③用分水器不断分离出水的目的是 。
(4)沸石的作用是 ,步骤⑥中无水CaCl2的作用是 。
(5)步骤④可使产品纯度变高,用化学方程式表示一种酸性杂质被除掉的反应原理 。
(6)步骤④中测定溶液pH值的方法是 。
-
有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是( )
A. 分离、提纯→确定化学式→确定实验式→确定结构式
B. 分离、提纯→确定实验式→确定化学式→确定结构式
C. 分离、提纯→确定结构式→确定实验式→确定化学式
D. 确定化学式→确定实验式→确定结构式→分离、提纯
-
有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是 ( )
A. 分离、提纯→确定化学式→确定实验式→确定结构式
B. 分离、提纯→确定结构式→确定实验式→确定化学式
C. 分离、提纯→确定实验式→确定化学式→确定结构式
D. 确定化学式→确定实验式→确定结构式→分离、提纯
-
有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物
让你研究,一般要采取的几个步骤是 ( )
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯


CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
密度为1g/mL),则正丁醇的利用率约为__________。