-
(16分)(1)某温度下,纯水中的c(H+)=2.0×10—7mol/L,此时溶液的c(OH—)= mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10—4mol/L,则溶液中c(OH—)= mol/L,由水电离产生的c(H+)= mol/L,此时温度 25℃(填“高于”、“低于”或“等于”)。
(2)室温时,将pH=5的H2SO4稀释10倍,则c(H+)∶c(SO42—)= ,将稀释后的溶液再稀释1000倍,则c(H+)∶ c(SO42—)= 。
(3)有稀硫酸和稀盐酸的混合溶液20ml,向此溶液中滴加0.025mol/LBa(OH)2溶液时,生成沉淀的质量和溶液pH的变化情况如图所示,求:
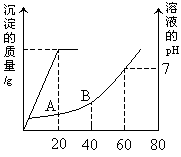
⑴原混合溶液中硫酸和盐酸的物质的量浓度?
⑵滴到A、B两点时溶液的pH 各是多少?
高二化学填空题中等难度题查看答案及解析
-
某温度下纯水中的C(H+)=2×10-7mol/L,则此时溶液中的C(OH-)=______;若温度不变,滴入稀盐酸,使C(H+)=5×10-4mol/L,则溶液中C(OH-)=______,此时溶液中由水电离产生的C(H+)=______.
高二化学解答题中等难度题查看答案及解析
-
某温度下,纯水中的c(H+)=2.0×10-7mol/L,此时溶液的c(OH-)=_______mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10-4mol/L,则溶液中c(OH-)=________mol/L,由水电离产生的c(H+)=_______mol/L,此时温度_______25℃(填“高于”、“低于”或“等于”)。
高二化学简答题困难题查看答案及解析
-
(1)某温度下,纯水中的c(H+)=2.0×10—7mol/L,此时溶液的c(OH—)= mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10—4mol/L,则溶液中,由水电离产生的c(H+)= mol/L,此时温度 25℃(填“高于”、“低于”或“等于”)。
(2)某温度下的水溶液中,c(H+) = 10x mol/L,c(OH—) = 10y mol/L,x和y的关系
如图所示。计算:
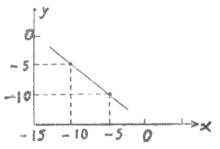
①该温度下水的离子积为_____
②该温度下,0.01mol/L的NaOH溶液的pH为_______
高二化学填空题困难题查看答案及解析
-
(1)某温度下,纯水的c(H+)=2×10-7mol•L-1,则此时c(OH-)为________;若温度不变,滴入稀盐酸使c(H+)=5×10-4mol•L-1则溶液中c(OH-)为________,由水电离产生的c(H+)为________,此时温度________(填“高于”、“低于”或“等于”25℃)
(2)已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
①C(s)+O2(g)═CO2(g)△H1=-393.5kJ/mol
②H2(g)+O2(g)═H2O(g)△H2=-242.0kJ/mol
③CO(g)+O2(g)═CO2(g)△H3=-283.0kJ/mol
写出C(s)与水蒸气反应生成CO和H2的热化学方程式:________.
(3)在25℃下,向浓度均为0.1mol•L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20).
(4)常温下,0.l mol•L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)________c(CO32-)(填“>”、“=”或“<”).
(5)在25℃下,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,反应完成后溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”),a________0.01mol•L-1(填“>”、“=”或“<”).高二化学填空题中等难度题查看答案及解析
-
(1)某温度下,纯水中的c(H+)=2.0×10-7mol·L-1,则此时溶液的c(OH-)=________ mol·L-1;若温度不变,滴入稀盐酸使c(H+)=5.0×10-6 mol·L-1,则c(OH-)=_________ mol·L-1。
(2)在2mL 0.1mol·L-1的NaCl溶液中,加入2mL 0.1mol·L-1的AgNO3溶液,可观察到白色沉淀生成。将此混合液过滤,向滤渣中加入2mL 0.1mol·L-1的KI溶液,搅拌,可观察到_______________, 反应的离子方程式为______________________。
(3)下列说法不正确的是_____________。
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
B.所有物质的溶解都是吸热的
C.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全
D.除去溶液中的Mg2+,用OH-沉淀Mg2+比
用效果好,说明 Mg(OH)2的溶解度比MgCO3大
(4)25 ℃,两种常见酸的电离常数如下表所示。
Ka1
Ka2
H2SO3
1.3×10-2
6.3×10-8
H2CO3
4.2×10-7
5.6×10-11
①
的电离常数表达式 K =_____________。
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为______________。
高二化学综合题中等难度题查看答案及解析
-
下列说法正确的是( )
A.强酸的水溶液中不存在OH-
B.pH=0的溶液是酸性最强的溶液
C.在温度不变时,水溶液中c(H+)和c(OH-)不能同时增大
D.某温度下,纯水中c(H+)=2×10-7mol·L-1,其呈酸性
高二化学单选题中等难度题查看答案及解析
-
(1)25℃时,0.05mol/L H2SO4溶液的pH= _________
(2)某温度下纯水的c(H+)=4.0×10-7mol/L,则此溶液中的c(OH-)= ________;若温度不变,滴入稀盐酸,使c(H+)=2.0×10-4mol/L,则此溶液中由水电离产生的c(H+)= _________。
(3)氢氧化铜悬浊液中存在如下平衡:Cu(OH)2(s)
Cu2+(aq)+2OH-(aq),常温下其Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol·L-1,如要生成Cu(OH)2沉淀,应调整溶液使之pH> ________
(4)向明矾溶液中逐滴加入Ba(OH) 2溶液至硫酸根离子刚好完全沉淀时,溶液的pH________7(填>、<、=),离子反应总方程式________________________________________向明矾溶液中逐滴加入Ba(OH) 2溶液至铝离子刚好完全沉淀时,溶液的pH________7(填>、<、=),离子反应总方程式________________________________________
高二化学填空题中等难度题查看答案及解析
-
(14分)
(1)纯水中c(H+)=5.0×10-7mol/L,则此时纯水中的c(OH-)= ;
若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,则c(OH-)= 。
(2)在CH3COONa的溶液中,各离子的物质的量浓度由大到小的顺序是 。
(3)明矾的水溶液显酸性,其原因是(用离子方程式表示) 。
(4)在25℃、101kPa下,0.5mol的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为 。
(5)1L 1 mol·L-1 H2SO4溶液与2L 1 mol·L-1 NaOH溶液完全反应,放出114.6kJ热量,则表示中和热的热化学方程式为 。
(6)已知:① N2(g)+2O2(g)=2NO2(g) △H=+67.7 kJ/mol ;
② N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534 kJ/mol
则N2H4与NO2与完全反应生成氮气和气态水的热化学方程式为 。
高二化学填空题中等难度题查看答案及解析
-
(6分)
(1)纯水中c(H+)=5.0×10-7mol/L,则此时纯水中的c(OH-) =_______________;若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,则c(OH-) =_______________;在该温度时,往水中滴入NaOH溶液,溶液中的C(OH-)=5.0×10-2 mol/L,则溶液中c(H+)= ________。
高二化学填空题中等难度题查看答案及解析