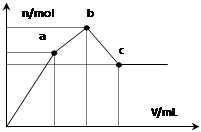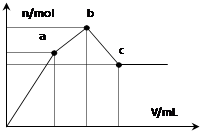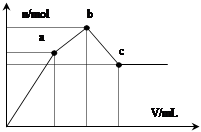-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积(V)的变化,沉淀的总物质的量(n)的变化如右图所示。则下列说法中正确的是( )
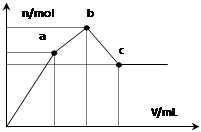
A.a点的溶液呈中性
B.b点发生反应的离子方程式是: Al3++2SO42-+2Ba2++3OH— = Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200mL
D.c点溶液呈碱性
-
浓度为 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液100 mL中,逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )
A.a点对应的沉淀,其物质的量为0.01mol
B.b点发生反应的离子方程式是:
Al3++2SO42-+2Ba2++3OH-== Al(OH)3↓+2BaSO4↓
C.沉淀质量最大值为4.66g
D.c点加入Ba(OH)2溶液的体积为250 mL
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4 )2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )
)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )
A.a点发生反应的离子方程式是:
Al3++2SO42-+2Ba2++3OH— = Al(OH)3↓+2BaSO4↓
B.b点消耗Ba(OH)2溶液体积为200mL
C.从a→b 、b→c点过程中发生反应的离子方程式依次为:NH4++OH-=NH3·H2O;Al(OH)3+OH-=AlO2-+2H2O
D.沉淀的质量:a点>c点
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )
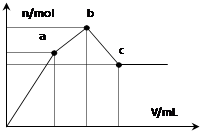
A.a点发生反应的离子方程式是: Al3++2SO42-+2Ba2++3OH— = Al(OH)3↓+2BaSO4↓
B.b点消耗Ba(OH)2溶液体积为200mL
C.从a→b 、b→c点过程中发生反应的离子方程式依次为:
NH4++OH-=NH3·H2O Al(OH)3+OH-=AlO2-+2H2O
D.沉淀的质量:a点>c点
-
向100mL 0.1mol∙ L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol ·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积(V)的变化,沉淀总物质的量(n)的变化如右图所示。下列叙述正确的是

A.a点的沉淀总物质的量为0.03mol
B.oa段发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-= 2BaSO4↓+Al(OH)3↓;
C.ab段发生反应的离子方程式是:2NH4++SO42-+Ba2++2OH-=2NH3∙H2O+ BaSO4↓
D.反应到c点时,加入Ba(OH)2溶液的总体积为250mL
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )
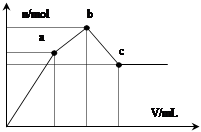
A.a点发生反应的离子方程式是:
Al3++2SO42-+2Ba2++3OH— = Al(OH)3↓+2BaSO4↓
B.b点消耗Ba(OH)2溶液体积为200mL
C.从a→b 、b→c点过程中发生反应的离子方程式依次为:NH4++OH-=NH3·H2O Al(OH)3+OH-=AlO2-+2H2O
D.沉淀的质量:a点>c点
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是
A.a点的溶液呈中性
B.从开始到b点发生反应的总的离子方程式是:
Al3++2SO42-+2Ba2++3OH-= Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.c点溶液呈碱性
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如右图所示。则下列说法中正确的是

A.a点的溶液呈中性
B.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH— == Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.c点溶液呈碱性
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如右图所示。

则下列说法中正确的是 ( )
A.a点的溶液呈中性
B.b点发生反应的离子方程式是:
Al3++2SO42-+2Ba2++3OH— == Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.c点溶液呈碱性
-
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是

A.a点的溶液呈中性
B.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓
C.c点溶液呈碱性
D.c点加入Ba(OH)2溶液的体积为200 mL
)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )