-
对于反应 2H2(g)+ O2(g) 2H2O(g);△H=-483.6 kJ/mol,下列说法正确的是
A.反应物具有的总能量高于生成物 B.H2的燃烧热△H=-241.8kJ/mol,
C.破坏H-H键要放出热量 D.升高温度重新达到平衡,平衡常数增大
高二化学选择题简单题查看答案及解析
-
已知:2H2(g) +O2(g)=2H2O(g) ΔH =-483.6 kJ·mol−1
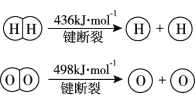
下列说法不正确的是
A.该反应可作为氢氧燃料电池的反应原理
B.破坏1 mol H-O键需要的能量是463.4 kJ
C.H2的燃烧热ΔH<-241.8 kJ·mol−1
D.H2(g)中的H-H键比H2O(g)中的H-O键牢固
高二化学单选题简单题查看答案及解析
-
对于2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ·mol-1热化学方程式的下列说法正确的是( )
A. 氢气与氧气反应放出483.6kJ 热量
B. 氢气与氧气反应生成1mol 水蒸气时放出483.6kJ 热量
C. 2个H2分子燃烧生成水蒸气放出483.6kJ
D. 2molH2与1molO2生成2mol水蒸气放出483.6kJ热量
高二化学选择题简单题查看答案及解析
-
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
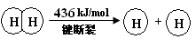

下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H—O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
高二化学选择题中等难度题查看答案及解析
-
已知热化学方程式:2H2(g)+O2(g)=2H2O(g) ΔH1=-483.6kJ/mol, 则对于热化学方程式:2H2O(l)=2H2(g)+O2(g) ΔH2=b,下列说法正确的是[ ]
A.该反应的ΔH2=+483.6kJ/mol B.|ΔH2|<|ΔH1|
C.|ΔH2|>|ΔH1| D.热化学方程式中化学计量数表示分子个数
高二化学选择题简单题查看答案及解析
-
已知热化学方程式:2H2(g)+O2(g)═2H2O(g);△H1=-483.6kJ•mol-1.
则对于热化学方程式:2H2O(g)═2H2(g)+O2(g);△H2=bkJ•mol-1的说法正确的是( )
A.热化学方程式中H2O前面的“2”表示“每2个液态水分子分解,就有bkJ•mol-1的热量变化”
B.b=+483.6
C.|△H2|>|△H1|
D.|△H2|<|△H1|高二化学选择题中等难度题查看答案及解析
-
已知热化学方程式:2H2(g)+O2(g)===2H2O(g)ΔH1=-483.6kJ/mol
则对于热化学方程式:2H2O(l)===2H2(g)+O2(g)ΔH2=QkJ/mol
下列说法正确的是
A.热化学方程式中化学计量数表示分子个数 B.Q = 483.6
C.Q > 483.6 D.Q < 483.6
高二化学选择题简单题查看答案及解析
-
已知热化学方程式:2H2(g)+O2(g)===2H2O(g) ΔH1=-483.6 kJ/mol,则对于热化学方程式:2H2O(l)===2H2(g)+O2(g) ΔH2=b,下列说法正确的是
A.热化学方程式中化学计量数表示分子个数
B.该反应的ΔH2=+483.6 kJ/mol
C.|ΔH2|<|ΔH1|
D.|ΔH2|>|ΔH1|
高二化学选择题简单题查看答案及解析
-
下列有关反应热的叙述中正确的是( )
(1)已知2H2(g)+ O2(g)= 2H2O(g)△H= -483.6 kJ/mol,则氢气的燃烧热为△H= -241.8 kJ/mol;
(2)由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定;
(3)X(g)+ Y(g)
Z(g)+ W(s) △H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大;
(4)已知:
共价键
C
C
C=C
C
H
H
H
键能/(kJ/mol)
348
610
413
436
上表数据可以计算出
(g) + 3H2(g) →
(g) 的反应热;
(5)由盖斯定律推知: 在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等;
(6)25℃,101kPa,时,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A. (1)(2)(3)(4) B. (3)(4)(5) C. (4)(5) D. (6)
高二化学选择题中等难度题查看答案及解析
-
已知反应:2H2(g)+O2(g)=2H2O(l);△H= -571.6kJ·mol-1,下列对于反应2H2O(l)=2H2(g)+O2(g)的说法不正确的是
A.吸热反应 B.△S>0
C.只能在电解条件下进行 D.在一定温度下可以自发进行
高二化学选择题中等难度题查看答案及解析