在分析化学中,NH3或其水溶液是一种常用的沉淀剂,用于物质的分离和提纯。已知:NH3•H2O的电离常数K=1.8×10-5,K sp[Mg(OH)2]=1.8×10-11。向体积为1.0 L、浓度为2.0×10-4 mol·L-1的MgCl2溶液中通入NH3,若不考虑溶液体积变化,当反应开始有白色沉淀出现时,通入NH3的体积(标准状况)为( )
A.112mL B.224mL C.118.72 mL D.201.6 mL
高三化学选择题中等难度题
在分析化学中,NH3或其水溶液是一种常用的沉淀剂,用于物质的分离和提纯。已知:NH3•H2O的电离常数K=1.8×10-5,K sp[Mg(OH)2]=1.8×10-11。向体积为1.0 L、浓度为2.0×10-4 mol·L-1的MgCl2溶液中通入NH3,若不考虑溶液体积变化,当反应开始有白色沉淀出现时,通入NH3的体积(标准状况)为( )
A.112mL B.224mL C.118.72 mL D.201.6 mL
高三化学选择题中等难度题
在分析化学中,NH3或其水溶液是一种常用的沉淀剂,用于物质的分离和提纯。已知:NH3•H2O的电离常数K=1.8×10-5,K sp[Mg(OH)2]=1.8×10-11。向体积为1.0 L、浓度为2.0×10-4 mol·L-1的MgCl2溶液中通入NH3,若不考虑溶液体积变化,当反应开始有白色沉淀出现时,通入NH3的体积(标准状况)为( )
A.112mL B.224mL C.118.72 mL D.201.6 mL
高三化学选择题中等难度题查看答案及解析
25℃时,部分物质的电离平衡常数如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O | H2SO3 |
| 电离平衡常数 | 1.8×10-5 | K1=4.2×10-7 K2=5.6×10-11 | 4.7×10-8 | 1.8×10-5 | Ka1=1.3×10-2;Ka2=6.2×10-8 |
(1) 25℃时,等浓度的Na2CO3溶液、CH3COONa溶液、Na2SO3溶液,三种溶液的pH由大到小的顺序为 _______________
(2)工业上可用氨水除去尾气SO2。将SO2通入氨水中,当c(OH-)降至1.0×10-7mol/L时,溶液中的=___________
(3)常温下,用0.1000mol/L溶液滴定20.00mL0.1000mol/L CH3COOH溶液所得滴定曲线如图:
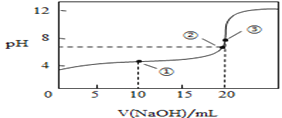
①在滴定的实验过程中,不需要的仪器或用品是________(填序号)
a.100mL容量瓶 b.锥形瓶 c.滴定管夹 d.漏斗 e.玻璃棒 f.滴定管
②到达滴定终点的标志是:___________________________
③下列操作会导致测定结果偏高的是 _________________
A.碱式滴定管在装液前未用标准NaOH溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
④如图点①所示溶液中c(CH3COO-)+c(OH-)__________ c(CH3COOH)+c(H+)(填“”“
”或“
”,下同);点②所示溶液(pH=7)c(Na+)________ c(CH3COO-)+c(CH3COOH);点③所示溶液中所有离子浓度由大到小的顺序为:_______________
(4)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO42-生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为_______mol/L,此时溶液中c(CrO42-)等于_________mol/L(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
高三化学综合题中等难度题查看答案及解析
常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20 mL浓度均为0.1 mol/L NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。下列说法不正确的是
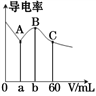
A.a=20,b=40,且溶液呈中性处于A、B两点之间
B.B点溶液中:c(CH3COO-)>c(Na+)>c(NH)
C.已知lg3≈0.5,则C点的pH≈5
D.A、B、C三点中,B点溶液中水的电离程度最大
高三化学单选题中等难度题查看答案及解析
常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20 mL浓度均为0.1 mol/L NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。下列说法不正确的是
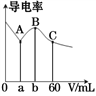
A. a=20,b=40,且溶液呈中性处于A、B两点之间
B. B点溶液中:c(CH3COO-)>c(Na+)>c(NH)
C. 已知lg3≈0.5,则C点的pH≈5
D. A、B、C三点中,B点溶液中水的电离程度最大
高三化学单选题困难题查看答案及解析
已知:25℃时,氨水的电离常数Kb(NH3·H2O) = 1.8×10-5。该温度下,用0.1 mol·L-1的氨水滴定10.00 mL 0.1 mol·L-1的HA溶液,溶液的pH与所加氨水的体积(V)的关系如图所示。下列说法正确的是( )
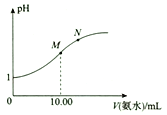
A. HA为弱酸
B. M点溶液中存在c(A-)=c(NH4+)+c(NH3·H2O)
C. M、N两点溶液中水电离出来的c(H+):M<N
D. 25℃时,NH4+的水解平衡常数为1.8×10-9
高三化学选择题困难题查看答案及解析
常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5mol·L-1。向20mL浓度均为0.1mol·L-1 NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的电导率与加入CH3COOH溶液的体积(V)关系如图所示。下列说法错误的是
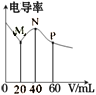
A. M点:c(Na+)>c(CH3COO-)>c(NH3·H2O)>c(NH4+)
B. 溶液呈中性的点处于N、P之间
C. 已知1g3≈0.5,P点的pH=5
D. P点:3[c(CH3 COO-)+ c(CH3COOH)]=2[ c(Na+)+c(NH4+)+c(NH3·H2O)]
高三化学单选题困难题查看答案及解析
常温下,CH3COOH与NH3•H2O的电离常数均为1.8×10-5。现向20mL浓度为0.1mol/LNH3•H2O的溶液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。
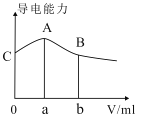
下列说法正确的是( )
A.a=20,A点溶液的pH=7
B.A、B两点中,B点溶液中水的电离程度最大
C.A点溶液中:c(CH3COO-)>c(NH4+)>c(H+)>c(OH-)
D.B、C两点中溶液的pH相等
高三化学单选题中等难度题查看答案及解析
常温下,已知电离常数Kb(NH3·H2O)=1.8×10-5; Ka1(H2C2O4)=5.9×10-2, Ka2(H2C2O4)=6.4×10-5。下列说法正确的是
A.NH4HC2O4溶液中,c(NH4+)= c(HC2O4-)
B.用H2C2O4溶液中和氨水至中性时,溶液中c(NH4+)=c(HC2O4-)+2c(C2O42-)
C.(NH4)2 C2O4溶液呈酸性,属于酸式盐
D.等物质的量浓度的氨水和H2C2O4溶液等体积混合,所得溶液呈碱性。
高三化学单选题中等难度题查看答案及解析
(10分)分子筛可用于物质的分离提纯。某种型号的分子筛的工业生产流程可简单表示如下:

(1)在加NH3·H2O调节pH的过程中,若pH控制不当会有Al(OH)3生成。已知常温下,Al(OH)3浊液的pH=3,其Ksp=1×10-36,则其中c(Al3+)=▲ 。
(2)生产流程中所得滤液的主要成分为▲ (写化学式)。
(3)假设生产流程中铝元素和硅元素均没有损耗,钠原子的利用率为10%,试通过计算确定该分子筛的化学式(写出计算过程)。
(4)分子筛的孔道直径为4Å称为4A型分子筛;当Na+被Ca2+取代时就制得5A型分子筛,当Na+被K+取代时就制得3A型分子筛。要高效分离正丁烷(分子直径为4.65Å)和异丁烷(分子直径为5.6Å)应该选用▲ 型的分子筛。
高三化学填空题中等难度题查看答案及解析
常温下,向0.1 mol·L-1氨水中加入少许N2O5,使溶液中c(NH3·H2O)∶c(NH)=5∶9,此时溶液的pH=________。(25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5)
高三化学计算题中等难度题查看答案及解析