-
氧化铁是重要工业颜料,以废铁屑为原料制备氧化铁的步骤如下:(部分操作和条件略)
步骤1:用碳酸钠溶液洗去铁屑表 面的油污。
面的油污。
步骤2:加入稍过量的稀硫酸,保持50~80℃,充分反应后,过滤。
步骤3:将滤液与稍过量的NH4HCO3溶液混合,得到FeCO3的浊液。
步骤4: 、 、 ,得到FeCO3固体。
步骤5:煅烧FeCO3,得到Fe2O3固体。
(1)步骤2中,如何判断反应已经充分? 。
(2)步骤2所得的滤渣中主要含有一种铁的化合物W(Fe3C),经以下处理后,回收利用:W在足量的空气中高温煅烧,生成有磁性的固体X;将X溶于稀硫酸。
①煅烧时1 mol W消耗O2 mol。
②X溶于稀硫酸的离子方程式为 。
(3)步骤3生成FeCO3反应的化学方程式为 。
(4)将步骤4补充完整: 、 、 。
(5)若煅烧时条件控制不当,会使产品中存在杂质FeO。
①若要设计实验检验产品中是否存在FeO,且只能选用两种试剂,这两种试剂是 。
②现煅烧116.0 kg的FeCO3,得到79.2 kg产品,则该产品的纯度为__________。(设产品中只有一种杂质FeO,计算结果保留3位有效数字)
-
氧化铁是重要工业颜料,以废铁屑为原料制备氧化铁的步骤如下:(部分操作和条件略)
步骤1:用碳酸钠溶液洗去铁屑表面的油污。
步骤2:加入稍过量的稀硫酸,保持50~80℃,充分反应后,过滤。
步骤3:将滤液与稍过量的NH4HCO3溶液混合,得到FeCO3的浊液。
步骤4: 、 、干燥,得到FeCO3固体。
步骤5:煅烧FeCO3,得到Fe2O3固体。
(1)步骤2中,如何判断反应已经充分? 。
(2)步骤2所得的滤渣中主要含有一种铁的化合物W(Fe3C),经以下处理后,回收利用:W在足量的空气中高温煅烧,生成有磁性的固体X;将X溶于稀硫酸。
①煅烧时1 mol W消耗O2 mol。
②X溶于稀硫酸的离子方程式为 。
(3)步骤3生成FeCO3反应的化学方程式为 。
(4)将步骤4补充完整: 、 。
(5)若煅烧时条件控制不当,会使产品中存在杂质FeO。
①若要设计实验检验产品中是否存在FeO,且只能选用两种试剂,这两种试剂是 。
②现煅烧116.0 kg的FeCO3,得到79.2 kg产品,则该产品的纯度为__________。(设产品中只有一种杂质FeO,计算结果保留3位有效数字)
-
氧化铁是重要的工艺颜料,用废铁屑制备它的流程如下:回答下列问题:
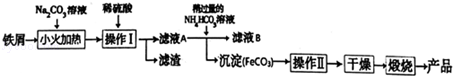
(1)①加碳酸钠溶液并小火加热的操作目的是 ;
②操作Ⅰ的名称是 ,操作Ⅱ的名称是 ;
(2)①流程所发生的反应为FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O过程中,加入稍过量的NH4HCO3溶液后,且要控制溶液的为6.8~7.2之间.加入稍过量的目的是 ,溶液的pH不能过低的原因是
②检验滤液B中含有NH4+的方法是 .
(3)有些同学认为KMnO4溶液滴定能进行铁元素含量的测定.
a、称取2.85g绿矾(FeSO4•7H2O)产品,配成250mL溶液;
b、量取25.00mL待测溶液于锥形瓶中;
c、用硫酸化的0.0100mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式 .
②用KMnO4标准溶液滴定时应选用 滴定管(填“酸式”或“碱式”).
③计算上述样品中FeSO4•7H2O的质量分数为 .
-
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3mol·L-1H2SO4溶液,在 60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有__________(填仪器编号)
①铁架台 ②燃烧匙 ③锥形瓶 ④广口瓶 ⑤研体 ⑥玻璃棒 ⑦酒精灯
(2)在步骤1中所加的碳酸钠溶液中需要煮沸,其目的是_______;
(3)在步骤3中,“一系列操作”依次为______、_______和过滤;
(4)本实验制得的硫酸亚铁铵晶体常含有Fe3+杂质。检验Fe3+常用的操作方法是_____。
-
硫酸亚铁铵(NH4)2SO4·FeSO4·6H2O为浅绿色晶体,实验室中以废铁屑为原料来制备,步骤如下:
步骤1:将铁屑放入与铁不反应的洗涤剂去除铁表面的油污,分离出液体,洗净铁屑
步骤2:向处理过的铁屑中加入过量的稀硫酸 溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3:向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1中的分离操作,所用到的玻璃仪器有____________________。(填仪器编号)
①漏斗 ②分液漏斗 ③烧杯 ④广口瓶 ⑤铁架台 ⑥玻璃棒 ⑦酒精灯
(2)为确认晶体中Fe2+在制备过程中没有被氧化,请你设计简单的实验方案进行验证(写出简单的实验过程、实验现象及结论)_______________________________________
-
铝是一种重要金属,工业上用铝土矿(主要成分为Al2O3,还有少量的Fe2O3,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
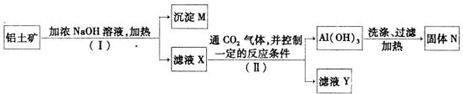
①I和II步骤中分离溶液和沉淀的操作是__________________;
②沉淀M中除含有泥沙外,一定还含有_____________________;
③步骤Ⅲ中加热Al(OH)3得到固体N的操作需要使用的仪器除了酒精灯、三角架、泥三角,还有______________;(填入仪器的名称)
④滤液X中,含铝元素的溶质的化学式为___________;实验室里常往AlCl3溶液中加入___________(填“氨水”或“NaOH溶液”)来制取A1(OH)3.
-
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO47H2O。
Ⅱ.将FeSO47H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀, 干燥后得到FeCO3固体。
干燥后得到FeCO3固体。
Ⅴ.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是_________________。
(2)Ⅱ中,需加一定量硫酸。运用化学平衡原理简述硫酸的作用_____________。
(3)Ⅲ中,生成FeCO3的离子方程式是_____________。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是_____________。
(4)Ⅳ中,通过检验SO42-来判断沉淀是否洗涤干净。检验SO42-的操作是_____________。
(5)已知煅烧FeCO3的化学方程式是4FeCO3+O2 2Fe2O3+4CO2。现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是_________kg。(摩尔质量/gmol-1:FeCO3116Fe2O3160FeO72)
2Fe2O3+4CO2。现煅烧464.0kg的FeCO3,得到316.8kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是_________kg。(摩尔质量/gmol-1:FeCO3116Fe2O3160FeO72)
-
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO4•7H2O.
Ⅱ.将FeSO4•7H2O配制成溶液.
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液.
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO3固体.
V.煅烧FeCO3,得到Fe2O3固体.
已知:NH4HC03在热水中分解.
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是______.
(2)Ⅱ中,需加一定量硫酸.运用化学平衡原理简述硫酸的作用______.
(3)Ⅲ中,生成FeCO3的离子方程式是______.若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是______.
(4)IV中,通过检验SO42-来判断沉淀是否洗涤干净.检验SO42的操作是______.
(5)已知煅烧FeCO3的化学方程式是4FeCO3+O2  2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品.若产品中杂质只有FeO,则该产品中Fe2O3的质量是______Kg.
2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品.若产品中杂质只有FeO,则该产品中Fe2O3的质量是______Kg.
-
有“锂”走遍天下。氧化锂(Li2O)是锂电池工业的重要原料,以粗碳酸锂为原料制备氧化锂的一种工艺流程如下:

注:常温下,碳酸锂微溶于水,氢氧化锂可溶于水。
(1)反应Ⅰ中通入CO2需加压的原因是______。
(2)反应Ⅱ生成LiOH的化学方程式为______。
(3)浓缩、结晶所得LiOH·H2O通过灼烧得到Li2O。LiOH·H2O中常含有少量的Li2CO 3,但该物质对所制Li2O的纯度无影响,其原因是______。
(4)锂离子电池大量应用在手机、笔记本电脑和家用小电器上。标记为Li-ion的锂离子电池的电池反应可表示为:Li + 2Li0.35NiO2 2Li0.85NiO2。
2Li0.85NiO2。
①放电时,负极的电极反应式为______。
②充电时,能量转化形式主要是______。
③锂离子电池使用非水溶液做离子导体的原因是______(用离子方程式表示)。
④安全使用锂离子电池的措施有______。
-
工业以黄铜矿(主要成分是CuFeS2)为原料制备粗铜,进一步以粗铜为原料制备CuSO4·5H2O晶体。工艺流程如下(部分操作和条件略):
I. 煅烧黄铜矿,得到粗铜(含铁及铁、铜的化合物等);
II. 向粗铜中加入稀H2SO4和稀HNO3,并使产生的NO与H2O、O2反应;
III. 调节Ⅱ中所得溶液的pH,过滤;
Ⅳ. 将Ⅲ中滤液浓缩后冷却结晶,过滤,得到CuSO4·5H2O晶体。
已知:生成氢氧化物的pH
| Cu(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 4.8 | 1.5 |
| 完全沉淀时 | 6.7 | 2.8 |
注:金属离子的起始浓度为0.1 mol/L
请回答:
(1)I中主要发生如下两个化学反应。请将反应ii的化学方程式补充完整。
i. 2CuFeS2+4O2 Cu2S+3SO2+2FeO
Cu2S+3SO2+2FeO
ii.  Cu2S+
Cu2S+ O2
O2 
 _________+
_________+  SO2
SO2
(2)II中NO与H2O、O2反应的化学方程式是_________。
(3)III中的滤渣主要是Fe(OH)3。调节溶液的pH时,pH范围是_________。
(4)有关上述过程的说法中,正确的是_________(填序号)。
a. I中尾气含有SO2,可综合利用制备H2SO4。
b. II中稀HNO3的作用之一是使Cu单质转化为Cu2+
c. 在上述过程中,HNO3可循环利用
面的油污。


