-
某实验小组为了探究SO2的性质,设计了如下装置,
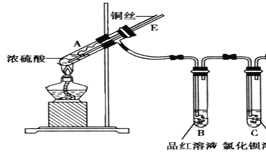
实验步骤:
①先连接好装置,检查气密性,再加入试剂;
②加热A试管;
③将铜丝向上抽动离开液面。
(1)A试管中发生反应的化学方程式是______。
(2)B试管中的现象是______。
(3)试管C无明显现象,某小组取一部分反应后的溶液,分别滴加以下试剂,请你预测能否生成沉淀,若生成沉淀,写出生成沉淀的化学式。
| 加入试剂 | 能否生成沉淀 | 沉淀的化学式 |
| 氯水 | _____________ | __________ |
| 氨水 | __________ | ___________ |
-
(16分)Ⅰ、某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示:
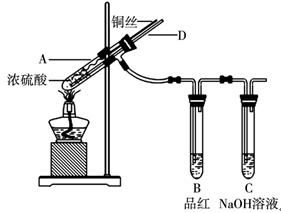
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。
(3)若将B中品红溶液换成溴水,通入一段时间后溴水褪色,这说明了二氧化硫具有漂白性,你是否同意这个观点 ,(填“同意”或“不同意”),说明理由 (用离子方程式表示)。
Ⅱ、以浓硫酸、浓硝酸、粗铜、水和空气为原料可制得硫酸铜晶体。其过程如下图所示。
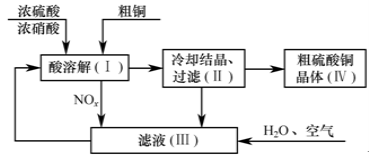
回答下列问题:
(4)配平在滤液(Ⅲ)中发生反应的化学方程式: NOx+ H2O+ O2= HNO3
(5)写出制取硫酸铜的总反应方程式: 。
(6)在上述生产过程中,被循环使用的物质是 。
-
某同学对教材中铜与浓硫酸的实验作出如下改进。实验装置如图所示(加热和夹持装置已略去)。
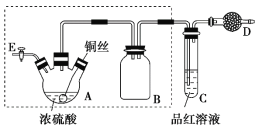
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检查虚线框内装置气密性的方法是____________________________。
(2)装置A的名称是________,装置B的作用是_________,装置D中所盛药品是__________。
(3)装置A中发生反应的化学方程式为____________________________。
(4)实验后,拆除装置前,为避免有害气体的泄漏,应当采取的操作是__________。
(5)实验后装置A中有白色固体产生,将装置A中固液混合物缓慢转移至盛有少量水的烧杯中,可观察到的现象是______________;不可直接向装置A中加水的原因是__________。
-
某课题组为了深入探究二氧化硫的性质设计以下装置进行了实验。

步骤一:检验装置气密性后向B、C中各加入20mL图示液体。
步骤二:打开A中活塞,反应进行10分钟后关闭活塞。
步骤三:用pH计分别测量B、C试管中溶液的pH。
结合上述实验,回答以下问题:
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为_______________________。
(2)甲同学认为两瓶中pH大致相等,原因是二氧化硫溶于水后生成了酸性物质_____________,该物质发生电离所致。
(3)通过pH计测定,B瓶中pH为2.13,C瓶中pH为1.05。为了解释该实验现象,该同学提出进行多次平行实验,目的是_______________________。
测定结果如下:
| 第1次实验 | 第2次实验 | 第3次实验 |
| B瓶中pH | 2.15 | 2.10 | 2.17 |
| C瓶中pH | 1.10 | 1.12 | 1.09 |
实验发现:C瓶中溶液的酸性始终比B瓶中的酸性强。
(4)通过查阅文献,I﹣可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程分两步进行如下,将ii补充完整。
i.SO2+4I﹣+4H+=S↓+2I2+2H2O
ii.I2+2H2O+___═___+___+2I﹣
(5)最终结论:C瓶中溶液酸性强于B瓶,是由于生成了____________,该过程中体现出二氧化硫哪些化学性质________________(选填“氧化性”,“还原性”)。
-
某班在实验室进行制取乙酸乙酯的分组实验,主要步骤如下:
①按下图连接好装置,并检查装置的气密性。
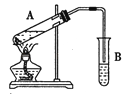
②在试管A中加入3 mL乙醇,然后边振荡试管边慢慢加入2 mL浓硫酸和2 mL乙酸,再加入沸石。然后用酒精灯缓慢加热.
③待试管B中收集到一定量产物后停止加热,撤出试管B,振荡后静置。
| 相对分子质量 | 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | 水中溶解性 |
| 乙醇 | 46 | 0.789 | -117.3 | 78.5 | 以任意比互溶 |
| 乙酸 | 60 | 1.050 | 16.6 | 117.9 | 易溶 |
| 乙酸乙酯 | 88 | 0.897 | -84 | 77 | 难溶 |
回答下列问题:
(1)反应的化学方程式为______________。
(2)两组同学想要比较所制得的乙酸乙酯的产量,简便的方法是__________。
(3)该反应为可逆反应,要提高乙酸乙酯的产率,该实验中采取的措施有_________。
(4)现对全班同学试管B中的液体集中处理,得到乙酸乙酯的粗产品并回收乙醇,需进行的操作名称是__________。
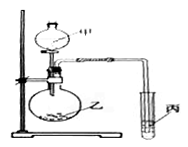
(5)用下图所示装置验证:乙酸的酸性比碳酸强,碳酸的酸性比苯酚强。
装置中所装的药品分别是:甲_________,乙________,丙____________。试管中观察到的现象是________。
-
某同学设计了如图所示的实验装置(夹持装置已略去)来研究苯和溴发生的反应.
实验步骤如下:①按如图所示的装置连接好仪器;②检查装置的气密性;③在装置A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞;④待烧瓶a中气体收集满后,向烧杯中加水,挤压预先盛有水的胶头滴管,观察实验现象.
请回答下列问题:

(1)装置A中发生反应的化学方程式为 .
.
(2)能证明装置A中发生的反应为取代反应的实验现象是
(3)装置B的作用是 .
(4)为除去溴苯中混有的少量溴,常向混合物中加入的试剂是 (填化学式),充分振荡,静置后再 (填操作名称).
-
为了探究乙醇氧化的反应机理,某研究性学习小组的学生设计了下列实验方案:将一根粗铜丝绕成螺旋状,称得其质量为m1g。另取一支试管,加入3mL乙醇。
(1)将上述已称量过的铜丝放在酒精灯火焰上加热至红热后稍冷,可看到铜丝______(填写现象),再称得其质量为m2g,并且m2________m1(填大于、小于或等于)。
(2)若将红热的铜丝伸入试管中的酒精溶液中,可看到铜丝__________(填写现象)。
(3)反复多次,可闻到试管里溶液有刺激性气味。最后将从酒精中取出的铜丝烘干后称量,其质量为m3g,则m3________m1(填写大于、小于或等于)。
(4)此实验总的化学反应方程式为__________________。
-
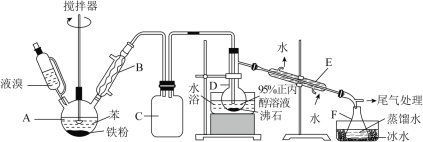
溴苯和1-溴丙烷是重要的医药中间体。某化学兴趣小组设计如下方案制得两种有机物,实验步骤如下:
I.连接装置后,检査气密性。向各容器中加入一定量的药品。
II.将液溴滴入装置A中,保持75℃水浴加热装置C10min。
III.反应完毕后,将装置F馏出液分离,得1-溴丙烷的粗产品。
IV.将分出的粗产品,依次用12mLH2O、12mL5%Na2CO3溶液和12mLH2O洗涤,进一步提纯得1-溴丙烷。
有关数据如下:
| 苯 | 溴 | 溴苯 | 1-溴丙烷 | 正丙醇 |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 | 1.36 | 0.8 |
| 沸点/℃ | 80 | 59 | 156 | 71 | 97.1 |
| 水中溶解度 | 难溶 | 难溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)写出装置A中发生反应的方程式:________。
(2)装置B的作用________。
(3)步骤IV中第一步水洗的目的主要是________。
(4)制得的溴苯中含有少量的苯,提纯溴苯的实验操作名称________。
(5)从锥形瓶内分离出1-溴丙烷粗产品,所采用的操作名称是________ 检验1-溴丙烷中的溴原子,需加入的试剂
检验1-溴丙烷中的溴原子,需加入的试剂 按照先后顺序写
按照先后顺序写 ________。
________。
-
某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题.
Ⅰ探究浓硫酸的某些性质
(1)按图示连接装置,检查装置的气密性,称量E的质量.
(2)将a g铁碳合金样品放入A中,再加入适量的浓硫酸.仪器A的名称为______,
未点燃酒精灯前,A、B均无明显现象,其原因是:______.
(3)点燃酒精灯一段时间后,A、B中可观察到明显现象.
A中开始发生反应的化学方程式为:2Fe+6H2SO4  Fe2(SO4)3+3SO2↑+6H2O和______ CO2↑+2SO2↑+2H2O
Fe2(SO4)3+3SO2↑+6H2O和______ CO2↑+2SO2↑+2H2O
-
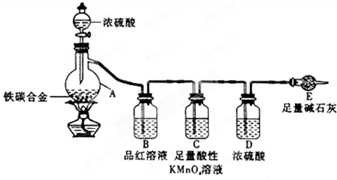
某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题。
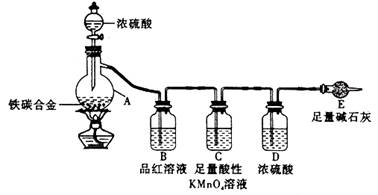
Ⅰ 探究浓硫酸的某些性质
(1)按图示连接装置,检查装置的气密性,称量E的质量。
(2)将a g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为____________,
未点燃酒精灯前,A、B均无明显现象,其原因是:_______________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显现象。
A中开始发生反应的化学方程式为:2Fe +6H2SO4  Fe2(SO4)3 + 3SO2↑ +6H2O
Fe2(SO4)3 + 3SO2↑ +6H2O
和______________________________________ (写化学方程式)。
B中的现象是_________,由此可得到浓硫酸具有_______性,C装置的作用________。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式__ __。
(5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是_____________________________________。
Ⅱ 测定铁的质量分数
(6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。
铁碳合金中铁的质量分数为_____________________(写表达式),为使实验数据更为精确,可在装有碱石灰的干燥管后加入________________________________。








 .
.

