-
以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料可制备金属镁和溴。流程如下:

(1)操作Ⅰ的名称是 ,所用主要玻璃仪器的名称是 。
(2)加入Ba2+的目的是 。用CaO调节溶液Y的pH,可以使Mg2+沉淀完全。由下表中数据可知,理论上选择pH范围是 。
| 开始沉淀时 | 沉淀完全时 |
| Mg2+ | pH=9.6 | pH=11.0 |
| Ca2+ | pH=12.2 | c(OH-) =1.8mol/L |
(3)在空气中加热MgCl2·6H2O,可以生成Mg(OH)Cl,相应反应的化学方程式是 。
(4)化肥厂生产铵态氮肥(NH4)2SO4的部分流程如图:

向装有CaSO4悬浊液的沉淀池中先通氨气,再通CO2的原因(请从溶解度和平衡移动角度分析) 。
-
以含有Ca2+、Mg2+、Clˉ、SO42ˉ、Brˉ 等离子的卤水为主要原料可制备金属镁和溴。流程如下:

(1)操作Ⅰ的名称是______,所用主要玻璃仪器的名称是_________、_________;需要选择的试剂是____________(填序号)。
a.乙醇 b.苯 c.四氯化碳 d.裂化汽油
(2)通氯气反应的离子方程式__________________________________。
(3)证明SO42ˉ完全沉淀的方法是______________________________。
(4)CaO用来调节溶液Y的pH,可以使Mg2+沉淀完全,由下表中数据可知,理论上应控制pH范围是__________。
| 开始沉淀时 | 沉淀完全时 |
| Mg2+ | pH=9.6 | pH=11.0 |
| Ca2+ | pH=12.2 | c(OH-) =1.8mol/L |
(5)操作Ⅱ用下图所示操作______________实现(填“能”或“不能”)。原因是______________________________(用化学方程式解释)。
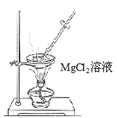
(6)工业上用惰性电极电解熔融状态下的氯化镁来冶炼镁,不能直接电解氯化镁溶液的原因是___________________________(用离子方程式表示)。
(7)在探究Mg(OH)2溶解性的实验中,发现向装有少量Mg(OH)2浊液的试管中加入适量NH4Cl晶体,充分振荡后浊液会变澄清,请用化学平衡的原理解释浊液变澄清的原因_________________________________。
-
实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
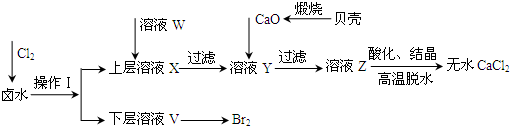
(1)操作Ⅰ使用的试剂是______,所用的主要仪器名称是______.
(2)加入溶液W的目的是______.用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择的pH最大范围是______.酸化溶液Z时,使用的试剂为______.
| 开始沉淀时的pH | 沉淀完全时的pH |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol•L-1 |
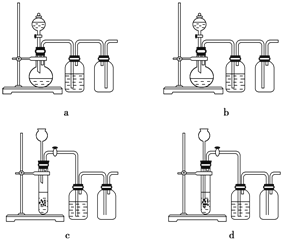
(3)实验室用贝壳与稀盐酸反应制备并收集气体,下列装置中合理的是______.
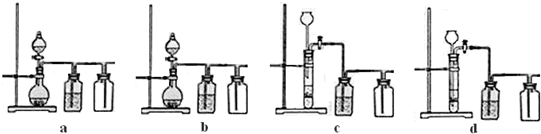
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11.某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3.该实验设计不正确,错误在于______.
设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论).______.
仪器自选.
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸.
-
实验室以含有Ca2+、Mg2+、Cl-、SO 、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
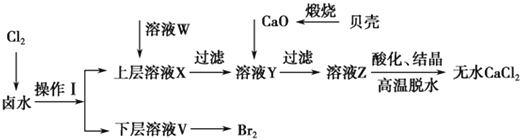
(1)操作Ⅰ使用的试剂是____________,所用主要仪器的名称是________。
(2)加入溶液W的目的是______________。用CaO调节溶液Y的pH,可以除去Mg2+。由表中数据可知,理论上可选择的pH最大范围是____________。酸化溶液Z时,使用的试剂为__________。
| 开始沉淀时的pH | 沉淀完全时的pH |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8 mol·L-1 |
(3)实验室用贝壳与稀盐酸反应制备并收集CO2气体,下列装置中合理的是__________。
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11。某同学设计实验验证H2SO3的酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于___________________________。用一个化学方程式表示H2SO3酸性强于H2CO3: __________________。
-
天然海水中主要含有Na+、K+ ,Ca2+、Mg2+、Cl-、SO42—、Br-、CO32—、HCO3—等离子,火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
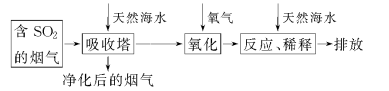
下列说法错误的是 ( )
A.天然海水pH≈8的原因是海水中的CO32—、HCO3—水解
B.“氧化”是利用氧气将H2SO3、HSO3—、SO32—等氧化生成SO42—
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸
D.“排放”出来的海水中SO42—的物质的量浓度与进入吸收塔的天然海水相同
-
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示,下列说法错误的是( )
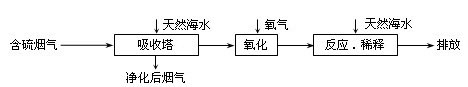
A.天然海水pH ≈ 8的原因是由于海水中的CO32-、HCO3-水解
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应.稀释”时加天然海水的目的是中和.稀释经氧化后海水中生成的酸
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
-
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示,下列说法错误的是
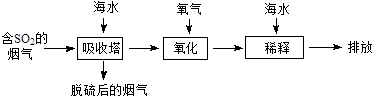
A.海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B.吸收塔中发生的反应有SO2+H2O H2SO3
H2SO3
C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42-
D.经稀释“排放”出的废水中,SO42-浓度与海水相同
-
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示,下列说法错误的是
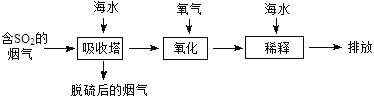
A.海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B.吸收塔中发生的反应有SO2+H2O H2SO3
H2SO3
C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42-
D.经稀释“排放”出的废水中,SO42-浓度与海水相同
-
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示:
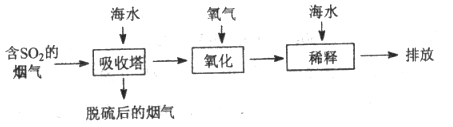
下列说法错误的是
A. 海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B. 吸收塔中发生的反应有SO2+H2O H2SO3
H2SO3
C. 氧化主要是氧气将HSO3-、SO2-、H2SO3氧化为SO42-
D. 经稀释“排放”出的废水中,SO42-浓度与海水相同
-
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示,下列说法错误的是
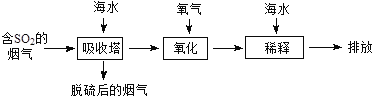
A.海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B.吸收塔中发生的反应有SO2+H2O H2SO3
H2SO3
C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42-
D.经稀释“排放”出的废水中,SO42-浓度与海水相同













