-
综合利用海水可以制备氯化铵、纯碱、金属镁等物质,其流程如下图所示:
 (1)反应①~⑤中,属于氧化还原反应的是__________(填编号)
(1)反应①~⑤中,属于氧化还原反应的是__________(填编号)
(2)写出反应②的离子方程式_______________
(3)X溶液中的主要阳离子是Na+和___________
(4)已知氨气极易溶于水,实验室可用NH4Cl和Ca(OH)2固体混合加热制取。根据流程原理制取碳酸氢钠固体,下列实验装置正确且能达到实验目的的是_________
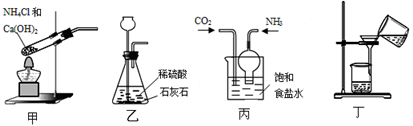
A.用装置甲制取氨气
B.用装置乙制取二氧化碳
C.用装置丙制取碳酸氢钠
D.用装置丁分离碳酸氢钠固体与母液
(5)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次滴加过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③______________;④滴加适量盐酸;⑤_____________________(请补全缺少的实验操作)
(6)检验纯碱样品中是否含NaCl,至少应选用的试剂是____________________
(7)电解熔融氯化镁制镁,得到的镁蒸气可在下列哪种气体氛围中冷却(填序号)________________
A.H2 B.CO2 C.O2 D.N2
-
综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:

(1)反应①~⑤中,属于氧化还原反应的是 (填编号)。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③ ;④加适量盐酸;⑤ 。(请补全缺少的实验步骤);若②步中改为依次加入过量的Na2CO3溶液、NaOH溶液、BaCl2溶液,则产生的后果是 。
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
-
综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:
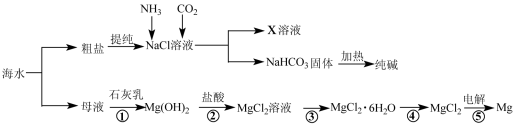
(1)反应①~⑤中,属于氧化还原反应的是 (填编号)。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③ ;④加适量盐酸;⑤ (请补全缺少的实验步骤)。
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
-
综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:
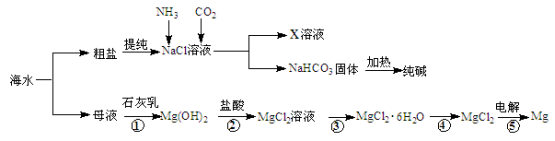
(1)反应①~⑤中,属于氧化还原反应的是 (填编号)。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③ ;④加适量盐酸;⑤ 。(请补全缺少的实验步骤)
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
-
综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示:

(1)反应①~⑤中,属于氧化还原反应的是 。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;
③ ;④加适量盐酸;⑤ (请补全缺少的实验步骤)。
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
-
海水的综合利用可以制备金属钠和镁,其流程如下图所示:
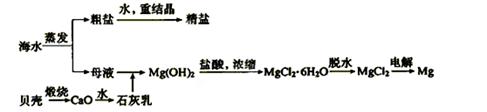
下列说法不正确的是( )
A.要检验母液中是否含氯离子应当用硝酸酸化的硝酸银溶液进行实验
B.上述流程中所有反应都是非氧化还原反应
C.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2= Mg(OH)2+Ca2+
D.不用电解MgO来制取镁是因为MgO熔点高,能耗大
-
综合利用海水可以制备食盐、纯碱、金属镁等钩质,其流程示意图如下:
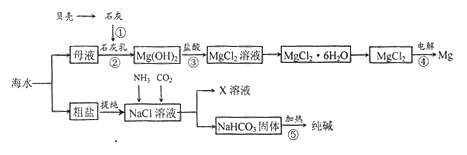
(1)在上述反应①~⑤中,没有涉及的化学反应类型是______。
A.分解反应 B.化合反应
C.复分解反应 D.置换反应
(2)写出反应③的离子方程式______________。
(3)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;
②依次加入过量的BaCl2溶液、NaOH溶液、_____________;
③过滤;
④______________;
⑤蒸发结晶。
其中加入过量氯化钡溶液的目的是____________________。
(4)X溶液中的主要阳离子是Na+和________________。
(5)检验纯碱样品中是否含NaCl应选用的试剂是______________。
-
海水的综合利用可以制备金属镁,其流程如下图所示
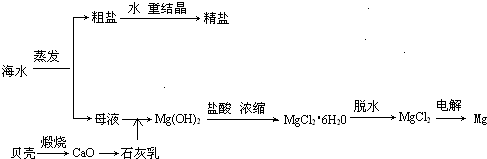
(1)制取金属镁时,可以用电解MgCl2的方法,写出相应的反应的化学方程式______ Mg+Cl2↑
-
海水的综合利用可以制备金属钠和镁等,其流程如下图所示:
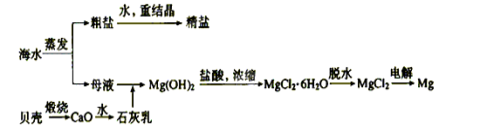
下列说法不正确的是 ( )
A.海水提盐都属于物理变化
B.利用母液可进一步提取溴,但要富集
C.上述流程中生成Mg(OH)2沉淀的离子方程式为:Mg2++Ca(OH)2= Mg(OH)2+Ca2+
D.不用电解MgO来制取镁是因为MgO熔点高,能耗大
-
海水的综合利用可以制备金属镁,其流程如下图所示:

(1)完成下列方程式:
煅烧贝壳(化学方程式): ;
Mg(OH)2加盐酸(离子方程式):
(2)电解熔融MgCl2的反应化学方程式是 。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,分别说明在这3种情况下使用玻璃棒的目的。
溶解时: 。
过滤时: 。
蒸发时: 。
(4)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl和HCl,写出相应反应的化学方程式: 。
 (1)反应①~⑤中,属于氧化还原反应的是__________(填编号)
(1)反应①~⑤中,属于氧化还原反应的是__________(填编号)








