-
某小组同学在实验室设计实验模拟工业生产。
Ⅰ.用消石灰和氯化铵固体制备NH3

(1)NH3的发生装置应选择图中的__(填字母代号),制备NH3的化学方程式为__。
(2)欲收集一瓶干燥的NH3,选择图中的装置,其连接顺序为:发生装置→__(按气流方向,用小写字母表示)。
Ⅱ.设计了如图所示的实验装置模拟工业生产制备少量硝酸。

(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃以上,由此可知该反应是__(填“吸热”或“放热”)反应,反应的化学方程式是__。
(4)B中试剂为__,NaOH溶液的作用是__。
(5)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。白烟的化学式是__。
②欲使氨气尽可能完全转化为硝酸,理论上n(NH3):n(NO)的最佳比例为__。
-
某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如图所示的实验装置。
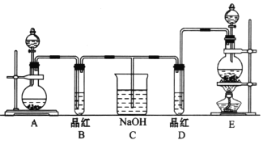
(1)实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用图中A、E两发生装置中___装置(填装置序号)制Cl2。在制Cl2的反应中浓盐酸所表现出的性质是___。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:___D:___。
(3)装置C的作用是____。
(4)甲乙两名同学分别利用如图所示装置探究两种气体按不同比例混合后的漂白性,试
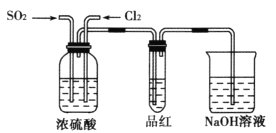
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是___。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色写出其相应的离子方程式:___。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅。其原因是__。
-
氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
(1)用消石灰和氯化铵固体制备NH3
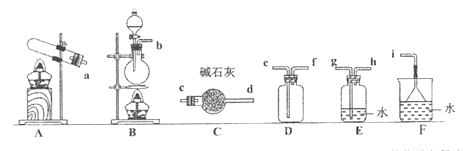
①NH3的发生装置应选择上图中的_______(填序号),制备NH3的化学方程式为______。
②欲收集一瓶干燥的NH3,选择上图中的装置,其连接顺序为:发生装置→_________(按气流方向,用小写字母表示)。
(2)研究NH3与NO2的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
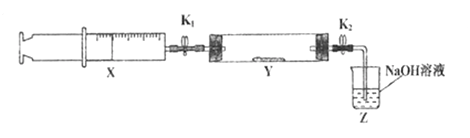
| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中__________ | ②反应的化学方程式 _______________ |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
| 打开K2 | 溶液倒吸入Y管 | ③________________ |
-
某学习小组同学利用如图装置研究氨气的性质。

请回答下列问题。
(1)实验室用熟石灰与氯化铵制备氨气的化学方程式是_______。
(2)下列物质能用于干燥氨气的有_____________(填字母序号)。
a.  固体 b.
固体 b.  固体
固体
c.碱石灰 d.浓
(3)B中观察到的现象是_________,反应的化学方程式是_________。
(4)C中观察到的现象是__________,反应的化学方程式是___________。
-
某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了下列装置进行实验。已知:
①A 中反应为 KClO3+6HCl(浓) = KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为 Ca(OH)2,其他杂质不参与反应。
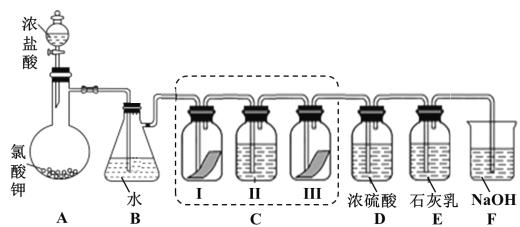
(1)写出 B 装置中反应的化学方程式_______________。实验结束后,立即将 B 中溶液滴几滴在紫色石蕊试纸上,可观察到的现象是______________
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中 I、II、III 处依次放入的物质正确的是_________(填编号)。
| 编号 | I | II | III |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 浓硫酸 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
(3)待 E 中物质完全反应后,经过一系列加工处理,得到漂白粉样品,其主要成份为_________、____________(填化学式)。
(4)F 装置的作用是(用离子方程式表示)_____________
(5)为测定(3)中所得漂白粉的有效成份含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2 至不再产生沉淀为止,该过程的化学方程式为_____________。若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成份的质量分数为_________________(用含 a、b 的式子表示)。
-
某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
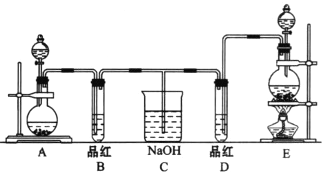
(1)实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中______装置(填装置序号)制Cl2,在制Cl2的反应中浓盐酸所表现出的性质是______.
(2)应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:________, D:_________.
(3)装置C的作用是__________。
(4)甲乙两名同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性,试分析:
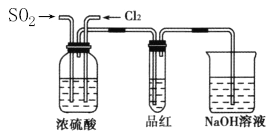
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是____________。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色。其原因是 ,并写出其相应的离子方程式:_________.
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅。其原因________
-
化学小组利用下图装置进行某些气体的制备和性质实验,图中夹持装置有省略
(1)为制取干燥氨气,可将装置C与装置D连接,则装置D中 的固体宜选用__ __。
A.碱石灰 B.无水氯化钙 C.五氧化二磷 D.生石灰
(2)装置F可用于探究氯气和氨气反应,实验室打开开关1、3,关闭2,先向烧瓶中通入__ __,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,写出该反应的化学方程式 。请设计一个实验方案鉴定该固体中的阳离子________ __________。
(3)利用装置A、E,可设计实验比较氯离子和溴离子的还原性强弱,能证明结论的实验现象是______ ______.
(4)将装置B、C分别与F相连后,进行硫化氢和二氧化硫反应的实验,若通入烧瓶中的硫化氢和二氧化硫体积比为2:1,打开开关3后烧瓶中的实验现象为__________ _________.
-
学生设计的用氨催化法制取少量HNO3溶液的实验装置如图所示:

(1)实验室制备NH3,下列方法中适宜选用的是 (填序号).
①固态氯化铵与熟石灰混合加热 ②固态氯化铵加热分解
③碱石灰中滴加浓氨水 ④氯化铵溶液与氢氧化钠溶液共热
(2)装置B中发生反应的化学方程式为 .
(3)装置C的作用是 ;
装置C中的现象是 ;为确保装置D中尽可能多地生成HNO3,所通入O2和NH3的体积比应大于 .
(4)装置D中发生的反应化学方程式为 .
-
某化学实验小组设计下图装置制备氯气,图中涉及气体发生、除杂、干燥、收集及尾气处理装置。
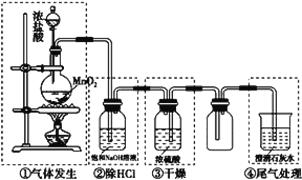
(1)上述装置中,错误的是____________(选填字母)。
A.①②④ B.①②③ C.①③④ D.②③④
(2)写出装置①中发生反应的化学方程式_____________________________________。该反应中,氧化剂是__________________。
(3)使0.15mol MnO2 与过量的12mol/L的浓盐酸反应,使50mL 12mol/L的浓盐酸与足量MnO2反应,两者产生的氯气相比(其他条件相同)____________(选填字母)。
A.一样多 B.前者较后者多
C.后者较前者多 D.无法比较
(4)将新制氯水滴到pH试纸上,有何现象?_________________________________。
(5)工业上用氯气生产漂白粉的化学反应方程式为______________________________。
-
某研究性学习小组设计实验验证氨气与二氧化硫的性质。请你完成下列研究:
(一)氨气性质探究
(1)实验室制备氨气,下列方法中可选用的是 (填编号)
①加热浓氨水;②固体生石灰中滴加浓氨水;③固态氯化铵加热分解;④固态硝酸铵加热分解;
(2)该小组成员设计实验探究氨气还原性及产物,提供实验装置如下:
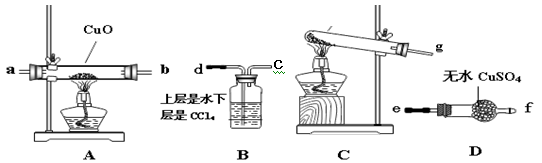
(3)请你根据提供的装置从左至右连接接口序号( )( )( )( )( )( )
(4)该装置在设计上有一定的缺陷,为确保实验结果的准确性,你对该装置的改进措施是________________;
(5)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式________________;
(6)装置B的作用是:________________;
(二)二氧化硫性质探究
下图是实验室制取SO2并验证SO2的某些性质的装置,试回答:
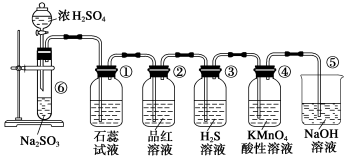
(1)盛放浓硫酸仪器的名称:_________________;
(2)若将浓硫酸改用浓硝酸能否完成此实验探究?答:____________,请写出改用浓硝酸后⑥中的离子反应方程式:_____________________________________
(3)②实验现象为:_________________,证明SO2具有________性;
(4)若③中的试剂改为Na2S溶液,实验现象与原溶液是否相同:______________,含有1mol Na2S的水溶液最多可以吸收SO2的物质的量为:________。
(5)④中发生的离子反应为:_______________________________________。














