-
常温下,将0.20 mol/LKMnO4酸性溶液 0.l0L与一定量pH=3.0的草酸(HOOC-COOH)溶液混合,放出VL气体。NA表示阿伏加德罗常数的值,下列说法正确的是
A.9 g HOOC-COOH含共用电子对数目为0.9NA
B.当0.01mol KMnO4 被还原时,强酸提供的H+数目为 0.01NA
C.pH=3.0的草酸溶液含有H+数目为0.001NA
D.该反应释放 CO2分子数目为VNA/22.4
高三化学单选题中等难度题查看答案及解析
-
常温下,将0.1L0.2mol/LKMnO4酸性溶液与一定量pH=3的草酸(HOOC-COOH)溶液混合,放出VL气体。NA代表阿伏加德罗常数的值,下列说法正确的是
A. pH=3的草酸溶液含有H+数目为0.001NA
B. 当1molKMnO4被还原时强酸提供H+数目为NA
C. 1molHOOC-COOH含共用电子对数目为9NA
D. 该反应释放CO2分子数目为
高三化学单选题中等难度题查看答案及解析
-
常温下,将0.1L0.2mol/LKMnO4酸性溶液与一定量pH=3的草酸(HOOC-COOH)溶液混合,放出VL气体。NA代表阿伏加德罗常数的值,下列说法正确的是
A. pH=3的草酸溶液含有H+数目为0.001NA
B. 当1molKMnO4被还原时强酸提供H+数目为NA
C. 1molHOOC-COOH含共用电子对数目为9NA
D. 该反应释放CO2分子数目为
高三化学选择题中等难度题查看答案及解析
-
常温下,将0.2mol/LKMnO4酸性溶液0.1L与一定量pH=3的草酸(HOOC—COOH)溶液混合,放出VL气体。NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.0.1molHOOC—COOH含共用电子对数目为0.9NA
B.当1molKMnO4被还原时,强酸提供的H+数目为NA
C.pH=3的草酸溶液含有H+数目为0.001NA
D.该反应释放CO2分子数目为
NA
高三化学单选题中等难度题查看答案及解析
-
常温下,将0.2mol/LKMnO4酸性溶液0.1L与一定量pH=3的草酸(HOOC—COOH)溶液混合,放出VL气体。NA表示阿伏加德罗常数的值,下列说法正确的是
A.该反应释放CO2分子数目为
NA
B.pH=3的草酸溶液含有H+数目为0.001NA
C.0.1molHOOC—COOH含共用电子对数目为0.9NA
D.当1molKMnO4被还原时,转移电子数为10NA
高三化学单选题简单题查看答案及解析
-
锰是重要的过渡元素。
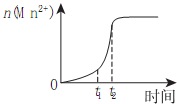
(1)已知常温下KMnO4溶液的pH=7,则0.01mol/LHMnO4溶液的pH=___________;研究表明,一定温度下将酸性KMnO4溶液与草酸溶液混合在一起后,溶液内n(Mn2+)随时间变化的情况如右图,则Mn2+物质的量在t1、t2时段内快速增加的原因可能是___________。
(2)工业上以菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰有多种方法,下面是其中的一种生产流程示意图

常温下几种金属氢氧化物沉淀时的pH:

①滤渣Ⅱ的成分是___________,滤液I中反应的离子方程式为___________,
为确保除尽杂质而又不损失锰,pH的调整范围为___________。
②滤液Ⅱ中加入KClO3、H2SO4后反应的化学方程式为___________,用电解法制备MnO2时阳极上的电极反应式为___________。
(3)锰也是制备某些高能原电池的材料,某二次水溶液锂离子电池充电时,总反应方程式为LiMn2O=4Li1-xMn2O4+xLi。若电池的化学能转化为电能时的能量转化率为85%,则当消耗14g锂时,电路中转移的电子数目为___________NA。
高三化学填空题中等难度题查看答案及解析
-
乙二酸俗称草酸(结构简式为HOOC—COOH,可简写为H2C2O4),它是一种重要的化工原料。(常温下0.01 mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示。)填空:
H2C2O4
KHC2O4
K2C2O4
pH
2.1
3.1
8.1
(1)写出H2C2O4的电离方程式________________。
(2)KHC2O4溶液显酸性的原因是_________________;向0.1 mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是______。
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-) b.c(Na+)=c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-) d.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失。写出反应的离子方程式____________________;又知该反应开始时速率较慢,随后大大加快,可能的原因是______________________。
高三化学综合题中等难度题查看答案及解析
-
常温下,将0.20mol/LH2X溶液与0.20mol/LNaOH溶液等体积混合,所得溶液pH=3.6,继续滴加NaOH溶液至pH=4.0时,溶液中部分粒子浓度(Na+、H2X、HX-、X2-)如下图所示。下列说法错误的是( )

A.图中a代表Na+,d代表H2X分子
B.H2X为二元弱酸,HX-的电离程度大子水解程度
C.混合溶液pH= 3.6时:c(H+)+c(H2X)=c(x2-)+c(OH-)
D.继续滴加NaOH溶液至pH= 7.0时:c(Na+) >c(HX-)+2c(X2-)
高三化学选择题困难题查看答案及解析
-
常温下,有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的盐酸;③pH=11的氨水;④pH=11的NaOH溶液。下列说法正确的是( )
A.①和②混合溶液中:c(H+)=3.0 mol·L-1
B.①和④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)
C.②和③混合溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-)
D.四种溶液稀释100倍,溶液的pH:③>④>②>①
高三化学选择题简单题查看答案及解析
-
常温下,向10mL 0.2mol/L草酸溶液中逐滴加入等浓度的NaOH溶液,溶液中各微粒的物质的量与混合溶液pH的关系如图所示,下列说法正确的是
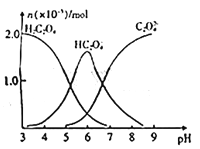
A. 当V(NaOH溶液)< 10mL时,溶液中可能存在:c(Na+)=2c(C2O42-)+c(HC2O4-)
B. 当V(NaOH溶液)=10mL时,溶液中水的电离程度比纯水大
C. 当V(NaOH溶液) =15 mL时,溶液中存在: c(Na+)>c(HC2O4-)>c(C2O42-)
D. 当V(NaOH溶液)=20mL时,溶液中存在:c(OH-) =2c(H2C2O4)+c(H+)+c(HC2O4-)
高三化学单选题中等难度题查看答案及解析