实验室用 NH4Cl、盐酸、NaClO2 为原料制备 ClO2 的过程如下图所示,下列说法不正确的是

A.X 中大量存在的阴离子有 Cl-和 OH- B.NCl3 的键角比 CH4 的键角大
C.NaClO2 变成 ClO2 发生了氧化反应 D.制取 3 mol ClO2 至少需要 0.5mol NH4Cl
高三化学单选题简单题
实验室用 NH4Cl、盐酸、NaClO2 为原料制备 ClO2 的过程如下图所示,下列说法不正确的是

A.X 中大量存在的阴离子有 Cl-和 OH- B.NCl3 的键角比 CH4 的键角大
C.NaClO2 变成 ClO2 发生了氧化反应 D.制取 3 mol ClO2 至少需要 0.5mol NH4Cl
高三化学单选题简单题
实验室用 NH4Cl、盐酸、NaClO2 为原料制备 ClO2 的过程如下图所示,下列说法不正确的是

A.X 中大量存在的阴离子有 Cl-和 OH- B.NCl3 的键角比 CH4 的键角大
C.NaClO2 变成 ClO2 发生了氧化反应 D.制取 3 mol ClO2 至少需要 0.5mol NH4Cl
高三化学单选题简单题查看答案及解析
实验室用 NH4Cl、盐酸、NaClO2 为原料制备 ClO2 的过程如下图所示,下列说法不正确的是

A.X 中大量存在的阴离子有 Cl-和 OH- B.NCl3 的键角比 CH4 的键角大
C.NaClO2 变成 ClO2 发生了氧化反应 D.制取 3 mol ClO2 至少需要 0.5mol NH4Cl
高三化学单选题简单题查看答案及解析
实验室用 NH4Cl、盐酸、NaClO2 为原料制备 ClO2 的过程如下图所示,下列说法不正确的是

A.X 中大量存在的阴离子有 Cl-和 OH- B.NCl3 的键角比 CH4 的键角大
C.NaClO2 变成 ClO2 发生了氧化反应 D.制取 3 mol ClO2 至少需要 0.5mol NH4Cl
高三化学单选题简单题查看答案及解析
实验室用NH4Cl盐酸、NaClO2(亚氯酸纳)为原料制备C1O2的过程如下图所示。

下列说法不正确的是
A. X中大量存在的阴离子有C1-和OH-
B. NH3和NC13中N元素的化合价相同
C. NaClO2变成ClO2发生了氧化反应
D. 制取lmolClO2至少需要molNH4Cl
高三化学选择题简单题查看答案及解析
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色的气体,易溶于水。实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料来制备ClO2,其流程如下:

(1)写出电解时发生反应的化学方程式:。
(2)除去ClO2中的NH3可选用的试剂是________。(填字母)
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.水
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去VmL硫代硫酸钠溶液。
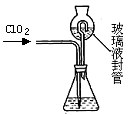
①装置中玻璃液封管的作用是;________。
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式________ ________。
③滴定终点的现象是:________。
④测得通入ClO2的质量m(ClO2)=________。(用含c、V的代数式表示)(已知:ClO2的相对分子质量为67.5)
(4)设计实验来确定溶液X的成分,请补充完成实验步骤和现象。
| 实验步骤 | 实验现象 | 实验结论 |
| ① | 溶液X中含有Na+ | |
| ② | 溶液X中含有Cl- |
高三化学实验题极难题查看答案及解析
(14分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程下如下:
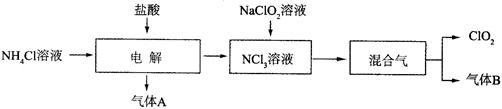
已知:①NCl3是黄色黏稠状液体或斜方形晶体,极易爆炸,有类似氯气的刺激性气味,自然爆炸点为95℃,在热水中易分解,在空气中易挥发,不稳定。②气体B能使湿润的红色石蕊试纸变蓝。
回答下列问题:
(1)电解时,发生反应的化学方程式为________。为保证实验的安全,在电解时需注意的问题是:①控制好生成NCl3的浓度;②________。
(2)NCl3与NaClO2(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO2,该反应的离子方程式为________。
(3)实验室制取气体B的化学方程式为________。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10 mL,稀释成100 mL试样;
步骤2:量取V1 mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30 min。
步骤3:以淀粉溶液作指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。
(已知I2+2S2O32-=2I-+S4O62-)
①若步骤2中未将锥形瓶“在暗处静置30 min”,立即进行步骤3,则测定的结果可能
________(选填“偏大”、“偏小”、“无影响”);
②上述步骤3中滴定终点的现象是________。
③根据上述步骤可计算出原ClO2溶液的浓度为________g / L(用含字母的代数式表示)。
高三化学填空题极难题查看答案及解析
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下图所示:
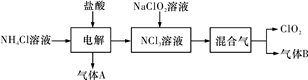
已知:①NCl3是黄色黏稠状液体或斜方形晶体,极易爆炸,有类似于氯气的刺激性气味,自然爆炸点为95 ℃,在热水中易分解,在空气中易挥发,不稳定;②气体B能使湿润的红色石蕊试纸变蓝。
回答下列问题:
(1)电解时,发生反应的化学方程式为_____________。为保证实验的安全,在电解时需注意的问题是:①控制好生成NCl3的浓度;②_________。
(2)NCl3与NaClO2(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO2,该反应的离子方程式为:___________。
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10 mL,稀释成100 mL试样;
步骤2:量取V1 mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30 min。
步骤3:以淀粉溶液作指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL(已知:I2+2S2O===2I-+S4O
)。
①若步骤2中未将锥形瓶“在暗处静置30 min”,立即进行步骤3,则测定的结果可能____(填“偏大”“偏小”或“无影响”);
②根据上述步骤可计算出原ClO2溶液的浓度为_______g/L(用含字母的代数式表示)。
高三化学简答题困难题查看答案及解析
(18分)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,请答题:
(1)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2: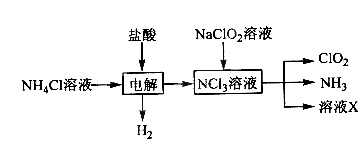
①电解时发生反应的化学方程式为 。
②溶液X中大量存在的阴离子有__________。
③除去ClO2中的NH3可选用的试剂是 (填标号)。
a.水 b.碱石灰 c.浓硫酸 d.饱和食盐水
(2)用下图装置可以测定混合气中ClO2的含量:
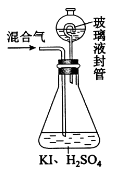
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为 。
②玻璃液封装置的作用是 。
③V中加入的指示剂通常为 ,滴定至终点的现象是 。
④测得混合气中ClO2的质量为 g。(相对原子质量Cl 35.5 O 16)
(3)用ClO2处理过的饮用水会含有一定最的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是_______(填标号)。
a.明矾 b.碘化钾 c.盐酸 d.硫酸亚铁
高三化学填空题困难题查看答案及解析
与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:
NaClO2+HCl→ClO2↑+NaCl+H2O(没有配平)
(1)配平方程式。
NaClO2+
HCl—
ClO2↑+
NaCl+
H2O
(2)该反应中氧化剂和还原剂的物质的量之比_______________________。生成0.2 mol ClO2转移电子的物质的量为________mol。
(3)ClO2对污水中的Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN- a mg·L-1,现用ClO2将CN-氧化,只生成两种无毒气体。处理100 m3这种污水,至少需要ClO2________mol。
高三化学填空题困难题查看答案及解析
以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如下,下列说法中,不正确的是
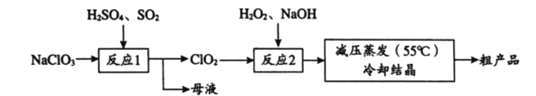
A. 反应1中,每生成1 mol ClO2有0.5 mol SO2被氧化
B. 从母液中可以提取Na2SO4
C. 反应2中,H2O2做氧化剂
D. 采用减压蒸发可能是为了防止NaClO2受热分解
高三化学单选题困难题查看答案及解析