-
粗盐中常含有Ca2+、SO42-和Mg2+等杂质例子,下列除杂试剂添加顺序错误的是
A.NaOH、BaCl2、Na2CO3、HCl B.BaCl2、Na2CO3、NaOH、HCl
C.BaCl2、NaOH、Na2CO3、HCl D.Na2CO3、BaCl2、NaOH、HCl
高三化学单选题简单题查看答案及解析
-
海水是重要的资源,可以制备一系列物质。
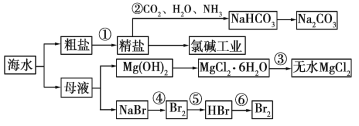
下列说法正确的是
A. 除去粗盐中 SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH 溶液→BaCl2 溶液→Na2CO3 溶液→过滤→盐酸
B. 步骤②中,应先通 CO2,再通 NH3
C. 步骤③中可将 MgCl2·6H2O 晶体在空气中直接加热脱水
D. 步骤④、⑤、⑥反应中,溴元素均被氧化
高三化学单选题中等难度题查看答案及解析
-
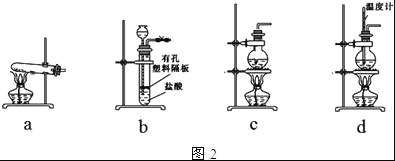
纯碱(Na2CO3)在生产生活中具有广泛的用途.如图1是实验室模拟制碱原理制取Na2CO3的流程图.
完成下列填空:
已知:粗盐中含有Ca2+、Mg2+、SO42﹣等杂质离子.
(1)精制除杂的步骤顺序是____→___→____→____→____ (填字母编号).
a 粗盐溶解 b 加入盐酸调pH c 加入Ba(OH)2溶液 d 加入Na2CO3溶液 e 过滤
(2)向饱和食盐水中先通入NH3,后通入CO2,理由是______.在滤液a中通入NH3和加入精盐的目的是______.
(3)请在图1流程图中添加两条物料循环的路线.____
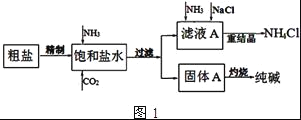
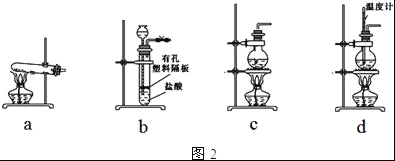
(4)图2装置中常用于实验室制备CO2的是__(填字母编号);用c装置制备NH3,烧瓶内可加入的试剂是___(填试剂名称).
(5)一种天然碱晶体成分是aNa2CO3•bNa2SO4•cH2O,利用下列提供的试剂,设计测定Na2CO3质量分数的实验方案.请把实验方案补充完整:
供选择的试剂:稀H2SO4、BaCl2溶液、稀氨水、碱石灰、Ba(OH)2溶液
①______.
②______.
③______.
④计算天然碱晶体中含Na2CO3的质量分数.
高三化学实验题中等难度题查看答案及解析
-
纯碱(Na2CO3)在生产生活中具有广泛的用途.如图1是实验室模拟制碱原理制取Na2CO3的流程图.
完成下列填空:
已知:粗盐中含有Ca2+、Mg2+、SO42﹣等杂质离子.
(1)精制除杂的步骤顺序是____→___→____→____→____ (填字母编号).
a 粗盐溶解 b 加入盐酸调pH c 加入Ba(OH)2溶液 d 加入Na2CO3溶液 e 过滤
(2)向饱和食盐水中先通入NH3,后通入CO2,理由是______.在滤液a中通入NH3和加入精盐的目的是______.
(3)请在图1流程图中添加两条物料循环的路线.____
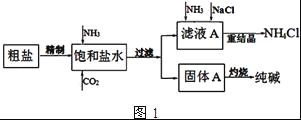
(4)图2装置中常用于实验室制备CO2的是__(填字母编号);用c装置制备NH3,烧瓶内可加入的试剂是___(填试剂名称).
(5)一种天然碱晶体成分是aNa2CO3•bNa2SO4•cH2O,利用下列提供的试剂,设计测定Na2CO3质量分数的实验方案.请把实验方案补充完整:
供选择的试剂:稀H2SO4、BaCl2溶液、稀氨水、碱石灰、Ba(OH)2溶液
①______.
②______.
③______.
④计算天然碱晶体中含Na2CO3的质量分数.
高三化学实验题中等难度题查看答案及解析
-
根据如图海水综合利用的工业流程图,判断下列说法正确的是( )

A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.在过程④中SO2被氧化
C.从第③步到第⑤步的目的是为了浓缩
D.从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
高三化学选择题中等难度题查看答案及解析
-
根据海水综合利用的工业流程图,判断下列说法不正确的是( )
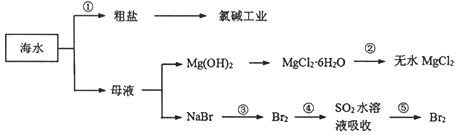
A. 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
B. 在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 从能量转换角度看,氯碱工业电解饱和食盐水是一个将电能转化为化学能的过程
D. 从第④步到第⑤步的目的是富集Br2
高三化学单选题中等难度题查看答案及解析
-
下图所示为海水综合利用的部分流程,下列有关说法正确的是

A. 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质加入的药品顺序为NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B. 第②步是一个将电能转化为化学能的过程,工业上可采用石墨为电极,采用阴离子交换膜的电解装置
C. 第③步中结晶出的MgC12·6H2O可在空气中受热分解制无水MgC12
D. 第④步中反应的离子方程式为C12+2Br-=2C1-+Br2,第④⑤步的目的是富集溴元素
高三化学单选题困难题查看答案及解析
-
如下图所示,利用海水可提取很多重要的化工原料。
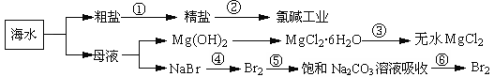
下列有关说法正确的是
A.第①步中除去粗盐中的SO42—、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.第②步中工业上可采用石墨为阴极,铁为阳极,采用阳离子交换膜的电解装置
C.第③步中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2
D.在第④步中溴元素被氧化,第⑤、⑥步中既有溴元素被氧化也有溴元素被还原
高三化学选择题中等难度题查看答案及解析
-
海水是巨大的资源宝库,利用海水提取食盐的过程如图所示。回答下列问题:

(1)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:
A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Na2CO3.溶液。
加入试剂的顺序是 ______。
②电解饱和食盐水时,与电源正极相连的电极上发生的反应为 ______,与电源负极相连的电极附近溶液pH的变化是 。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱,则气体B是 (填化学式),由NaCl制取纯碱反应的化学方程为_______ 、______ ___。
(3)海水提镁的一段工艺流程如图:

浓海水的主要成分如下:
离子
Na+
Mg2+
Cl-
SO42-
浓度/(g•L-1)
63.7
28.8
144.6
46.4
该工艺过程中,脱硫阶段主要反应的离子方程式为 ______,1 L浓海水最多可得到产品2的物质的量为 mol。
高三化学填空题困难题查看答案及解析
-
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图。

根据示意图回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时所用试剂为盐 酸、BaCl2溶液、NaOH溶液、Na2CO3溶液,加入试剂的顺序是、 、、。
(2)电解饱和食盐水的总反应的化学方程式为。
(3)工业上MgCl2·6H2O晶体在________气氛中加热脱水,通入此种气体的作用是。
高三化学综合题简单题查看答案及解析