-
天然水因含有Ca2+、Mg2+、HCO3—等离子,煮沸后会形成水垢。现有一种干燥水垢6.32g ,加热除去全部结晶水,得到固体M 5.78 g;高温灼烧M至恒重,残余固体为CaO和MgO;放出的气体通入足量澄清石灰水中,产生沉淀6.00g;若产生的气体完全被碱石灰吸收,碱石灰增重2.82g。下列推断合理的是( )
A.M 中一定不含Mg(OH)2 B.M中一定含有MgCO3
C.5.78 g M中含CaCO30.05mol D.水垢中碳酸盐质量分数为0.823
高三化学多选题困难题查看答案及解析
-
天然水因含有Ca2+、Mg2+、HCO3—等离子,煮沸后会形成水垢。现有一种干燥水垢6.32g ,加热除去全部结晶水,得到固体M 5.78 g;高温灼烧M至恒重,残余固体为CaO和MgO;放出的气体通入足量澄清石灰水中,产生沉淀6.00g;若产生的气体完全被碱石灰吸收,碱石灰增重2.82g。下列推断合理的是( )
A.M 中一定不含Mg(OH)2 B.M中一定含有MgCO3
C.5.78 g M中含CaCO30.05mol D.水垢中碳酸盐质量分数为0.823
高三化学多选题困难题查看答案及解析
-
天然水大多含Ca2+、Mg2+、HCO3-等离子,加热会产生水垢,水垢中一定含有CaCO3和Mg(OH)2,可能含有MgCO3。
(1)天然水中的HCO3-来自于空气中的CO2。用相关方程式表示CO2溶于水形成HCO3-的过程。______________________________________________________________
(2)天然水煮沸时,其中微溶的MgCO3转换成难溶的Mg(OH)2,写出发生反应的化学方程式。____________________________________________
为确定某水垢样品的成分,利用CaCO3、MgCO3、Mg(OH)2高温分解的性质,精确称量5.000g水垢样品,用如下图装置进行实验。
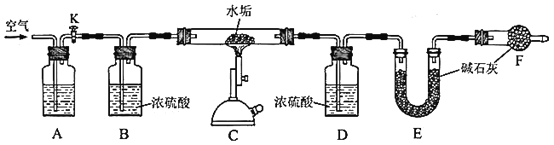
(3)A中盛放的试剂是__________。装置F的作用是_________________________。反应结束后,需要再通入一段时间的空气,目的是_______________________。
(4)利用上述装置测定水垢中Mg(OH)2的含量时,需要测量的数据有__________。
(5)实验测得装置E增重2.200g,请问水垢样品中是否含有MgCO3?判断依据是_______________________________________________________。
高三化学实验题困难题查看答案及解析
-
下列有关硬水及其软化的说法中错误的是( )
A.离子交换法可以软化硬水
B.硬水中含有较多Ca2+,Mg2+
C.生产、生活使用的天然水必须经软化
D.加热可使硬水中的Ca(HCO3)2生成CaCO3沉淀
高三化学单选题简单题查看答案及解析
-
金属Mg及其化合物有重要的用途,请回答下列问题
(1)MgO的重要用途有_______。(写出一种)
(2)井水中含有较多的Ca2+、Mg2+、HCO3-等离子,可以通过煮沸的方式将Mg2+转化为Mg(OH)2,发生的离子方程式是:__________________。
(3)金属Mg可以用来冶炼Ti:2Mg+TiCl4
Ti+2MgCl2。可以用作该反应保护气的是_______。
A. He B. C02 C.N2 D.HCl
(4)在蒸发皿中放人研细的碘和镁粉,无现象,滴入几滴水后立即产生大量的紫烟,紫烟的成分是_________(填分子式);对于实验中水的作用,甲同学认为是水溶解了I2,增大了I2与Mg的接触面积,导致了反应加快,乙同学认为是I2与H2O反应生成了酸,是酸与Mg反应放出热量,加快了I2与Mg的反应,请利用供选试剂:0.01mol/L I2的CCl4溶液、0.01 mol/L I2水、I2粉、Mg粉、蒸馏水,设计实验证明哪位同学的说法合理:____________。(包括实验过程、现象和结论)
(5)一种新型的Mg-H2O2酸性介质电池工作原理如图,正极发生的电极方程式为:__________。
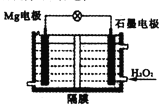
高三化学简答题困难题查看答案及解析
-
用下列方法除去含Ca2+、Mg2+、Cl-、
的硬水,所得的水中含离子浓度最小的是( )
A.蒸馏 B.加热煮沸
C.加Ca(OH)2与Na2CO3 D.离子交换法
高三化学选择题中等难度题查看答案及解析
-
海水的综合利用一直是研究课题。某地天然海水(主要含Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子),研究用海水吸收燃煤排放的含有SO2烟气的工艺流程如图所示,下列说法中正确的是
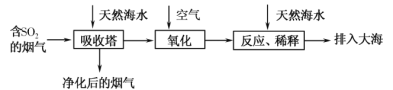
A.工艺中天然海水显酸性
B.氧化过程中可能发生的离子反应为2SO2+2H2O+O2=4H++2SO42-
C.排入大海的溶液与天然海水相比,只有SO42-数量发生了变化
D.若将氧化后的液体进行蒸发结晶,得到的晶体中CaSO4含量最高
高三化学单选题中等难度题查看答案及解析
-
天然海水中主要含有Na+、K+ ,Ca2+、Mg2+、Cl-、SO42—、Br-、CO32—、HCO3—等离子,火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
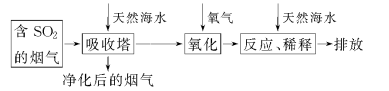
下列说法错误的是 ( )
A.天然海水pH≈8的原因是海水中的CO32—、HCO3—水解
B.“氧化”是利用氧气将H2SO3、HSO3—、SO32—等氧化生成SO42—
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸
D.“排放”出来的海水中SO42—的物质的量浓度与进入吸收塔的天然海水相同
高三化学选择题简单题查看答案及解析
-
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示,下列说法错误的是( )
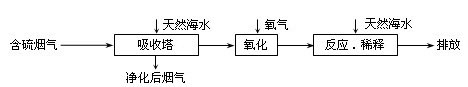
A.天然海水pH ≈ 8的原因是由于海水中的CO32-、HCO3-水解
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应.稀释”时加天然海水的目的是中和.稀释经氧化后海水中生成的酸
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
高三化学选择题简单题查看答案及解析
-
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子.火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:

下列说法错误的是
A.天然海水pH≈8的原因是由于海水中的CO32-、HCO3-水解
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应、稀释”时加天然海水的目的是防止净化海水时生成沉淀
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
高三化学选择题简单题查看答案及解析