-
某烟道气的主要成分是CO2,并含有少量硫氧化物、氮氧化物等杂质。其中的硫元素可在高温下通过CH4的作用回收,主要反应如下:2SO2(g)+CH4(g)⇌CO2(g)+2H2O(g)+S2(g)+Q(Q>0)
(1)以mol/(L•min)为单位,SO2的反应速率是S2生成速率的_________倍。
(2)恒容条件下,不能说明该反应已经达到平衡状态的是_______(选填编号)
a.混合气体中水蒸气含量不再变化
b.混合气体密度不发生变化
c.容器内压强不再变化
d.混合物平均相对分子质量不再变化
达到平衡后升高体系温度,则平衡常数K_________(填“增大”、“减小”、或“不变”)。
(3)请在下式中标出上述反应中电子转移的方向和数目:_____
2SO2(g)+CH4(g)⇌…该反应的氧化产物是_________。SO2的主要性质除氧化性、漂白性外还有________性。
(4)该反应混合物中有两种极性分子,分别是______和_____;固态硫的分子式可能是S8,它与S2互为________。
(5)烟道气中的NO2也能与CH4反应并生成无害气体,完全转化3.0molNO2气体时,需要甲烷的物质的量为__________mol.
高三化学综合题简单题查看答案及解析
-
软锰矿的主要成分是MnO2,还含有少量重金属化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上采用同槽酸酸等工艺制备碳酸锰并回收硫酸铵,其主要流程如下:

(1)为了提高锰元素的浸出率,在“浸取”时可采取的措施有:
①适当升高温度:②搅拌:③ ____________等。
(2) “氧化”中加入MnO2发生反应的离子方程式为____________________________。
(3)“滤渣2”中主要成分的化学式为_____________________。
(4)“除重金属”时使用(NH4)2S而不使用Na2S的原因是_____________________。
(5)“50℃碳化”得到碳酸锰,反应的化学方程式为 _____________________。
(6)生成的碳酸锰产品需经充分洗涤,检验产品完全洗净的方法是_____________________。
高三化学简答题中等难度题查看答案及解析
-
软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
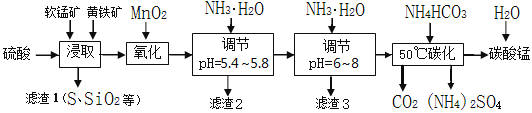
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子
Fe2+
Fe3+
Al3+
Cu2+
Mn2+
开始沉淀pH
7.5
2.7
4.1
5.9
8.8
完全沉淀pH
9.5
3.7
5.4
6.9
10.8
(1)提高浸出率的可采取的措施有_________。
A.适当升高温度 B.搅拌 C.加适量纯碱 D.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是____________________________________________。
(3)调节pH为5.4~5.8的目的是_____________________________________________。
(4)滤渣3的主要成分的化学式是_____________。
(5)50℃碳化过程发生反应的离子方程式是____________________________________。
高三化学填空题困难题查看答案及解析
-
软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
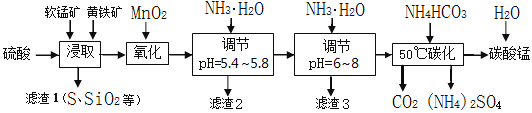
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子
Fe2+
Fe3+
Al3+
Cu2+
Mn2+
开始沉淀pH
7.5
2.7
4.1
5.9
8.8
完全沉淀pH
9.5
3.7
5.4
6.9
10.8
(1)提高浸出率的可采取的措施有____。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________。
(3)调节pH为5.4~5.8的目的是______________。
(4)滤渣3的主要成分的化学式是_______。
(5)采用50℃碳化的原因是_________________________________。该过程发生反应的离子方程式是__________________。
(6)检验碳酸锰产品完全洗净的方法是_______________________________。
高三化学实验题中等难度题查看答案及解析
-
软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
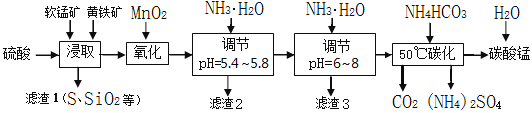
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子
Fe2+
Fe3+
Al3+
Cu2+
Mn2+
开始沉淀pH
7.5
2.7
4.1
5.9
8.8
完全沉淀pH
9.5
3.7
5.4
6.9
10.8
(1)提高浸出率的可采取的措施有____。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________。
(3)调节pH为5.4~5.8的目的是______________。
(4)滤渣3的主要成分的化学式是_______。
(5)采用50℃碳化的原因是_________________________________。该过程发生反应的离子方程式是__________________。
(6)检验碳酸锰产品完全洗净的方法是_______________________________。
高三化学实验题中等难度题查看答案及解析
-
软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
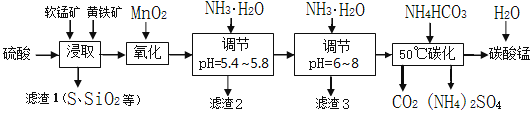
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子
Fe2+
Fe3+
Al3+
Cu2+
Mn2+
开始沉淀pH
7.5
2.7
4.1
5.9
8.8
完全沉淀pH
9.5
3.7
5.4
6.9
10.8
(1)提高浸出率的可采取的措施有____。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________。
(3)调节pH为5.4~5.8的目的是______________。
(4)滤渣3的主要成分的化学式是_______。
(5)采用50℃碳化的原因是_________________________________。该过程发生反应的离子方程式是__________________。
(6)检验碳酸锰产品完全洗净的方法是_______________________________。
高三化学实验题中等难度题查看答案及解析
-
软锰矿的主要成分是MnO2,还含有少量重金属化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上采用同槽酸浸工艺制备碳酸锰并回收硫酸铵,其主要流程如下:
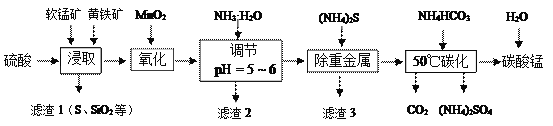
(1)为了提高浸出率,在浸取时可采取的措施有________。
A.适当升高温度 B.搅拌 C.矿石研成粉末 D.延长浸泡时间
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,浸取时发生反应的离子方程式是___________________________。
(3)加入MnO2氧化发生反应的离子方程式是___________________,还可使用______代替MnO2。
(4)滤渣2主要成分的化学式是________________。
(5)50℃碳化发生的化学反应方程式是______________________。
(6)加水洗涤,检验碳酸锰产品完全洗净的方法是___________________。
高三化学简答题困难题查看答案及解析
-
工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物和少量重金属化合物等杂质):
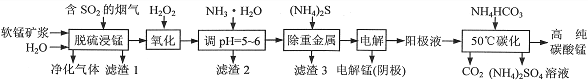
(1)一定温度下,“脱硫浸锰”主要产物为MnSO4,该反应的化学方程式为______________________。
(2)“滤渣2”中主要成分的化学式为______________________。
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是_______________________________________。
(4)“电解”时用惰性电极,阳极的电极反应式为____________________________。
(5)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为_______________________________________。“50℃碳化”时加入过量NH4HCO3,可能的原因是______________________________________(写两种)。
(6)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O
NH3·H2O+H+,则该反应的平衡常数为____________________。
高三化学工业流程中等难度题查看答案及解析
-
工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物和少量重金属化合物等杂质):
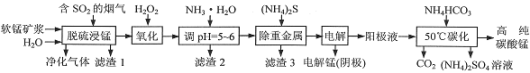
(1)一定温度下,“脱硫浸锰”主要产物为MnSO4,该反应的化学方程式为__。
(2)“滤渣2”中主要成分的化学式为__。
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是__。
(4)“电解”时用惰性电极,阳极的电极反应式为__。
(5)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为___。“50℃碳化”时加入过量NH4HCO3,可能的原因是__(写两种)。
(6)已知:25℃时,Kw=1.0×10-14,Ka(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:NH4++H2O
NH3·H2O+H+,则该反应的平衡常数为__。
高三化学工业流程中等难度题查看答案及解析
-
工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物和少量重金属化合物等杂质):
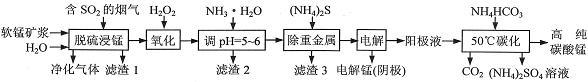
(1)一定温度下,“脱硫浸锰”主要产物为MnSO4,该反应的化学方程式为______________________。
(2)“滤渣2”中主要成分的化学式为______________________。
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是_______________________________________。
(4)“电解”时用惰性电极,阳极的电极反应式为____________________________。
(5)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为_______________________________________。“50℃碳化”时加入过量NH4HCO3,可能的原因是______________________________________(写两种)。
(6)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O
NH3·H2O+H+,则该反应的平衡常数为____________________。
高三化学填空题困难题查看答案及解析