乙炔为原料在不同条件下可以合成多种有机物.
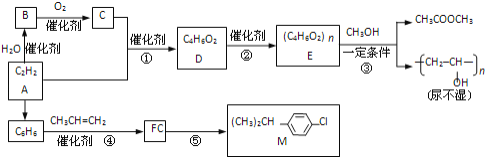
已知:①CH2=CH‑OH(不稳定) CH3CHO
②一定条件下,醇与酯会发生交换反应:RCOOR’+R”OH RCOOR”+R’OH
完成下列填空:
(1)写反应类型:③__反应;④__反应.反应⑤的反应条件__.
(2)写出反应方程式.B生成C__;反应②__.
(3)R是M的同系物,其化学式为,则R有__种.
(4)写出含碳碳双键、能发生银镜反应且属于酯的D的同分异构体的结构简式__.
高三化学推断题困难题
乙炔为原料在不同条件下可以合成多种有机物.

已知:①CH2=CH‑OH(不稳定) CH3CHO
②一定条件下,醇与酯会发生交换反应:RCOOR’+R”OH RCOOR”+R’OH
完成下列填空:
(1)写反应类型:③__反应;④__反应.反应⑤的反应条件__.
(2)写出反应方程式.B生成C__;反应②__.
(3)R是M的同系物,其化学式为,则R有__种.
(4)写出含碳碳双键、能发生银镜反应且属于酯的D的同分异构体的结构简式__.
高三化学推断题困难题
乙炔为原料在不同条件下可以合成多种有机物.

已知:①CH2=CH‑OH(不稳定) CH3CHO
②一定条件下,醇与酯会发生交换反应:RCOOR’+R”OH RCOOR”+R’OH
完成下列填空:
(1)写反应类型:③__反应;④__反应.反应⑤的反应条件__.
(2)写出反应方程式.B生成C__;反应②__.
(3)R是M的同系物,其化学式为,则R有__种.
(4)写出含碳碳双键、能发生银镜反应且属于酯的D的同分异构体的结构简式__.
高三化学推断题困难题查看答案及解析
乙炔为原料在不同条件下可以合成多种有机物.
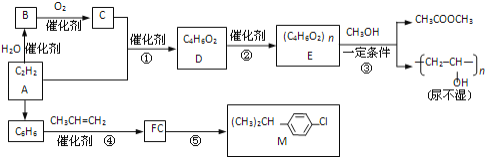
已知:①CH2=CH‑OH(不稳定) CH3CHO
②一定条件下,醇与酯会发生交换反应:RCOOR’+R”OH RCOOR”+R’OH
完成下列填空:
(1)写反应类型:③__反应;④__反应.反应⑤的反应条件__.
(2)写出反应方程式.B生成C__;反应②__.
(3)R是M的同系物,其化学式为,则R有__种.
(4)写出含碳碳双键、能发生银镜反应且属于酯的D的同分异构体的结构简式__.
高三化学推断题困难题查看答案及解析
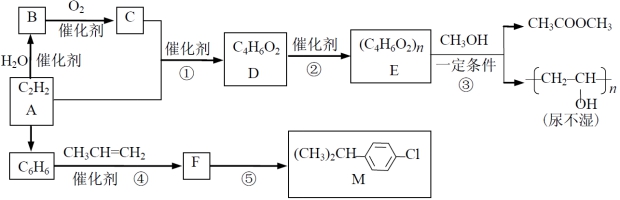
以乙炔为原料在不同条件下可以合成多种有机物。
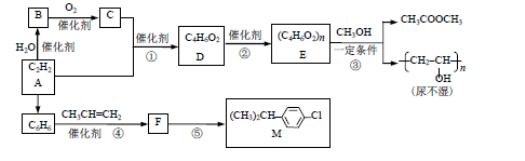
已知: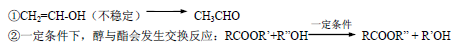
完成下列填空:
(1)B 中官能团名称 ;④的反应类型 。
(2)⑤的反应条件 。
(3)③的化学方程式 。
(4)D 的同分异构体中含碳碳双键、能发生银镜反应且属于酯的共有 种。
高三化学推断题困难题查看答案及解析
以乙炔为原料在不同条件下可以合成多种有机物。
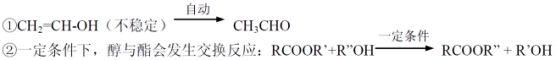
已知:
(1)B 中官能团名称 ;④的反应类型 。
(2)⑤的反应条件 。
(3)③的化学方程式 。
(4)D 的同分异构体中含碳碳双键、能发生银镜反应且属于酯的共有 种。
高三化学推断题困难题查看答案及解析
CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(1)CO2用于生产乙烯,已知:2CO2(g)+6H2(g)CH2=CH2(g)+4H2O(g) △H=QkJ/mol。一定条件下,按不同的投料比X[X=
]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
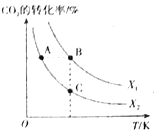
①X1___X2(填“>”或“<”,后同),Q___0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为___。
(2)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO):c(HCO
)=___[常温下K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11]。
②欲用5LNa2CO3溶液将23.3gBaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为___。[已知:常温下Ksp(BaSO4)=1×10-7、Ksp(BaCO3)=2.5×10-6].(忽略溶液体积积的变化)
高三化学综合题中等难度题查看答案及解析
乙炔是一种重要的有机物化工原料,现以它为原料,设计如下转化关系图(部分产物、反应条件已略去),其中A是由等物质的量的乙炔、一氧化碳和水反应而得.
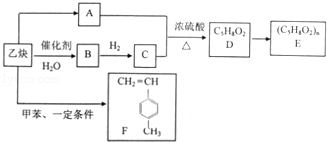
已知:物质不稳定,会自动转化R﹣CH2CHO.请回答:
(1)A分子中的官能团名称为 .
(2)乙炔→F的反应类型是 ;一定条件下,C→B的反应类型是 .
(3)E的结构简式为 .
(4)下列说法中正确的是 (选填编号).
A.F属于芳香烃,且苯是同系物
B.是D的一种同分异构体
C.D既是E是单体,又是E的链节
D.A、B、D、F四种物质都能使溴水褪色
(5)写出反应A+C→D的化学方程式 .
高三化学填空题简单题查看答案及解析
有机物Ⅰ可以用E和H在一定条件下合成如图:
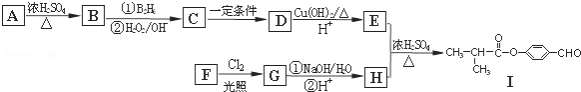
请根据以下信息完成下列问题:
①A为丁醇且核磁共振氢谱有2种不同化学环境的氢;
②R﹣CH=CH2R﹣CH2CH2OH
③一个碳原子上连有两个羟基不稳定,易脱水形成羰基.
(1)B的分子式为: .
(2)C→D、G→H的反应类型为 、 .
(3)芳香族化合物F的分子式为C7H8O,苯环上的一氯代物只有两种,则F的结构简式为: .
(4)D生成E的化学方程式为 .E与H反应生成I的方程式为 .
高三化学推断题极难题查看答案及解析
CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(1)CO2可用于生产甲醇,已知:2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。一定条件下,按不同的投料比X(X=n(H2)/n(CO2))向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。

①X1_______X2(填“>”或“<”,后同),Q_______0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为______。
③TK时,在该容积可变的恒压密闭容器中发生上述反应,测得有关数据如下表所示:
| 物质的量(mol) 时间(min) | 0 | 5 | 10 | 15 | 20 |
| H2(g) | 6.00 | 5.40 | 5.10 | 5.80 | 5.80 |
| CO2(g) | 2.00 | 1.80 | 1.70 | 1.60 | 1.60 |
| CH2=CH2(g) | 0 | 0.10 | 0.15 | 0.20 | 0.20 |
已知在10min时只改变了一个反应条件,用改变的条件可能是______。
④下列情况下能表明该反应达到平衡状态的是_____。
a.气体密度不变 b.混合气休的平均摩尔质量不变 c.消耗速率:2v(H2O)=v(CO2)
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
① 若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=______ [常温下K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11]。
② 欲用5L Na2CO3溶液将23.3 g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为_________。[已知:常温下Ksp(BaSO4)=1×10-7、Ksp(BaCO3)=2.5×10-6]。(忽略溶液体积积的变化)
高三化学填空题中等难度题查看答案及解析
CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(1)CO2可用于生产甲醇,已知:2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。一定条件下,按不同的投料比X(X=n(H2)/n(CO2))向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
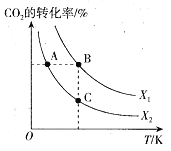
①X1_______X2(填“>”或“<”,后同),Q_______0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为______。
③TK时,在该容积可变的恒压密闭容器中发生上述反应,测得有关数据如下表所示:
| 物质的量(mol) 时间(min) | 0 | 5 | 10 | 15 | 20 |
| H2(g) | 6.00 | 5.40 | 5.10 | 5.80 | 5.80 |
| CO2(g) | 2.00 | 1.80 | 1.70 | 1.60 | 1.60 |
| CH2=CH2(g) | 0 | 0.10 | 0.15 | 0.20 | 0.20 |
已知在10min时只改变了一个反应条件,用改变的条件可能是______。
④下列情况下能表明该反应达到平衡状态的是_____。
a.气体密度不变 b.混合气休的平均摩尔质量不变 c.消耗速率:2v(H2O)=v(CO2)
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
① 若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=______ [常温下K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11]。
② 欲用5L Na2CO3溶液将23.3 g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为_________。[已知:常温下Ksp(BaSO4)=1×10-7、Ksp(BaCO3)=2.5×10-6]。(忽略溶液体积积的变化)
高三化学填空题中等难度题查看答案及解析
(17分)CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物。工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气。
(1) 已知:CH4、H2和CO的燃烧热分别为890.3kJ/mol、285.8kJ/mol和283.0kJ/mol,且1mol液态水汽化时的能量变化为44.0kJ。写出甲烷与水蒸气在高温下反应制取合成气的热化学方程式 。
(2)在一定条件下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
|
物质 浓度 | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol·L—1 | 0.13 mol·L—1 | 0.1 mol·L—1 | 0.1 mol·L—1 | 0.09 mol·L—1 |
| H2 | 0 mol·L—1 | 0.2 mol·L—1 | 0.3 mol·L—1 | 0.3 mol·L—1 | 0.33 mol·L—1 |
①3—4min之间,化学平衡向___ ____反应方向移动(填“正”或“逆”)。
②3min时改变的反应条件是____________________(只填一种条件的改变)
(3)已知温度、压强、投料比X〔n(CH4)/n(H2O)〕对该反应的影响如图所示。
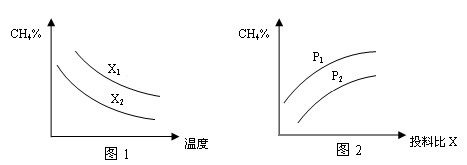
①图1中的两条曲线所示投料比的关系X1____X2(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:p1_______p2
(4)以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池
①放电时,正极的电极反应式_______________________________________
②设装置中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为8.96L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为 ____。
高三化学填空题困难题查看答案及解析