氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥(或单线桥)标出反应中电子转移的方向和数目。____________
反应中氧化剂是__________,被氧化的物质是______________。
高一化学填空题简单题
氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥(或单线桥)标出反应中电子转移的方向和数目。____________
反应中氧化剂是__________,被氧化的物质是______________。
高一化学填空题简单题
氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥(或单线桥)标出反应中电子转移的方向和数目。____________
反应中氧化剂是__________,被氧化的物质是______________。
高一化学填空题简单题查看答案及解析
实验室中可利用反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O来制取氯气。
(1)用双线桥(或单线桥)标出下列反应中电子转移的方向和数目:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O__________
(2)该反应中氧化剂是______,氧化产物是________。若有1 mol KMnO4参加反应,转移的电子的物质的量是______mol,被氧化的HCl的物质的量是________mol。
高一化学填空题简单题查看答案及解析
实验室中可利用反应来制取氯气。
(1)用双线桥(或单线桥)标出反应中电子转移的方向和数目_________。
(2)该反应中氧化剂是_____,氧化产物是________。
(3)若有1 mol KCl完全反应,则转移的电子的物质的量是_____mol,制得标准状况下氯气的体积为____ L。
高一化学综合题中等难度题查看答案及解析
(16分)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓) 2KCl + 2MnCl2 + 5Cl2↑ +8H2O
(1)用单线桥法标出电子转移的方向和数目。
(2)该反应中的氧化剂与还原剂物质的量之比是 。
(3)KMnO4的氧化性比Cl2的氧化性 (选填“强”或“弱”)。
(4)如反应中转移了2mol电子,则产生的Cl2在标准状况下体积为 L。
(5)某同学欲用KMnO4固体配制100 mL0.5mol.L-1的溶液。回答下列问题:
①配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、 、 。
②应用托盘天平称取KMnO4固体 g。
③不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小的是(请填序号) 。
A.加水定容时俯视刻度线
B.容量瓶内壁附有水珠而未干燥处理
C.颠倒摇匀后发现凹液面低于刻度线又加水补上
D.在溶解过程中有少量液体溅出烧杯外
高一化学填空题中等难度题查看答案及解析
实验室可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①请用“双线桥”标出电子转移的方向和数目;(2分)
②该反应中被氧化和未被氧化的HCl的物质的量之比是 _______。(1分)
高一化学填空题中等难度题查看答案及解析
实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法标出电子转移的方向和数目 ________。
(2)该反应中氧化剂与氧化产物物质的量之比是_____。
(3)由该反应判断, KMnO4 的氧化性比 Cl2 的氧化性(选填“强”或“弱”) ________。
(4)如反应中转移了 2mol 电子,则产生的 Cl2 在标准状况下体积为_____L 。
(5)某同学欲用 KMnO4 固体配制100mL 0.5mol/L 的溶液 。回答下列问题:
①配制 KMnO4 溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、_____、_____。
②下列对容量瓶及其使用方法的描述中正确的是(请填序号)_____。
A.容量瓶上标有容积、温度和刻线
B.容量瓶用蒸馏水洗净后,必须加热烘干
C.配制溶液时,把量好的 KMnO4 固体小心放入容量瓶中,加入蒸馏水到接近刻度线 1~2 cm 处,改 用胶头滴管加蒸馏水至刻度线
D.使用前要检查容量瓶是否漏水
③不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小的是_______(请填序 号)
A.加水定容时俯视刻度线 B.容量瓶水洗后有水残留
C.颠倒摇匀后发现凹液面低于刻度线又加水补上 D.在溶解过程中有少量液体溅出烧杯外
高一化学实验题中等难度题查看答案及解析
高一化学解答题中等难度题查看答案及解析
高一化学填空题中等难度题查看答案及解析
实验室经常用KMnO4与过量浓盐酸反应制备氯气,化学方程式如下:2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O。
(1)用单线桥标出电子转移的方向和数目:__________。
(2)将此反应改写为离子方程式:___________________。
(3)若31.6g KMnO4与过量浓盐酸充分反应,被氧化的HCl的物质的量为_____,在标准状况下生成的Cl 2的体积为____。
(4)用生成的氯气通入下面的装置来验证氯气的某些性质。
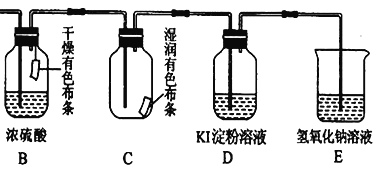
用离子方程式解释C中有色布条褪色的原因:______________,将B、C的顺序颠倒,可否达到原来的实验目的:______(填“可以”或“不可以”);D是用来检验氯气性质的实验,可观察到溶液由无色变为蓝色(I2单质遇淀粉变蓝色),请比较Cl2、I2 、KMnO4 的氧化性,由强到弱为_______。
高一化学综合题中等难度题查看答案及解析
(6分)完成下列反应的化学方程式或要求:
(1)写出电解饱和食盐水制氯气的化学反应方程式: 。
(2)写出电解熔融氯化镁制取金属镁的化学反应方程式: 。
(3)用双线桥标出下述反应中电子转移的方向和数目
C + 4HNO3(浓)
CO2↑ + 4NO2↑+2H2O
高一化学填空题中等难度题查看答案及解析