从结构角度分析,下列说法错误的是( )
A.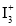 的立体构型为V形,中心原子的杂化方式为
的立体构型为V形,中心原子的杂化方式为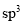
B.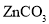 中,阴离子立体构型为平面三角形,C原子的杂化方式为
中,阴离子立体构型为平面三角形,C原子的杂化方式为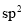
C.因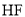 分子间存在氢键,所以
分子间存在氢键,所以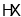 中其沸点最高
中其沸点最高
D.因金属性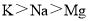 ,所以熔点:
,所以熔点: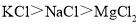
高三化学单选题困难题
从结构角度分析,下列说法错误的是( )
A.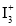 的立体构型为V形,中心原子的杂化方式为
的立体构型为V形,中心原子的杂化方式为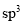
B.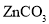 中,阴离子立体构型为平面三角形,C原子的杂化方式为
中,阴离子立体构型为平面三角形,C原子的杂化方式为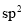
C.因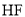 分子间存在氢键,所以
分子间存在氢键,所以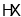 中其沸点最高
中其沸点最高
D.因金属性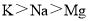 ,所以熔点:
,所以熔点: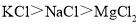
高三化学单选题困难题
从结构角度分析,下列说法错误的是( )
A.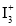 的立体构型为V形,中心原子的杂化方式为
的立体构型为V形,中心原子的杂化方式为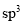
B.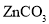 中,阴离子立体构型为平面三角形,C原子的杂化方式为
中,阴离子立体构型为平面三角形,C原子的杂化方式为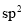
C.因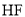 分子间存在氢键,所以
分子间存在氢键,所以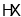 中其沸点最高
中其沸点最高
D.因金属性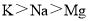 ,所以熔点:
,所以熔点: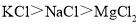
高三化学单选题困难题查看答案及解析
下列说法中错误的是( )
A.离子中心原子上的孤电子对数是1,立体构型为平面三角形
B.元素周期表第三周期主族元素中,简单离子半径最小的是
C.金刚石转化为石墨为放热反应,说明相同条件下石墨比金刚石稳定
D.、
都是非极性分子
高三化学单选题中等难度题查看答案及解析
氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下列关于氯化亚砜分子的几何构型和中心原子(S)采取杂化方式的说法正确的是
A. 三角锥形、sp3 B. V形、sp2 C. 平面三角形、sp2 D. 三角锥形、sp2
高三化学单选题中等难度题查看答案及解析
氯化亚砜()是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下列关于氯化亚砜分子的空间构型和中心原子(
)采取的杂化方式的判断正确的是( )
A.三角锥形、 B.
形、
C.平面三角形、 D.三角锥形、
高三化学单选题中等难度题查看答案及解析
关于甲醛(CH2O)分子,下列说法不正确的是 ( )
①分子中碳原子采用。 SP2杂化; ②分子中所有原子处于同一平面上;
③分子中每个原子都达到 8 电子稳定结构;④分子的立体构型为四面体
A.① ② B.② ③ C.③ ④ D.① ④
高三化学选择题中等难度题查看答案及解析
下列说法正确的是 ( )
A.某微粒空间构型为平面三角形,则中心原子一定是sp2杂化
B.某微粒空间构型为V形,则中心原子一定有孤电子对
C.某微粒空间构型为三角锥形,则该微粒一定是极性分子
D.某微粒空间构型为正四面体,则键角一定是109°28’
高三化学选择题中等难度题查看答案及解析
关于原子轨道的说法正确的是
A.凡是中心原子采取sp3杂化轨道成键的分子立体构型都是正四面体
B.CH4中的sp3杂化轨道是4个H原子的1s 轨道和C原子的2p轨道混合形成
C.sp3杂化轨道是由同一原子中能量相近的s 和p轨道混合形成的一组新轨道
D.凡AB3型的共价化合物,中心原子A均采用sp3杂化轨道成键
高三化学选择题简单题查看答案及解析
氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子构型为平面三角形,则其阳离子的构型和阳离子中氮的杂化方式为
A.直线 sp杂化 B.V型 sp2杂化
C.三角锥形 sp3杂化 D.平面三角形 sp2杂化
高三化学选择题中等难度题查看答案及解析
下列描述正确的是
A.的空间构型为平面三角形
B.和
的中心原子均为
杂化
C.分子中
键与
键的数目比为1:1
D.中有6对相同的成键电子对
高三化学单选题中等难度题查看答案及解析
下列描述中正确的是 ( )
A.CS2为V形的极性分子
B.ClO3—的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4的中心原子为sp3杂化,SO32—的中心原子为sp2杂化
高三化学选择题中等难度题查看答案及解析