-
四种短周期元素的相关信息如下表所示:
元素
相 关 信 息
X
它存在多种同素异形体,可用于制作钻头、电极和纳米材料
Y
最外层电子数是内层电子数的3倍
Z
第三周期中最高价氧化物的水化物碱性最强
W
与X元素处于同一主族,工业上常用X的单质还原W的氧化物制取W单质
下列说法正确的是
A.原子半径:W>Z>Y>X
B.Y、Z两种元素只能形成化合物Z2Y
C.最低价气态氢化物的热稳定性:W>X
D.最高价氧化物对应水化物的酸性:X>W
高三化学选择题中等难度题查看答案及解析
-
四种短周期元素的相关信息如下表所示:
元素
相关信息
X
它存在多种同素异形体,可用于制作钻头、电极和纳米材料
Y
最外层电子数是内层电子数的3 倍
Z
第三周期中最高价氧化物的水化物碱性最强
W
与X 元素处于同一主族,工业上常用X 的单质还原W的氧化物制取W单质
下列说法正确的是
A.原子半径: W>Z>Y>X B.最高价氧化物对应水化物的酸性: X>W
C.最低价气态氢化物的热稳定性: W>X D.Y、Z 两种元素只能形成化合物Z2Y
高三化学单选题中等难度题查看答案及解析
-
(14分)X、Y、及W是短周期中的四种元素,其原子序数依次增大。相关信息如下表
元素
相关信息
X
具有多种同素异形体,形成的化合物种类繁多
Y
短周期主族元素中原子半径最大
Z
位于元素周期表金属与非金属元素的分界线上,最高化合价为十4
W
富集在海水中的元素,它的某些化合物常用作消毒刹
(1)Z元素基态原子的核外电子排布式为 ,其未成对的电子数目为 。
(2)Y位于元素周期表中第 周期,第 族,四种元素的电负性由大到水的顺序是 (写元素符号)。
(3)氢化物中X-H和W-H的化学键极性较强的是 ,耐磨材料(XY)和单质y 熔点较高的
是 (均用元素符号表示)。
(4)已知400 ℃时,HW 可被氧气催化氧化生成W 的单质,从而实现化更生产上W的循环利用。若断开1mo1H一W化学键,该反应放热28.9KJ,试写出相应的热化学方程式: 。
高三化学填空题困难题查看答案及解析
-
(14分)X、Y、Z、W、M是元素周期表中原子序数依次增大的五种元素,其相关信息如下表:
元素
相关信息
X
元素周期表中核电荷数最小的元素
Y
Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质
Z
Z是大气中含量多的元素,其某些氧化物为大气中常见的污染物
W
W是地壳中含量最高的金属元素
M
常见金属,单质呈紫红色
(1)W位于元素周期表第 周期第 族;W的简单离子半径比Z的简单离子半径 (填“大”或“小”)。
(2)Z原子的第一电离能比氧原子的 (填“大”或“小”);M的基态原子价电子排布式是
(3)X与Y可形成多种化合物,其中常用来切割或焊接金属的气体分子中σ键和π键之比是 ,空间构型是
(4)X与Z形成的最简单化合物用途非常广泛,试列举两种用途: 、 ;该化合物具有较强的还原性,加热时能将M的氧化物MO还原,写出该反应的化学方程式:____。
(5)可用YX4还原ZOx以消除其污染。已知:
YX4 (g) +4ZO2 (g)=4ZO(g)+YO2(g)+2X2O(g) △H= - 574 kJ·mol-1
YX4 (g)+4ZO(g)=2Z2 (g)十YO2 (g) +2X2O(g) △H = - 1160 kJ·mol-1
试写出用YX4还原ZO2至Z2的热化学方程式:____。
高三化学填空题困难题查看答案及解析
-
X、Y、Z、W是短周期中常见元素,其相关信息如下表:
元素
相关信息
X
X元素形成的一种同素异形体是天然晶体中硬度最大的单质
Y
常温常压下,Y单质是淡黄色固体,用于制造黑火药
Z
Z的基态原子核外有3个能级上有电子,且有3个单电子
W
W元素形成的双原子分子,常温下为黄绿色气体,一种常见工业原料
(1)W元素位于元素周期表中第________周期________族,与Y同主族且位于第四周期元素的基态原子核外电子排布式为________。
(2)XY2分子中含有的σ键和π键个数比为________,在相同条件下XY2与XO2相比,熔点较高的是________(填化学式)。结合相关理论解释Z所在族的元素第一电离能大于同周期后一族元素的原因:________。
(3)Y、W元素形成的化合物Y2W2和过量氢化物ZH3在无水条件下反应生成Y4Z4、单质Y8和一种可以作为化肥的物质,请写出相应化学方程式:________。
(4)已知:①lmolY(s)转化为气态Y(g) \吸收能量280 kJ;
②2XO(g)+O2(g)= 2XO2(g) ΔH=-566.0KJ/mol;
③Y(s)+O2(g)=YO2(g) ΔH=-299.0KJ/mol;一定条件下,可以利用X的氧化物XO和Y的氧化物YO2生成Y(g)单质和X的氧化物而达到消除污染目的。请写出该反应的热化学方程式:________。
高三化学填空题极难题查看答案及解析
-
X、Y、Z、W、R、M 六种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,相关信息如下:
元素
相关信息
X
其单质为固体,常作电极材料
Y
原子核外有6种不同运动状态的电子
Z
非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同
W
主族元素,与Z原子的价电子数相同
R
价层电子排布为3d64s2
M
ⅠB族,其单质常用作导线
请回答下列问题(答题时,X、Y、Z、W、R、M用所对应的元素符号表示):
(1)X的单质与Z的单质反应的产物为_____________。(填化学式)。
(2)Z、W相比,第一电离能较大的是_____________,M2+的核外电子排布式为_____________。
(3)M2Z的熔点比M2W 的_____________(填“高”或“低”),请解释原因______________________。
(4)Y和Z形成的化合物YZ2的VSEPR模型为__________,其中Y原子 的杂化轨道类型为____________; N3-和YZ2互为等电子体,则N3-的结构式为_____________。
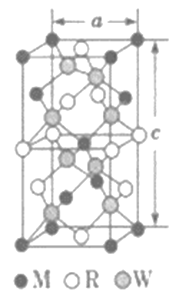
(5)MRW2的晶胞如图所示,晶胞参数a=0.524 nm,c=1.032 nm; MRW2的晶胞中每个M 原子与_________个W 原子相连,晶体密度ρ=________g·cm-3 (只要求列算式,不必计算出数值,NA=6.02×1023mol-1)。
高三化学推断题中等难度题查看答案及解析
-
X、Y、Z、W、R、M 六种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,相关信息如下:
元素
相关信息
X
其单质为固体,常作电极材料
Y
原子核外有6种不同运动状态的电子
Z
非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同
W
主族元素,与Z原子的价电子数相同
R
价层电子排布为3d64s2
M
ⅠB族,其单质常用作导线
请回答下列问题(答题时,X、Y、Z、W、R、M用所对应的元素符号表示):
(1)X的单质与Z的单质反应的产物为_____________。(填化学式)。
(2)Z、W相比,第一电离能较大的是_____________,M2+的核外电子排布式为_____________。
(3)M2Z的熔点比M2W 的_____________(填“高”或“低”),请解释原因______________________。
(4)Y和Z形成的化合物YZ2的VSEPR模型为__________,其中Y原子 的杂化轨道类型为____________; N3-和YZ2互为等电子体,则N3-的结构式为_____________。
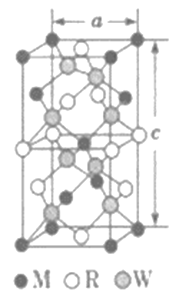
(5)MRW2的晶胞如图所示,晶胞参数a=0.524 nm,c=1.032 nm; MRW2的晶胞中每个M 原子与_________个W 原子相连,晶体密度ρ=________g·cm-3 (只要求列算式,不必计算出数值,NA=6.02×1023mol-1)。
【答案】 Li2O O [Ar]3d9 或1s22s22p63s23p63d9 高 O2-半径比S2-半径小,Cu2O 比Cu2S 的晶格能大,所以Cu2O的熔点高 直线形 sp杂化 [N=N=N]- 4
【解析】X、Y、Z、W、R、M六种元素,位于元素周期表的前四周期,它们的核电荷数依次增大。Y的原子核外有6个不同运动状态的电子,Y为C元素;X的单质为固体,常用作电极材料,X只能为Li元素;Z 是非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同,Z的电子排布式为1s22s22p4,为O元素;W是主族元素,与Z原子的价电子数相同 ,W为S元素;R 的价层电子排布式为3d64s2,R为Fe元素;M位于第IB族,其被称作“电器工业的主角”,为Cu元素。
(1)锂与氧气反应生成氧化锂,故答案为:Li2O;
(2)同一主族,从上到下,第一电离能逐渐减小,O和S元素相比,第一电离能较大的是O,Cu2+的核外电子排布式为[Ar]3d9,故答案为:O;[Ar]3d9;
(3)氧离子半径比硫离子半径小,Cu2O比Cu2S的晶格能大,所以Cu2O熔点高,故答案为:高;氧离子半径比硫离子半径小,Cu2O比Cu2S的晶格能大,所以Cu2O熔点高;
(4)CO2中的C采用sp杂化,VSEPR 模型为直线型;N3-和CO2是等电子体,则N3-的结构式为[N=N=N]-,故答案为:直线型; sp;[N=N=N]-;
(5)由面心上Cu与2个S相连,晶胞中每个Cu原子与4个S相连;8个S均在体内,由化学式为CuFeS2,则含晶胞质量为
,晶胞参数a=0.524nm,c=1.032nm,体积为(0.524×10-7cm)2×1.032×10-7cm,ρ=
=
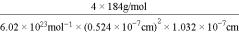 =
=g•cm-3,故答案为:4;
。
点睛:本题考查晶胞计算及杂化等,为高考常见题型和高频考点,侧重于学生的分析能力的考查,把握物质结构与性质、晶胞结构及计算等为解答该题的关键。本题的难点是晶胞的计算。
【题型】推断题
【结束】
12芳香烃A是基本有机化工原料,由A制备高分子E 和医药中间体K的合成路线(部分反应条件略去)如图所示:
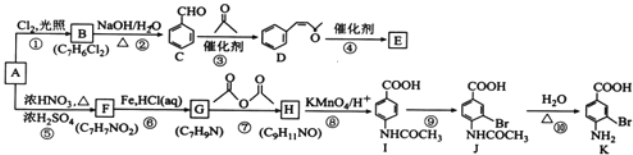
已知:
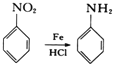 ;有机物分子中,同一个碳原子上连接有两个羟基时不稳定,会自动脱水。
;有机物分子中,同一个碳原子上连接有两个羟基时不稳定,会自动脱水。回答下列问题:
(1)A的名称是_____________。K含有官能团的名称是__________________。
(2)反应⑦的作用是____________________________,⑩ 的反应类型是____________________________。
(3)写出反应②的化学方程式:____________________________________________________________。
(4)D 分子中最多有_____________个原子共平面。E 的结构简式为_____________。
(5)1molD 与1molH2的加成产物同时满足下列条件的同分异构体有_____________种。
①苯环上只有四种不同化学环境的氢原子;
②能与FeCl3发生显色反应;
③分子中只存在一个环不含其它环状结构。
(6)将由D为起始原料制备
的合成路线补充完整。
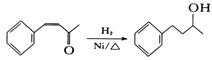 _________________________(无机试剂及溶剂任选)。合成路线流程图示例如下: CH3CHO
_________________________(无机试剂及溶剂任选)。合成路线流程图示例如下: CH3CHOCH3COOH
 CH3COOCH2CH3
CH3COOCH2CH3高三化学综合题中等难度题查看答案及解析
-
(14分)有A、B、C、D、E、F、G七种前四周期元素,原子序数依次增大,其相关信息如下表:
元素
元素的相关信息
A
存在多种核素,其中一种核素没有中子
B
核外电子排布式三个能级上的电子数相同
C
其第一电离能比同周期相邻元素的第一电离能都大
D
最外层电子数是内层电子数三倍的元素
E
单质或其化合物在火焰灼烧时,火焰呈黄色
F
位于第三周期ⅦA族
G
未成对电子数最多的副族元素
(1)G元素的价层电子排布式为 。
(2)D、E、F三种元素的简单离子的离子半径由大到小的顺序是 (用微粒符号表示)。
(3)B、C、F三种元素的最高价氧化物的水化物的酸性最强的是 (写名称)。
(4)由上述两种元素组成的与O3互为等电子体的负一价阴离子的化学式为 。
(5)由B、C、E三种元素的三原子组成的含σ键和π键的离子化合物的电子式 。
(6)由A、B、D三种元素组成的有两种官能团的能形成分子内氢键的芳香族化合物的结构简式为 (任写一种)。
(7)如图所示装置,两玻璃管中盛满滴有酚酞溶液的EF饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:C(Ⅱ)的电极反应式是 。
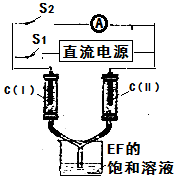
高三化学填空题困难题查看答案及解析
-
X、Y、Z、W、R、M六种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素
相关信息
X
其单质为固体,常用作电极材料
Y
原子核外有6个不同运动状态的电子
Z
非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同
W
主族元素,与Z原子的价电子数相同
R
价层电子排布式为3d64s2
M
IB族,其被称作“电器工业的主角”
请回答下列问题(X、Y、Z、W、R、M用所对应的元素符号表示):
(1)元素X的单质与元素Z的单质反应的产物为________(填化学式)。
(2)Z、W元素相比,第一电离能较大的是______,M2+的核外电子排布式为_______。
(3)M2Z的熔点比M2W的_____(填“高”或“低”) ,请解释原因______。
(4)Y和Z形成的简单化合物YZ2的VSEPR 模型名称为_______,其中Y原子轨道的杂化类型为_______;N3-和YZ2是等电子体,则N3-的结构式为_______。
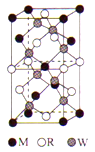
(5)MRW2的晶胞如图所示,晶胞参数a=0.524nm、c=1.032nm;MRW2的晶胞中每个M原子与___
个W原子相连,晶体密度ρ=______g/cm3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA=6.02×1023mol-1)。
高三化学推断题中等难度题查看答案及解析
-
A、B、C、D、E均为短周期元素,且原子序数依次增大;A的主族序数、周期数、原子序数均相同;B为非金属元素,其单质有多种同素异形体,其中一种可作电极材料;C是植物生长所需的主要元素之一;D和A可形成化合物
和
,且
是最常见的溶剂;E原子次外层电子数等于其它层电子数之和,则:
的离子结构示意图为 ______ ,B、C、D、E与A形成的化合物中稳定性最强的是 ______
填化学式
.
在加热和Cu作催化剂时,化合物
与
反应生成其中一种产物是
的化学方程式为 ______ .
五种元素中,含同一元素的各类物质能实现下列转化的有
图
______
填元素符号
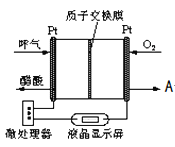
图所示是一种酸性燃料电池
检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.则该电池的负极反应为 ______
出口处的物质 ______ .
高三化学推断题困难题查看答案及解析