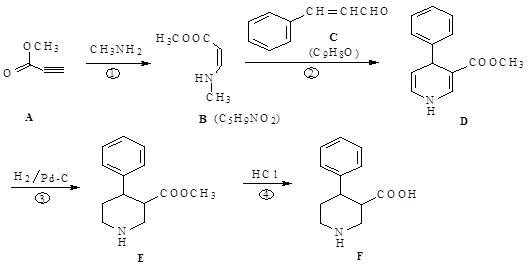-
丙炔酸甲酯(CH≡C-COOCH3 )是一种重要的有机化工原料,沸点为103℃。实验室制备少量丙炔酸甲酯的反应为:CH≡C-COOH+CH3OH CH≡C-COOCH3+H2O。实验步骤如下:
CH≡C-COOCH3+H2O。实验步骤如下:
步骤1:在反应瓶中加入14 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌加热回流一段时间;
步骤2:蒸出过量的甲醇(装置见图);

步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤,分离出有机相;
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得7.56g丙炔酸甲酯。
(1)步骤1中,加入过量甲醇的目的是________。
(2)步骤2中,图中所示的装置中仪器A的名称是________,自来水从________(填“e”或“f”)进入该仪器;加入碎瓷片的目的是________。
(3)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是________;分离出有机相的操作名称为________。
(4)步骤4中,蒸馏时不能用水浴加热的原因是________。
(5)丙炔酸甲酯的产率为________。
-
I.丙炔酸甲酯(CH≡C—COOCH3)是一种重要的有机化工原料,沸点为103~105℃。实验室制备少量丙炔酸甲酯的反应为CH≡C—COOH+CH3OH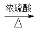 CH≡C—COOCH3+H2O
CH≡C—COOCH3+H2O
实验步骤如下:
步骤1:在反应瓶中,加入14g丙炔酸、50mL甲醇和2mL浓硫酸,搅拌,加热回流一段时间。
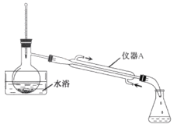
步骤2:蒸出过量的甲醇(装置见下图)。
步骤3:反应液冷却后,依次用饱和NaCl液、5%Na2CO3液、水洗涤。分离出有机相。
步骤4:有机相经无水 Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯。
(1)步骤l中,加入过量甲醇的目的是__________。
(2)步骤2中,图中所示的装置中仪器A的名称是________。
(3)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是__;分离出有机相的操作名称为___。
(4)步骤4中,蒸馏时不能用水浴加热的原因是______。
II.环己烯含量的测定
在一定条件下,向ag环己烯样品中加 入过量的bmolBr2,与环己烯充分反应后,剩余的Br2与足量KI作用生成I2,用cmol•L-1的Na2S2O3标准溶液滴定 ,终点时消耗Na2S2O3标准溶液vmL(以上数据均已扣除干扰因素)。测定过程中,发生的反应如下:
①Br2+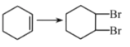
②Br2+2KI===I2+2KBr
③I2+2Na2S2O3===2NaI+Na2S4O6
(5)滴定所用的指示剂为_______。样品中环己烯的质量分数为________。
(6)下列情况会导致测定结果偏低的是________。
a.样品中含有苯酚杂质 b.在测定过程中部分环己烯挥发 c.Na2S2O3标准溶液部分被氧化
-
丙炔酸甲酯(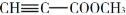 )是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为 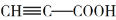 +CH3OH
+CH3OH
 +H2O
+H2O
实验步骤如下:
步骤1:在反应瓶中,加入14 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯。
(1)步骤1中,加入过量甲醇的目的是________。
(2)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是_______;分离出有机相的操作名称为__________。
(3)步骤4中,蒸馏时不能用水浴加热的原因是_________。
-
(每空2分,共10分)物质F是合成多种手性药物和生物活性物质的重要中间体,其合成路线如下:
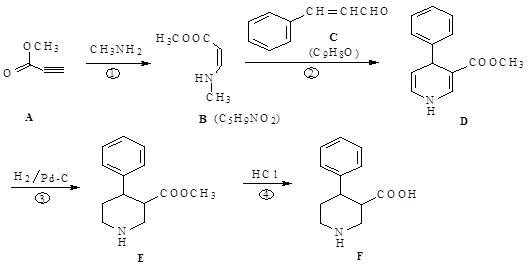
(1)反应①的类型为,反应④的类型为。
(2)物质A聚合可得聚丙炔酸甲酯,其结构简式为________。
(3)物质C的俗名为肉桂醛,写出其同时满足下列条件的一种同分异构体的结构简式 ________。
①能与氯化铁溶液显紫色;②苯环上有两个取代基;③分子的核磁共振氢谱有4个峰。
(4)若部分C被氧化为肉桂酸,反应②将产生副产物(分子式为C14H15NO3),写出其结构简式。
-
(每空2分,共10分)物质F是合成多种手性药物和生物活性物质的重要中间体,其合成路线如下:

(1)反应①的类型为,反应④的类型为。
(2)物质A聚合可得聚丙炔酸甲酯,其结构简式为________。
(3)物质C的俗名为肉桂醛,写出其同时满足下列条件的一种同分异构体的结构简式 ________。
①能与氯化铁溶液显紫色;②苯环上有两个取代基;③分子的核磁共振氢谱有4个峰。
(4)若部分C被氧化为肉桂酸,反应②将产生副产物(分子式为C14H15NO3),写出其结构简式。
-
“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应物中原子全部转化为欲制的产物,即原子的利用率为 100%。在用丙炔合成甲基丙烯酸甲酯 CH2=C(CH3)—COOCH3 的过程中,欲使原子利用率达到最高,还需要其他的反应物是( )
A. CH3OH 和 H2 B. CO2 和 H2O C. H2 和 CO2 D. CO 和 CH3OH
-
甲酸甲酯是重要有机化工原料,制备反应为CH3OH(g)+CO(g)  HCOOCH3(g) ΔH<0;相同时间内,在容积固定的密闭容器中,使反应在不同温度下进行(起始投料比均
HCOOCH3(g) ΔH<0;相同时间内,在容积固定的密闭容器中,使反应在不同温度下进行(起始投料比均 为1),相同时间内测得CO的转化率随温度变化的曲线如下图。下列说法中不正确的是
为1),相同时间内测得CO的转化率随温度变化的曲线如下图。下列说法中不正确的是
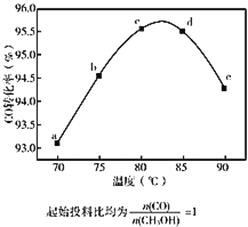
A. 70~80℃,CO转化率随温度升高而增大,其原因是升高温度反应速率增大
B. 85~90℃,CO转化率随温度升高而降低,其原因可能是升高温度平衡逆向移动
C. d点和e点的平衡常数:Kd < Ke
D. a点对应的CO的转化率与CH3OH的转化率相同
-
苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成。有关物质的物理性质、实验装置如下所示:
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
实验一:制取苯甲酸甲酯:在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验。
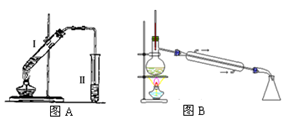
(1)苯甲酸与甲醇反应的化学方程式为______________________。
(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和沸石外还需要加入一定量浓硫酸,浓硫酸的作用是 。
(3)实验室制取乙酸乙酯时,为了除去乙酸乙酯中混有的乙酸所用试剂为 。
实验二:提纯苯甲酸甲酯:该实验要先把图A中制备的苯甲酸甲酯水洗提纯,再利用图B装置进行蒸馏提纯
(4)水洗提纯时所进行的操作为(填操作名称) 。
(5)用图B装置进行蒸馏提纯时,当温度计显示 时,可用锥形瓶收集苯甲酸甲酯。
-
苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成.有关物质的物理性质、实验装置如下所示:
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
实验一:制取苯甲酸甲酯
在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验.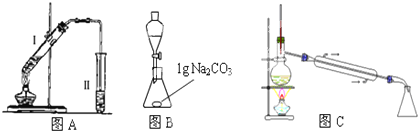
(1)苯甲酸与甲醇反应的化学方程式为______.
(2)中学实验室中制取乙酸乙酯时为了提高酯的产率可以采取的措施有______.
实验二:提纯苯甲酸甲酯
该实验要先利用图B装置把图A中制备的苯甲酸甲酯水洗提纯,再利用图C装置进行蒸馏提纯
(3)用图B装置进行水洗提纯时,B装置中固体Na2CO3作用是______.
(4)用图C装置进行蒸馏提纯时,当温度计显示______时,可用锥形瓶收集苯甲酸甲酯.
-
苯甲酸甲酯是重要的化工原料,某化学兴趣小组仿照实验室制乙酸乙酯的原理以苯甲酸(C6H5COOH)和甲醇为原料制备苯甲酸甲酯。有关数据如下:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度(g/cm3) | 水溶性 |
| 苯甲酸 | 122 | 122.4 | 249 | 1.2659 | 微溶 |
| 甲醇 | 32 | -97 | 64.6 | 0.792 | 互溶 |
| 苯甲酸甲酯 | 136 | -12.3 | 196.6 | 1.0888 | 不溶 |
I.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,在圆底烧瓶上连接冷凝回流装置后,小心加热2小时,得苯甲酸甲酯粗产品。
回答下列问题:
(1)该反应的化学方程式为__________,该反应的原子利用率是_______。
己知:原子利用率=(预期产物的总质量/全部反应物的总质量)×100%
(2)实验中,应选择(如下图)_____(填序号)作为冷凝回流装置,该仪器的名称为______。
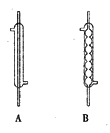
(3)使用过量甲醇的原因是__________。
Ⅱ.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制。
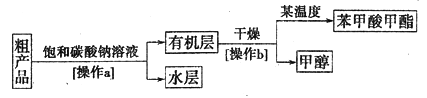
(4)饱和碳酸钠溶液的作用是________,操作a的名称为________。
(5)由于有机层和水层的密度比较接近,兴趣小组的同学无法直接判断有机层在上层还是下层,请你设计简单易行的方案,简述实验方法,可能的现象及结论__________。
(6)该实验中制得苯甲酸甲酯8.30g,则苯甲酸甲酯的产率为________。
 CH≡C—COOCH3+H2O
CH≡C—COOCH3+H2O


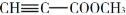 )是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为 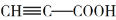 +CH3OH
+CH3OH
 +H2O
+H2O