-
重铬酸钾又名红矾钾,是化学实验室中的一种重要分析试剂。工业上以铬酸钾为原料,采用电化学制备重铬酸钾。制备装置如下图所示:
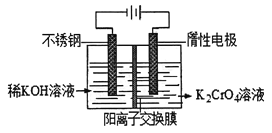
制备原理:2CrO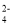 (黄色)+2H+⇌Cr2O
(黄色)+2H+⇌Cr2O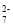 (橙色)+H2O
(橙色)+H2O
(1)通电后阳极室产生的现象为_____________,电极反应式是__________。
(2)该制备过程总反应的离子方程式可表示为4CrO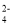 +4H2O=2Cr2O
+4H2O=2Cr2O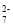 +4OH-+2H2↑+O2↑,若实验开始时在右室中加入38.8 g K2CrO4,t分钟后测得右室中K与Cr的物质的量之比为3:2,则溶液中K2CrO4和K2Cr2O7的物质的量之比为________;该过程中反应转移的电子数目为___________;此时阳极室与阴极室溶液质量变化之差(△m阴极室-△m 阳极室)为____g。
+4OH-+2H2↑+O2↑,若实验开始时在右室中加入38.8 g K2CrO4,t分钟后测得右室中K与Cr的物质的量之比为3:2,则溶液中K2CrO4和K2Cr2O7的物质的量之比为________;该过程中反应转移的电子数目为___________;此时阳极室与阴极室溶液质量变化之差(△m阴极室-△m 阳极室)为____g。
-
红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。
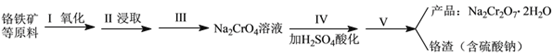
(1)步骤I中反应的化学方程式为:4FeO·Cr2O3(s)+8Na2CO3(s)+7O2 (g) 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) △H<0该反应的化学平衡常数的表达式为__________________________。
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) △H<0该反应的化学平衡常数的表达式为__________________________。
(2)在常温下该反应速度极慢,下列措施中能使反应速率增大的是_____________________________ 。
a.升高温度 b.及时转移生成CO2 c.将原料粉碎 d.增加纯碱的用量
(3)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是__________________________、____________________________。
(4)步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是_____________________________________。
(5)步骤Ⅳ酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:_________________。
-
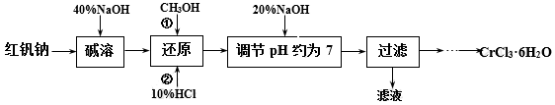
氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室中以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O的流程如下:
 已知:①Cr2O72-+H2O
已知:①Cr2O72-+H2O 2CrO42-+2H+;
2CrO42-+2H+;
②CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
③甲醇,无色液体,有毒,沸点64.7,易燃。
请回答:
(1)碱溶的目的是____,所加40%NaOH不宜过量太多的原因是____。
(2)还原时先加入过量CH3OH再加入10%HCl,生成CO2,该反应的离子方程式为____。
(3)使用下列用品来测定溶液的pH,合理的是____(填字母)。
A.pH计 B.pH试纸 C.酚酞溶液
(4)使用下图装置从滤液中分离出CH3OH。
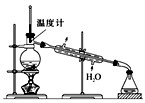
①该装置中存在的错误是____。
②在改正后的装置中,在仪器A中加入沸石,再加入滤液,蒸馏,收集蒸馏出的CH3OH循环使用。有的同学认为,该过程中需要加入CaO,防止水随CH3OH一起蒸出,你认为是否有必要并说明理由:____。
(5)请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得固体____,____,冷却结晶,过滤,____,低温干燥,得到CrCl3·6H2O。
(实验中可供选择的试剂:盐酸、硫酸、蒸馏水、乙醇、乙醚)
-
氨气是一种重要的工业原料,可以制备如下图所示的一系列物质(部分产物未标出)

(1)线路Ⅰ为硝酸的制备
写出反应①的化学方程式________;反应②中氧化剂与还原剂的物质的量之比为_______,工业尾气中的氮氧化物常采用碱液法吸收,若NO与NO2按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_______。
(2)路线为Ⅱ纯碱的制备
写出反应③的化学方程式________,最终得到的纯碱中可能含有NaCl,检验是否存在NaCl的实验方案是________
(3)路线Ⅲ为尿素的制备
写出合成尿素的化学方程式________
(4)实验室中需要少量氨气,写出制备氨气的化学方程式________
-
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作。回答下列问题:

(1)试剂Ⅰ的化学式为_______。
(2)试剂Ⅱ的化学式为_______,②中加入试剂Ⅱ的目的是除去A中的____,检验该离子已经除尽的方法是________________________________________________________。
(3)③中发生反应的化学方程式为_________________________________________________。
(4)由E得到KCl晶体的实验操作是_______________。
-
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。

(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是________;发生装置B应选择以下三种装置中的________(选填序号)。
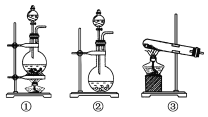
(2)D装置中主要反应的离子方程式为_______________________
(3)为验证通入D装置中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液 ⑤酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有________(选填一个序号)试剂的试管内,再加入________(选填一个序号)试剂。发生的现象是______________。若SO2过量,取适量D中溶液滴加至盛有________(选填一个序号)试剂的试管内,发生的现象是_________。
-
研究氮的循环和转化对生产、生活有重要的价值。
I.(1)写出实验室制备氨气的化学方程式________ 。
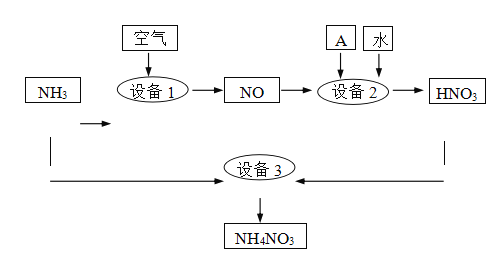
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。
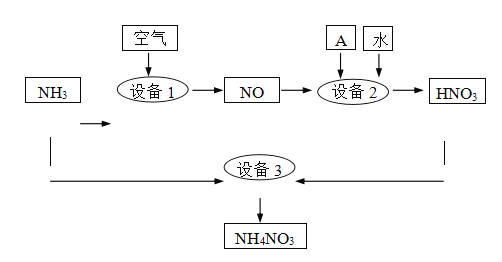
(2)设备1、3中发生反应的化学方程式分别是______、 ________ 。设备2中通入的物质A是________。
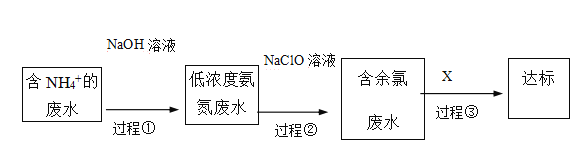
III.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH4+和NH3•H2O的形式存在。某工厂处理氨氮废水的流程如下:
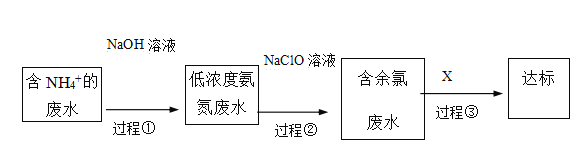
(3)过程①的目的是将NH4+转化为NH3,并通过鼓入大量空气将氨气吹出,写出NH4+转化为NH3的离子方程式________ 。
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为___、_______。
(5)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的(填序号)_________。
a.KOH b.Na2SO3 c.KMnO4 D.NaCl
写出其中一个反应的离子方程式__________ 。
-
研究氮的循环和转化对生产、生活有重要的价值。
I.(1)写出实验室制备氨气的化学方程式________ 。
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。
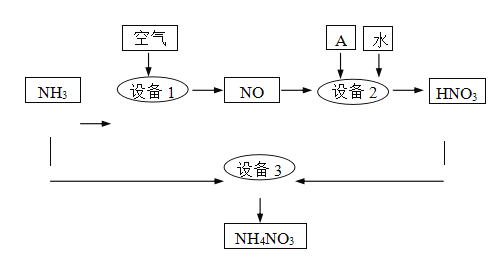
(2)设备1、3中发生反应的化学方程式分别是______、 ________ 。设备2中通入的物质A是________。
III.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH4+和NH3•H2O的形式存在。某工厂处理氨氮废水的流程如下:
(3)过程①的目的是将NH4+转化为NH3,并通过鼓入大量空气将氨气吹出,写出NH4+转化为NH3的离子方程式________ 。
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为___、_______。
(5)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的(填序号)_________。
a.KOH b.Na2SO3 c.KMnO4 D.NaCl
写出其中一个反应的离子方程式__________ 。
-
研究氮的循环和转化对生产、生活有重要的价值。
I.(1)写出实验室制备氨气的化学方程式________ 。
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。
(2)设备1、3中发生反应的化学方程式分别是______、 ________ 。设备2中通入的物质A是________。
III.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH4+和NH3•H2O的形式存在。某工厂处理氨氮废水的流程如下:
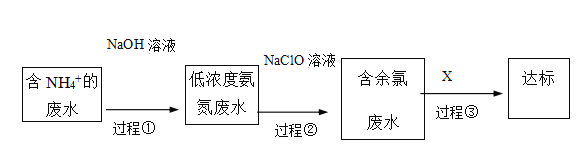
(3)过程①的目的是将NH4+转化为NH3,并通过鼓入大量空气将氨气吹出,写出NH4+转化为NH3的离子方程式________ 。
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为___、_______。
(5)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的(填序号)_________。
a.KOH b.Na2SO3 c.KMnO4 D.NaCl
写出其中一个反应的离子方程式__________ 。
-
环己烯是合成赖氨酸、环己酮、苯酚等的重要原料,也常用作石油萃取剂及高辛烷值汽油稳定剂。
制备环己烯的反应原理:主反应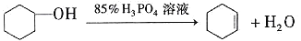 ;副反应
;副反应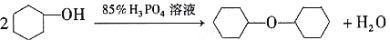
制备环己烯的实验装置图如下:(夹持装置及加热装置已省略)
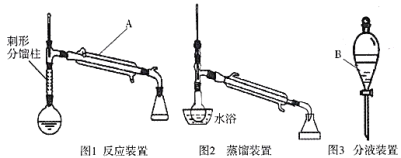
相应的实验流程如下图所示:
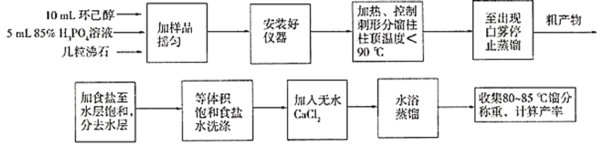
相关物质沸点、密度、溶解性如下:
| 沸点/℃ | 密度/( ) ) | 水中溶解性 |
| 环己醇 | 161 | 0.962 4 | 可溶于水 |
| 环己烯 | 83 | 0.811 | 不溶于水 |
| 85% 溶液 溶液 | | 1.69 | 易溶于水 |
| 环己烯与水形成的共沸物(含水10%) | 70.8 | | |
| 环己醇与水形成的共沸物(含水80%) | 97.8 | | |
回答下列问题:
(1)实验中不用浓硫酸,而用85% 溶液,说明理由________________(写出一条即可)。
溶液,说明理由________________(写出一条即可)。
(2)向粗产物环己烯中加入食盐使水层饱和的目的是_____________;水浴蒸馏前加入无水氯化钙的目的是___________________________.
(3)仪器A、B的名称分别是________________________。
(4)蒸馏提纯时用到水浴加热的方法,其优点是______________(写出两条即可)。
(5)文献资料要求本实验的反应温度应不超过90℃,其原因是_____________________。
(6)本实验最终得环己烯纯品2.75g,环己烯的产率为__________________%。

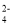 (黄色)+2H+⇌Cr2O
(黄色)+2H+⇌Cr2O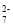 (橙色)+H2O
(橙色)+H2O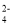 +4H2O=2Cr2O
+4H2O=2Cr2O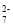 +4OH-+2H2↑+O2↑,若实验开始时在右室中加入38.8 g K2CrO4,t分钟后测得右室中K与Cr的物质的量之比为3:2,则溶液中K2CrO4和K2Cr2O7的物质的量之比为________;该过程中反应转移的电子数目为___________;此时阳极室与阴极室溶液质量变化之差(△m阴极室-△m 阳极室)为____g。
+4OH-+2H2↑+O2↑,若实验开始时在右室中加入38.8 g K2CrO4,t分钟后测得右室中K与Cr的物质的量之比为3:2,则溶液中K2CrO4和K2Cr2O7的物质的量之比为________;该过程中反应转移的电子数目为___________;此时阳极室与阴极室溶液质量变化之差(△m阴极室-△m 阳极室)为____g。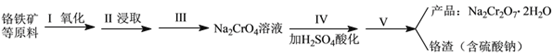
 已知:①Cr2O72-+H2O
已知:①Cr2O72-+H2O










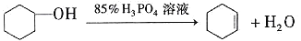 ;副反应
;副反应

