为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.下列叙述中错误的是( )

A.V=2240 B.n=0.02 C.原混合物中FeSO4的质量分数约为89% D.m=0.6
高三化学选择题困难题
为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.下列叙述中错误的是( )

A.V=2240 B.n=0.02 C.原混合物中FeSO4的质量分数约为89% D.m=0.6
高三化学选择题困难题
为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.下列叙述中错误的是( )

A.V=2240 B.n=0.02 C.原混合物中FeSO4的质量分数约为89% D.m=0.6
高三化学选择题困难题查看答案及解析
为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程。
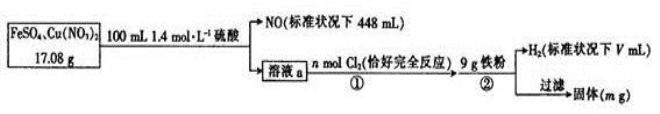 下列叙述中错误的是
下列叙述中错误的是
A.n = 0.02
B.V = 2240
C.原混合物中FeSO4的质量分数约为89%
D.m = 3.2
高三化学选择题困难题查看答案及解析
为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程:
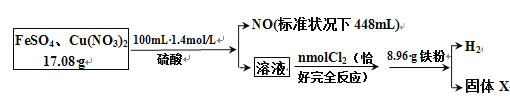
通过计算得出:
(1)原混合物中FeSO4的质量分数约为_______。
(2)通入的 n(Cl2) =________ mol。
(3)生成的H2在标准状况下的体积是________mL。
(4)固体X质量是________g。
高三化学综合题中等难度题查看答案及解析
碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。
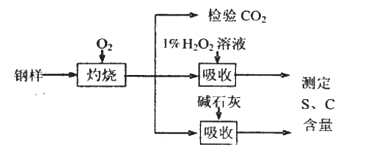
(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液 b.澄清石灰水 c.饱和小苏打溶液 d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000 mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如下图),碱石灰增重0.614 g。
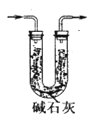
①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________(填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
高三化学填空题中等难度题查看答案及解析
碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。

(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液 b.澄清石灰水 c.饱和小苏打溶液 d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000 mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如下图),碱石灰增重0.614 g。

①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________(填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
高三化学填空题中等难度题查看答案及解析
碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。

(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液 b.澄清石灰水 c.饱和小苏打溶液 d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000 mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如下图),碱石灰增重0.614 g。

①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________(填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
高三化学填空题中等难度题查看答案及解析
为了测定NaCl、Na2CO3·10H2O和NaHCO3的混合物中各组分的含量,某同学设计如下实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法错误的是

A. ①、②、③中可以依次盛装碱石灰、无水CaCl2、碱石灰
B. 硬质玻璃管加热前,应关闭b,打开a,缓緩通入空气,直至a 处出来的空气不再使澄清石灰水变浑浊为止
C. 若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大
D. 实验过程中一直通入空气,停止加热后再停止通入空气
高三化学单选题中等难度题查看答案及解析
下列实验过程中,始终无明显现象的是
A. NH3通人FeS04溶液中
B.C02通入CaCl2溶液中
C.A1C13溶液中滴入NaHC03溶液
D.S02通入Ba(N03)2溶液中
高三化学选择题简单题查看答案及解析
软锰矿的主要成分是MnO2,还含有少量重金属化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上采用同槽酸酸等工艺制备碳酸锰并回收硫酸铵,其主要流程如下:

(1)为了提高锰元素的浸出率,在“浸取”时可采取的措施有:
①适当升高温度:②搅拌:③ ____________等。
(2) “氧化”中加入MnO2发生反应的离子方程式为____________________________。
(3)“滤渣2”中主要成分的化学式为_____________________。
(4)“除重金属”时使用(NH4)2S而不使用Na2S的原因是_____________________。
(5)“50℃碳化”得到碳酸锰,反应的化学方程式为 _____________________。
(6)生成的碳酸锰产品需经充分洗涤,检验产品完全洗净的方法是_____________________。
高三化学简答题中等难度题查看答案及解析
软锰矿的主要成分是MnO2,还含有少量重金属化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上采用同槽酸浸工艺制备碳酸锰并回收硫酸铵,其主要流程如下:
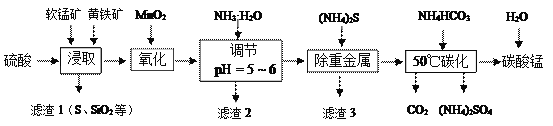
(1)为了提高浸出率,在浸取时可采取的措施有________。
A.适当升高温度 B.搅拌 C.矿石研成粉末 D.延长浸泡时间
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,浸取时发生反应的离子方程式是___________________________。
(3)加入MnO2氧化发生反应的离子方程式是___________________,还可使用______代替MnO2。
(4)滤渣2主要成分的化学式是________________。
(5)50℃碳化发生的化学反应方程式是______________________。
(6)加水洗涤,检验碳酸锰产品完全洗净的方法是___________________。
高三化学简答题困难题查看答案及解析