-
可逆反应2SO2(g)+O2(g) 2SO3(g)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
2SO3(g)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
(1)使用 V2O5 催化该反应时,涉及到催化剂 V2O5 的热化学反应有:
①V2O5 (s)+SO2 (g) V2 O4 (s)+SO3 (g) △H1=+59.6kJ·mol-1
V2 O4 (s)+SO3 (g) △H1=+59.6kJ·mol-1
②2V2O4(s)+O2(g) 2V2O5(s) △H2=-314.4kJ·mol-1
2V2O5(s) △H2=-314.4kJ·mol-1
则2SO2(g)+O2(g) 2SO3(g) △H3=_____,若降低温度,该反应速率会_____(填“增大”或“减小”)
2SO3(g) △H3=_____,若降低温度,该反应速率会_____(填“增大”或“减小”)
(2)向 10 L 密闭容器中加入 V2O4(s)、SO2(g)各 1 mol 及一定量的 O2,改变加入 O2 的量,在常温下反应一段时间后,测得容器中 V2O4、V2O5、SO2 和 SO3 的量随反应前加入 O2 的变化如图甲所示,图中没有 生成 SO3 的可能原因是____________________________________________________。
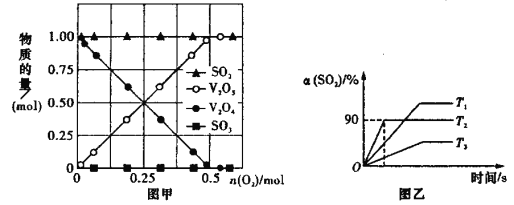
(3)向 10 L 密闭容器中加入 V2O5(s)、SO2(g)各 0.6mol,O2(g)0.3mol,保持恒压的条件下 分别在 T1、T2、T3 三种温度下进行反应,测得容器中 SO2 的转化率如图乙所示。
①T1 _____T2(填“>”或“<”)。
②T2时,2SO2(g)+O2(g) 2SO3(g)的平衡常数K=_____。若向该容器通入高温 He(g)(不参加反应,高于T2),SO3 的产率将______选填“增大”“减小”“不变”“无法确定”),理由是_____。
2SO3(g)的平衡常数K=_____。若向该容器通入高温 He(g)(不参加反应,高于T2),SO3 的产率将______选填“增大”“减小”“不变”“无法确定”),理由是_____。
③结合化学方程式及相关文字,解释反应为什么在 T3 条件下比 T2 条件下的速率慢:__________。
(4)T2 时使用 V2O5 进行反应:2SO2(g)+O2(g) 2SO3(g),在保证 O2(g)的浓度不变的条件下,增大容器的体积,平衡_____(填字母代号)。
2SO3(g),在保证 O2(g)的浓度不变的条件下,增大容器的体积,平衡_____(填字母代号)。
A.向正反应方向移动 B.不移动 C.向逆反应方向移动 D.无法确定
-
可逆反应2SO2(g)+O2(g) 2SO3(g)是硫酸工业的最重要反应,因该反应中使用催化剂而被命名为接触法制硫酸。
2SO3(g)是硫酸工业的最重要反应,因该反应中使用催化剂而被命名为接触法制硫酸。
(1)使用V2O5催化该反应时,涉及到催化剂V2O5的热化学反应有:
①V2O5(s)+SO2(g) V2O4(s)+SO3(g) △H1=+59.6kJ·mol-1
V2O4(s)+SO3(g) △H1=+59.6kJ·mol-1
②2V2O4(s)+O2(g) 2V2O5(s) △H2=-315.4kJ·mol-1
2V2O5(s) △H2=-315.4kJ·mol-1
则2SO2(g)+O2(g) 2SO3(g) △H3=__________kJ·mol-1
2SO3(g) △H3=__________kJ·mol-1
(2)向10 L密闭容器中加入V2O4(s)、SO2(g)各1 mol及一定量的O2,改变加入O2的量,在常温下反应一段时间后,测得容器中V2O4、V2O5、SO2和SO3的量随反应前加入O2的变化如图甲所示,图中没有生成SO3的可能原因是_________________________

(3)在原10 L的恒容装置中,加入V2O5(s)、SO2(g)各0.6 mol,O2(g)0.3 mol,分别在T1、T2、T3时进行反应,测得容器中SO2的转化率如图乙所示。
①T2时,2SO2(g)+O2(g) 2SO3(g)的平衡常数K=__________。
2SO3(g)的平衡常数K=__________。
②结合化学方程式及相关文字,解释反应为什么在T3条件下比T2条件下的速率慢:_____
(4)在温度T2使用V2O5进行反应:2SO2(g)+O2(g) 2SO3(g),在保证O2(g)的浓度不变的条件下,增大容器的体积,平衡__________(填字母代号)。
2SO3(g),在保证O2(g)的浓度不变的条件下,增大容器的体积,平衡__________(填字母代号)。
A.向正反应方向移动 B.向逆反应方向移动
C.不移动 D.无法确定
-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)⇌2SO3(g)△H<0
(1)该反应450℃时的平衡常数______500℃时的平衡常数(填“大于”、“小于”或“等于”).
(2)该化学达到平衡的标志是______.
a.v(O2)正=2v( SO3)逆 b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
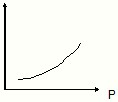
(3)恒温、密闭容器体系中充入一定量SO2、O2,反应达平衡时,某物理量随体系总压强(p)的关系如图所示所示.该物理量可能是______.
a.平衡体系中SO2的体积分数
b.气体的平均相对分子质量
c.混合气体的密度
d.平衡体系中SO2的转化率
(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10mol O2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=______ mol•L-1•min-1:若继续通入0.20mol SO2和0.10mol O2,则平衡______移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,______ mol<n(SO3)<______mol.
(5)压强及温度对SO2转化率的影响如表(原料气各成分的体积分数为:SO27%;O21l%;N2 82%);
| 压强转化率温度 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
利用表中数据分析.在实际生产中选择的适宜生产条件是:温度______℃,压强______MPa.
-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)⇌2SO3(g)+190kJ
1)该反应所用的催化剂是______ (填写化合物名称),该反应450℃时的平衡常数______ 500℃时的平衡常数(填“大于”、“小于”或“等于”).
2)该热化学反应方程式的意义是______.
3)对于反应2SO2+O2⇌2SO3(g),化学平衡状态的标志为______
a.v正(O2)=2v正(SO3)
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=______mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,则平衡______移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,______mol<n(SO3)<______ mol.
-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g) + O2(g) 2SO3(g) + 190 kJ
2SO3(g) + 190 kJ
(1)该反应的平衡常数表达式K =___________,该反应450℃时的平衡常数_________500℃时的平衡常数(填“>”“<”或“=”)。
(2)在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2) =____________mol/(L·min)
(3)请写出提高SO2转化率的两种方法__________________、___________________。
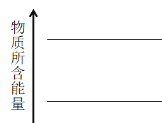
(4)根据反应方程式,请在图中,绘制反应方向箭头,并在合适位置标明物质与热量 ___________。
(5)将SO2与SO3的混合气体持续通入一定量的NaOH溶液中,产物中某离子的物质的量浓度与通入气体的体积有如图所示关系,该离子是______________。

-
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)⇌2SO3(g);△H=-190KJ/mol
(1)该反应的平衡常数表达式是________,该反应450℃时的平衡常数________ 500℃时的平衡常数(填“大于”、“小于”或“等于”).
(2)说明反应达到平衡状态是________.
a. V(O2)正=2V(SO3)逆 b.ひ(SO2)正׃ひ(O2)逆=2:1
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
e.容器中气体的平均分子量不随时间而变化
(3)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则V(O2)=________mol.L-1.min-1:若继续通入0.30mol SO2和0.15mol O2,则平衡________移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol<n(SO3)<________mol.
-
钒(V)及其化合物在工业催化、新材料和新能源等领域中有广泛的应用,其中接触法制硫酸工业中就要用到V2O5作催化剂:
2SO2(g)+O2(g)  2SO3(g) ΔH<0。
2SO3(g) ΔH<0。
某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,在V2O5作催化剂下经5min反应达平衡,SO2的平衡转化率(α)为80%。
(1)5min内 v(SO3 )= mol·L-1·min-1
(2)该温度下平衡常数K=
(3)若缩小容器体积,至达到新的平衡,在图中画出反应速率变化图象。

(4)硫酸工业尾气SO2用浓氨水吸收,反应的离子方程式是 ,吸收后的产物最终可制成肥料硫铵[即(NH4)2SO4]。
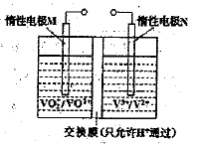
(5)某含钒化合物及硫酸的电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如下图所示。

①用该电池电解(NH4)2SO4溶液生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极电极反应式可表示为 ;若电解得1mol(NH4)2S2O8,则电池左槽中H+将 (填“增大”或“减少”) mol。
②电池使用一段时间后对其进行充电,充电过程中,阳电极反应式为: 。
-
(18分)钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。
(1)V2O5是接触法制硫酸的催化剂。 ’
①已知25℃.10lkPa时:
2SO2(g)+O2(g)+2H2O(1)=2H2SO4(1) △H = -457kJ·mol-l
SO3(g)+H2O(1)=H2SO4(1) △H= -130kJ·mol-l
 则反应2SO2(g)+O2(g) 2SO3(g)的△H= kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能 (填“增大”、“不变”或“减小”)。
则反应2SO2(g)+O2(g) 2SO3(g)的△H= kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能 (填“增大”、“不变”或“减小”)。
②SO2水溶液可与SeO2反应得到硫酸,当有79gSe生成时,转移电子的物质的量为 mol,此反应的化学方程式是 。
(2)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO42-。电池放电时,负极的电极反应为:
V2+-e一=V3+。
①电池放电时的总反应方程式为 。
充电时,电极M应接电源的 极。
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+。则第一步反应过程中阴极区溶液n(H+) (填“增大”、“不变”或“减小”),阳极的电极反应式为: 。
-
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。
(1)V2O5是接触法制硫酸的催化剂。
①已知25℃,10lkPa时:
2SO2(g)+O2(g)+2H2O(1)=2H2SO4(1) △H = -457kJ·mol-l
SO3(g)+H2O(1)=H2SO4(1) △H= -130kJ·mol-l
则反应2SO2(g)+O2(g) 2SO3(g)的△H=_______kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能______(填“增大”、“不变”或“减小”)。
2SO3(g)的△H=_______kJ·mol-l。使用V2O5作催化剂后该反应逆反应的活化能______(填“增大”、“不变”或“减小”)。
②SO2水溶液可与SeO2反应得到硫酸,当有79gSe生成时,转移电子的物质的量为______mol,此反应的化学方程式是___________________________。
(2)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO42-。电池放电时,负极的电极反应为:V2+-e一=V3+。
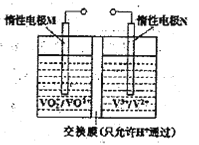
①电池放电时的总反应方程式为____________。充电时,电极M应接电源的____________极。
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+。则第一步反应过程中阴极区溶液n(H+)______(填“增大”、“不变”或“减小”),阳极的电极反应式为:_______________。
-
2SO2(g)+O2 (g)  2SO3 (g)是制备硫酸的重要反应。下列叙述正确的是
2SO3 (g)是制备硫酸的重要反应。下列叙述正确的是
A.催化剂V2O5增加该反应的正反应速率而不改变逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.进入接触室的SO2和空气必须进行净化,且该反应不需要在高压下进行
D.该反应是放热反应,降低温度将缩短反应达到平衡的时间
2SO3(g)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
V2 O4 (s)+SO3 (g) △H1=+59.6kJ·mol-1
2V2O5(s) △H2=-314.4kJ·mol-1
2SO3(g) △H3=_____,若降低温度,该反应速率会_____(填“增大”或“减小”)

2SO3(g)的平衡常数K=_____。若向该容器通入高温 He(g)(不参加反应,高于T2),SO3 的产率将______选填“增大”“减小”“不变”“无法确定”),理由是_____。
2SO3(g),在保证 O2(g)的浓度不变的条件下,增大容器的体积,平衡_____(填字母代号)。






