-
Al及其化合物在现代工业中有广泛的用途。回答下列问题:
(1)下列状态的铝中,电离最外层的一个电子所需能量最小的是_____(填标号)。
A [Ne]3s1 B [Ne]3s2 C [Ne]3s23p1 D [Ne] 3s13p2
(2)熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为_____(标出配位键);其中Al的配位数为_________。二聚体A12C16中Al原子的轨道杂化类型是________。
(3) 实际上,偏铝酸钠在水溶液中都是以Na[Al(OH)4]和形式存在,1mol Na[Al(OH)4]中含有σ键的数目为_________。
(4)Ga(镓)和铝是同一主族元素,Ga原子的电子排布式是___________。
高二化学综合题中等难度题查看答案及解析
-
第IIA族元素在地壳内蕴藏较丰富,其单质和化合物用途广泛。回答下列问题:
(1)基态Ca原子M能层有_______个运动状态不同的电子,Mn和Ca属于同一周期,且核外最外层电子构型相同,但金属Mn的熔沸点等都比金属Ca高,原因______。
(2)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,Ca(ClO3)2中的阴离子空间构型是_________,中心原子的杂化方式为_______。
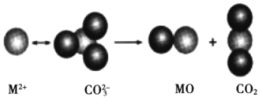
(3)碳酸盐的热分解示意图如下图所示。热分解温度:CaCO3__________(填“高于”或“低于”)SrCO3,原因是_______。从成键轨道看,CO2分子内的化学键类型有________。
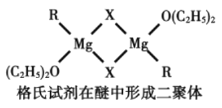
(4)格氏试剂RMgX是镁和卤代烃反应的产物,它在醚的稀溶液中以单体形式存在,在浓溶液中以二聚体存在,二聚体结构如下图所示。请在图中标出二聚体中的配位键__________。
高二化学综合题中等难度题查看答案及解析
-
铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态铜原子价电子排布式为____________;第一电离能I(Cu)________I (Zn)(填“>”或“<”)
(2)配合物[Cu (CH3CN) 4] BF4[四氟硼酸四(乙腈)合铜(Ⅰ)]是有机合成中常见催化剂。
①该配合物中阴离子的空间构型为__________,与其互为等电子体的分子或离子是________(各举1例)。
②配体分子中与Cu(I) 形成配位键的原子为____________;配体CH3CN 中:碳原子杂化方式是______。
(3)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,Cu2O 属于____晶体,前者熔点较高,其原因是______________________________________________________________________________
(4)Cu3N 的晶胞(立方)结构如下图所示:
①距离最近的两个Cu+间的距离为________nm。(保留两位小数)
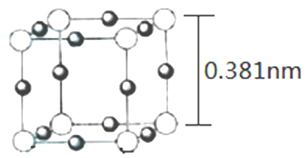
②Cu3N 晶体的密度为____________ g·cm-3。(列出计算式,不必计算出结果)
高二化学综合题困难题查看答案及解析
-
氮的化合物在农药生产及工业制造业等领域用途非常广泛,请根据提示回答下列相关问题:
(1)基态氮原子的电子排布式为____,碳、氮、氧元素的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)NH4Cl中阳离子的空间构型为______,与NH4+互为等电子体的一种非极性分子的化学式为________。
(3)NH4Cl受热易分解产生氨气,向CuSO4溶液中通入氨气至过量,产生蓝色沉淀,随后沉淀溶解得到深蓝色溶液,该溶液中存在的配离子的结构式为_______(配位键用→表示)。
(4)GaAs与GaN均为原子晶体,GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为_________。
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_______。已知GaAs的密度为ρ g/cm3,Ga和As的摩尔质量分别为 MGa g/mol和MAsg/mol,阿伏伽德罗常数的值为NA,则GaAs晶胞中Ga之间的最短距离为_______pm(写出表达式)。

高二化学综合题中等难度题查看答案及解析
-
铜及其化合物在生产生活中用途广泛。回答下列问题:
(1)目前,低压甲醇铜基催化剂的主要组分是CuO、ZnO和Al2O3,下列氧原子电子排布图表示的状态中,能量最高的是__(填序号)。
A.
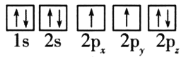 B.
B.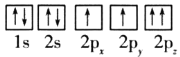
C.
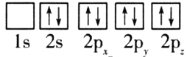 D.
D.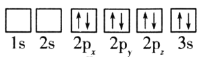
(2)铜离子是人体内多种酶的辅因子,某化合物与Cu+结合形成如图所示的离子。
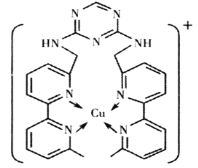
①该离子中含有化学键的类型有___(填序号)。
A.极性键 B.离子键 C.非极性键 D.配位键
②H、N、Cu三种元素的电负性由大到小的顺序是___。H、N、Cu三种元素形成单质其熔点由低到高顺序为___。
(3)某磷青铜晶胞结构如图所示:

①其中原子坐标参数A为(0,0,0);B为(0,
,
)。则P原子的坐标参数为___。
②该晶体中距离Cu原子最近的Sn原子有__个,这些Sn原子所呈现的构型为___。
高二化学综合题简单题查看答案及解析
-
(16分)镁化合物和氯气均具有广泛用途,请回答下列问题:
(1)写镁和氯气反应产物的电子式________
(2)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。则下列选项中正确的是________
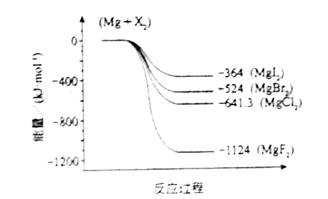
A MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
B Mg与X2的反应是放热反应
C MgBr2与Cl2反应的△H<0
D 化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
(3)在298K、100Kpa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
① 该反应的离子方程式为________,平衡常数表达式为________
②在上述平衡体系中加入少量NaCl固体,平衡将________(填“正向移动”、“逆向移动”、“不移动”);增大氯气的压强,氯气的溶解度将________ ,氯气和水反应的平衡常数将________
________(填“变大”、“变小”、“不变”)。
③已知: H2CO3
HCO3- + H+ Ka1(H2CO3) = 4.45×10-7
HCO3-
CO32- + H+ Ka2(H2CO3) = 5.61×10-11
HClO
H+ + ClO- Ka(HClO) = 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
将少量的氯气通入到过量的碳酸钠溶液中____________________________________;
高二化学填空题简单题查看答案及解析
-
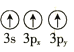
下列状态的铝元素中,电离最外层的一个电子所需能量最小的是
A. [Ne]
B. [Ne]
C.[Ne] D. [Ne]
高二化学单选题简单题查看答案及解析
-
铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1) Fe2+的最外层电子排布式____________。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______I3(Mn)(填“>”、“<")。
(2)气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为__________。根据等电子原理,AlO2-的空间构型为_____。
(3) Fe(CO)5的熔点为-20 ℃,沸点为103 ℃,易溶于乙醚,其晶体类型为______,
(4) 科学家们发现某些含铁的物质可催化尿素合成肼(N2H4),沸点:N2H4>C2H6的主要原因为______________________。
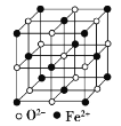
(5) FeO晶体的晶胞如图所示,己知:FeO晶体的密度为ρ g/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-最短核间距为______pm(用ρ和NA表示)。
高二化学综合题中等难度题查看答案及解析
-
铜、锌及其化合物用途广泛。回答下列问题:
(1)Zn2+的价层电子轨道表达式为__。
(2)元素第二电离能(I2):Zn_Cu(填“>”“<”或“=”)。
(3)卤化锌的熔点如表所示:
ZnF2
ZnCl2
ZnBr2
ZnI2
溶点/℃
872
275
394
446
①ZnCl2、ZnBr2、ZnI2的熔点呈表中变化规律的原因___。
②ZnF2的熔点远高于其它三种卤化锌,其原因为___。
(4)邻氨基吡啶(
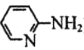 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
①邻氨基吡啶的铜配合物中,C原子杂化类型为__。
②1mol
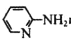 中σ键和π键的数目之比为__。
中σ键和π键的数目之比为__。(5)铜的晶胞为面心立方(如图所示),已知晶胞参数为a,则该晶胞的空间利用率为__。(圆周率为π)。
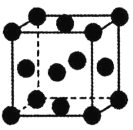
高二化学综合题中等难度题查看答案及解析
-
铝广泛应用于航空、建筑、汽车等行业,目前工业上采用电解氧化铝和冰晶石混合物的方法制取铝。回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.
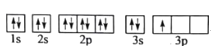
B.
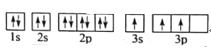
C.
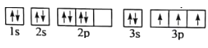
D.
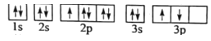
其中能量最低的是____(填字母),电子由状态C到状态B所得原子光谱为____光谱(填“发射”或“吸收”) ,状态D是铝的某种激发态,但该电子排布图有错误,主要是不符合_____。
(2)熔融态氯化铝可挥发出二聚分子Al2Cl6,其结构如图所示。
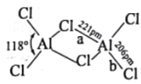
①a键的键能_____b键的键能(填“>”“<”或“=”),其理由是_______。
②Al2Cl6中铝原子的杂化方式为___;AlCl3的空间结构为______。
(3)冰晶石属于离子化合物,由Na+和AlF63−组成,在冰晶石的晶胞中,AlF63−占据的位置相当于氯化钠晶胞中Cl−的位置。
①冰晶石的化学式为_____,一个冰晶石晶胞中Na+的个数为_____。
②已知冰晶石的密度为2.95 g/cm3,则冰晶石晶胞的边长a=____pm(列出算式即可,阿伏加德罗常数值为6.02×1023)。
高二化学填空题简单题查看答案及解析