-
X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比p电子数多3个,Y、Z间形成的某种化合物是一种常用的漂白剂、供氧剂,R和Z位于同一周期且基态原子中有3个电子能量最高,M2+与过量氨水作用先得到蓝色沉淀,后转化为深蓝色溶液Q。请回答下列问题:
(1)基态M2+的核外电子排布式为__,Y、Z、R、M四种元素的第一电离能由大到小的顺序为__(用元素符号表示)。
(2)化合物XCl3的中心原子的杂化类型为__,RCl3的立体构型为__,XCl3、RCl3分子中属于非极性分子的是__;导致Q溶液显色的粒子中存在的化学键类型有__与配位键。
(3)已知H2Y2的熔点为-0.43℃、沸点为158℃,RH3的熔点为-133℃、沸点为-87.7℃,但H2Y2、RH3的相对分子质量相同,其主要原因是__。
(4)X、R两元素可形成一种具体立体网状结构的化合物,其晶胞结构如图所示。
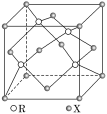
①该化合物的晶体类型是__,该晶体的化学式为___。
②设两个X原子最近距离为apm,列式计算该晶胞的密度ρ=__g·cm-3。
-
短周期元素X、Y、W、R的原子序数依次增大。 元素X是形成化合物种类最多的元素,Y、R同主族,R原子的最外层电子数是内层电子总数的一半, W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是
A.X、W、R的最高价氧化物的水化物酸性强弱顺序是X<W<R
B.气态氢化物的稳定性:Y>R
C.X、Y、W、R的原子半径由大到小的顺序为R﹥ W﹥ X﹥Y
D.X、W的氧化物由固态转化为气态时,克服相同的作用力
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是( )
A.原子半径:C>D>A>B
B.C和E的单质可通过电解饱和的CE水溶液获得
C.C与B形成的两种化合物中化学键类型完全相同
D.A、D、E的最高价氧化物对应水化物的酸性逐渐增强
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是
A. 原子半径:C>D>A>B
B. C和E的单质可通过电解饱和的CE水溶液获得
C. C与B形成的两种化合物中化学键类型完全相同
D. A、D、E的最高价氧化物对应水化物的酸性逐渐增强
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是
A.原子半径:C>D>A>B
B.C和E的单质可通过电解饱和的CE水溶液获得
C.C与B形成的两种化合物中化学键类型完全相同
D.A、D、E的最高价氧化物对应水化物的酸性逐渐增强
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是
A.原子半径:C>D>A>B
B.C和E的单质可通过电解饱和的CE水溶液获得
C.C与B形成的两种化合物中化学键类型完全相同
D.A、D、E的最高价氧化物对应水化物的酸性逐渐增强
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E的两倍。D与C形成的化合物是一种耐高温材料,A、B形成的气态化合物常用作制冷剂。下列说法正确的是( )
A. 原子半径: E>D>C>B>A B. 单质D可用海水作原料获得
C. 热稳定性:EA4>A2C D. 化合物DC 与化合物EC2中化学键类型相同
-
己知A、B、C、D、E是短周期中原子序数依次增大的五种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是
A. 原子半径:C>D>B>A
B. A、D、E的最高价氧化物对应水化物的酸性逐渐增强
C. C与B形成的两种化合物均属于离子化合物,且化学键类型完全相同
D. B的单质比A的单质更易与氢气化合
-
短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子最外层电子数是内层的2倍,Y是地壳中含量最高的元素,Y与Z形成的化合物能与NaOH溶液反应,其生成物是常用防火材料。X、Y、Z、W最外层电子数之和为19。下列说法错误的是
A. 常温常压下X的单质为固态
B. 原子半径:r(Z)>r(W)>r(Y)
C. Y的简单气态氢化物的热稳定性比Z的氢化物强
D. W的最高价氧化物对应的水化物是强酸
-
短周期元素A、B、C、D、E的原子序数依次增大,A元素阳离子的原子核外没有电子,B是空气中含量最多的元素;C元素原子最外层电子数是其电子层数的三倍;C与D可形成两种常见的离子化合物;工业上常用电解C与E的化合物来制备E单质。
(1)C、D、E的简单离子半径由小到大的顺序 (用离子符号表示)。
(2)工业上常用A和B的单质合成一种常见气体,该气体的电子式 。检验该气体的常用方法是 。
(3)D2C2与H2O反应的化学方程式是 ,D2C2与CuSO4溶液反应的现象是 。(4)A、B、C三种元素可组成一种常见离子化合物,其水溶液呈酸性,该溶液中离子浓度由大到小的顺序是 。
(5)电动汽车的某种燃料电池,通常用NaOH作电解质,用E单质、石墨作电极,在石墨电极一侧通入空气,该电池的负极反应: 。
