-
(6分)①~⑤五种元素在元素周期表中的位置如下图所示:回答下列问题:
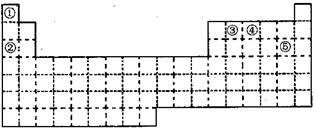
(1)①~⑤五种元素中,非金属性最强的元素在周期表中的位置是________;
(2)②③④元素原子中,半径最小的是________(填元素符号);
(3)元素①和③可以形成众成多的化合物,其中最简单的是________ (化学式)。该化合物中,化学键的类型为________(选填“极性共价键”、 “非极性共价键”或“离子键”);
(4)元索④的最高价氧化物对应水化物能与其最低价的气态氢化物发生反应,产物是
________(化学式);
(5)元素⑤单质与水反应的离子方程式:________ 。
-
①~⑤五种元素在元素周期表中的位置如下图所示:

回答下列问题:
(1)①~⑤五种元素中,非金属性最强的元素在周期表中的位置是___________;
(2)②③④元素原子中,半径最小的是_________(填元素符号);
(3)元素①和③可以形成众成多的化合物,其中最简单的是_____(化学式)。该化合物中,化学键的类型为_________(选填“极性共价键”、 “非极性共价键”或“离子键”);
(4)元素④的最高价氧化物对应水化物能与其最低价的气态氢化物发生反应,产物是________(化学式);
(5)元素⑤单质与水反应的离子方程式:________________________________。
-
下图为周期表的一部分,元素①~⑨在元素周期表中的位置如下:
请回答下列问题:
(1)表中化学性质最稳定的元素是____(填元素符号);
(2)非金属性最强的元素是____(填元素符号);
(3)元素⑧的元素符号为____,在周期表中的位置是____;
(4)元素③的最高价氧化物对应水化物中含有的化学键类型为____;
(5)比较元素⑤、⑥的简单氢化物的稳定性____(用化学式表示);比较元素⑤、⑥的最高价氧化物对应水化物的酸性强弱____(用化学式表示);
(6)设计实验比较元素⑥、⑧的非金属性强弱____。
-
现有a~i 9种短周期元素,它们在同期表中的位置如下,请据此回答下列问题:(请用具体的元素符号及化学用语作答)
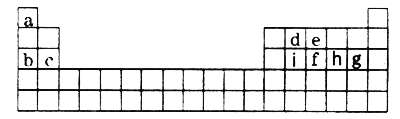
(1)a~i元素中,金属性最强的是________,最高价氧化物对应水化物中,酸性最强的物质是___________。g所在族的元素形成的氢化物中沸点最低的是____________________。
(2)比较b、e、g简单离子半径的大小___________________(用离子符号作答)。
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式__________________、___________________。
(4)用一个化学反应方程式表示d的非金属性强于i_______________________________。
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是______(填序号)。
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号_________;镓(Ga)与As同周期,最外层有3个电子,Ga与As可以形成一种新型化合物半导体材料,其性能更优越。这种新型化合物化学式为____________________。
(6)c与a形成的化合物的电子式为___________,用电子式表示a与h形成a2h的过程__________________________________________。
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式_________________________________。
-
I.根据所学知识,回答下列问题:
(1)元素周期表1~20号元素中,金属性最强的元素是______(填元素符号,下同);属于稀有气体的是_________;非金属性最强的元素在周期表中的位置是__________________。
(2)己知NO2和N2O4之间发生可逆反应:2NO2(g)(红棕色) N2O4(g)(无色)。将装有NO2和N2O4混合气体的烧瓶浸入热水中,观察到的现象是_______,产生该现象的原因是________。
N2O4(g)(无色)。将装有NO2和N2O4混合气体的烧瓶浸入热水中,观察到的现象是_______,产生该现象的原因是________。
(3)一定条件下,向2L恒容密闭容器中按体积比1:3充入4.48L(标准状况)N2和H2的混合气体,发生反应N2(g)+3H2(g) 2NH3(g),5min时反应达到平衡状态,测得c(N2)=0.02mol/L。
2NH3(g),5min时反应达到平衡状态,测得c(N2)=0.02mol/L。
①0~5min内,v(NH3)=_______________。
②下列叙述可证明上述反应达到平衡状态的是________(填序号)。
a.V(H2)=3v(N2)
b.容器内压强保持不变
c.每消耗ImolN2,同时生成2molNH3
d.N2、H2和NH3的物质的量浓度不再变化
II.五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C的简单离子和B的简单离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物中阴阳离子的个数比为1:1。回答下列问题:
(1)五种元素中,原子半径最大的是______(填元素名称),非金属性最强元素的是_________。
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是_____(用化学式表示)。
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为______,其中存在的化学键类型为______________。
(4)E离子的结构示意图是____________;元素D最高价氧化物的水化物的化学式为_____。
(5)单质E与水反应的离子方程式为__________________。
-
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
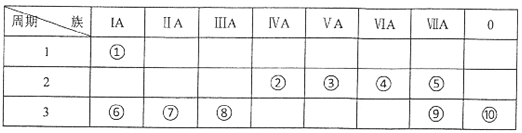
(1)化学性质最稳定的元素是_____(填元素名称),非金属性最强的元素是_____(填元素符号)。
(2)图中标出的元素最高价氧化物对应的水化物中,碱性最强的是_____(用化学式回答,下同),写出该水化物与⑧的最高价氧化物反应的离子方程式________________。
(3)④与⑥按照原子个数比 1:1形成的化合物中,化学键类型为_____,其电子式为_____。
(4)①与③形成的原子个数比为3:1的化合物的结构式为_____;⑤、⑨的氢化物的沸点由高到低的顺序为_____。
(5)③可以形成多种氧化物,其中一种是红棕色气体,试用化学方程式说明该气体不宜采用排水法收集的原因_____。
(6)利用如图装置可验证同主族元素非金属性的变化规律
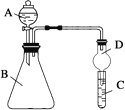
①仪器A的名称为_____;干燥管D的作用为_____;
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(已知KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,如果试管C中溶液变蓝,即可证明。
写出试管C中发生反应的离子方程式:_____。
-
下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,用相应的化学用语回答下列问题;
(1)表中用序号标出的10种元素中,非金属性最强元素的离子结构示意图是____________。
(2)④、⑦、⑩的离子半径由大到小的顺序为____________(用元素符号作答)。
(3)由表中④、⑥元素可以组成一种淡黄色的物质,画出该物质的电子式____________,该物质含有的化学键类型有____________。
(4)元素②的简单气态氢化物为X,0.1molX完成燃烧生成稳定氧化物时放出akJ的能量,写出X燃烧热的热化学方程式:____________。
(5)写出实验室制备氨气的反应方程式____________。
(6)一种氢气燃料电池的原理如图:
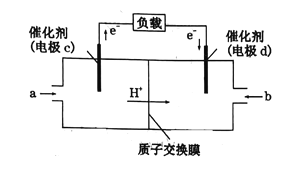
a极通入的气体是____________,正极的电极反应式为____________。
-
下表是元素周期表中的一部分元素,用元素符号或化学式回答下列问题:
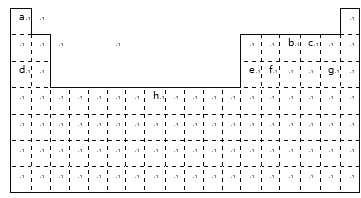
(1)h元素在周期表中的位置是_______;
(2)表中所列元素中,金属性最强的是____;元素最高价含氧酸酸性最强的是____;(填化学式)
(3)c、d、e、g中,离子半径最小的是____;(填离子符号)
(4)a和b化合时形成_____键;a和d化合时形成______键;
(5)由a、c、d形成的化合物的电子式为__________。
-
下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
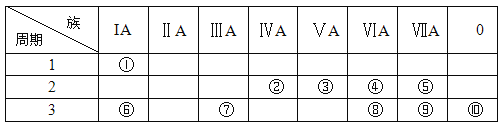
(1)非金属性最强的是___(填元素名称),化学性质最不活泼的是____(填元素符号)。
(2)元素①-⑩中半径最大的元素是____(填元素符号)
(3)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是________。(填化学式)
(4)表中能形成两性氢氧化物的元素是______(填元素符号)
-
下表列出了①~⑥六种元素在元素周期表中的位置。
 [
[
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是____(填写元素符号);
(2)元素⑥的气态氢化物的分子式是____;
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是____________________________。








 [
[